临床大队列蛋白质组学整体解决方案助力精准诊疗
临床大队列蛋白质组学整体解决方案助力精准诊疗


在精准医学和大数据时代、人工智能的大背景下,高通量大队列样本组学(Omics)研究在生命科学研究以及在临床病理研究、临床诊疗领域得到广泛应用。蛋白质作为生命活动和功能的直接执行者,在研究生理、病理机制以及临床诊断、预后评估、治疗靶点以及药物靶点研究中扮演着重要角色。蛋白质组学大队列样本在临床诊疗、疾病机制研究中的应用受到科学家的广泛关注。
然而,制约大队列样本蛋白质组学技术的两大因素极大地限制了其应用,一是针对大样本质谱检测的机时问题以及由此带来的批次效应(质谱长时间运行导致其性能下降,样品间的仪器误差增大),二是对复杂的大样本数据的深度挖掘。金开瑞针对这两个问题专门开发了包含蛋白质组学技术服务、大数据深度挖掘和标志物深度验证三大模块的临床大队列样本蛋白质组学整体解决方案,为科研工作者提供专业、全方位的技术服务。


1. 蛋白质组学技术


2. 大数据深度挖掘
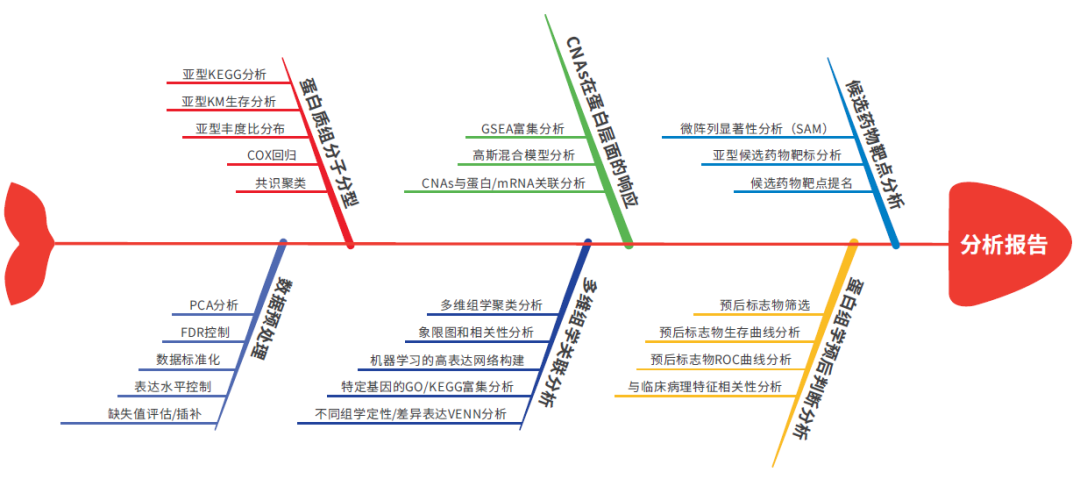

3. 疾病标志物验证
通过高通量、大规模蛋白质组学技术及生物信息学、统计学等手段,可以筛选到部分候选蛋白标志物,其表达量往往在疾病/正常样本中具有明显的差异。但是,仅仅通过蛋白质组学手段不足以确定,还需要进行进一步验证和确证[1](下图)。金开瑞拥有成熟的抗体制备平台、Wester Blot实验平台、免疫组织化学平台和ELISA制备平台,为您提供完整的标志物各阶段验证实验。
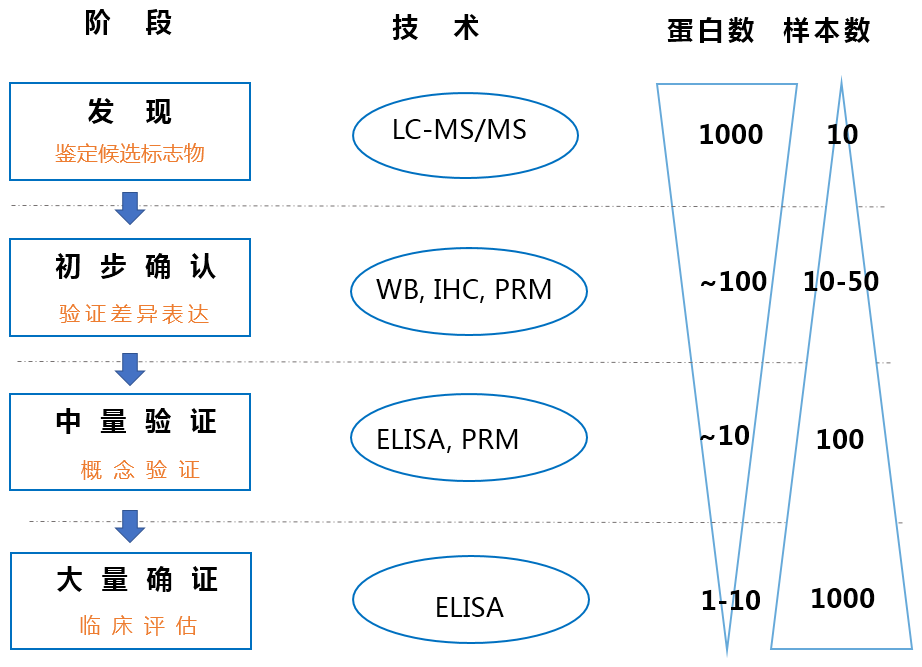
标志物筛选的四个步骤


1. microflow-LC技术[2-5]
微流控液相色谱-质谱(microflow-LC MS/MS)系统由于其大流速、粗管路的特点,具有耐脏、高稳定性、短梯度等优势,在处理大队列样本过程,可大大降低质谱数据采集过程的偏差,提升队列数据的整体质量。具体表现为如下优势:
-
大幅缩短检测周期。处理100例样本,传统LC-MS/MS系统大约需12天左右,采用micro-SWATH仅需5天即可完成。
-
有效降低批次效应。得益于微流控系统的高稳定性和短梯度等特点,microflow系统在处理大队列样本时表现出卓越的一致性,几乎无批次偏倚。
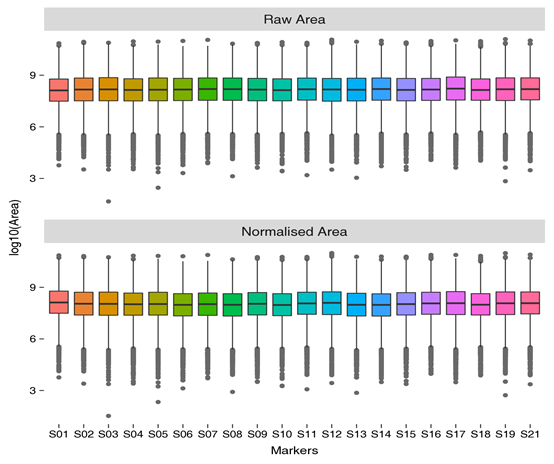
定量结果表现出良好的一致性(20例人血浆样本)
-
极大提升定量准确性。microflow针对大样本定量检测表现出极佳的准确性,样品间的相关系数普遍在0.9以上。
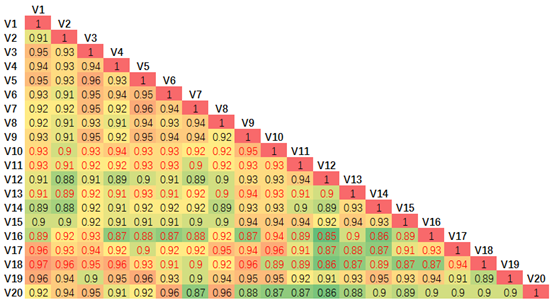
microflow-SWATH结果表现出良好的相关性(20例血浆样本)

2. 数据分析整体解决方案
在精准医学和大数据时代、人工智能的大背景下,大队列样本的数据分析成为科学家关注的重点,也是难点。通过调阅相关CNS文献报道,结合蛋白质组学数据本身特点,我们开发了一套专门针对临床疾病(尤其是肿瘤)的大队列数据分析方案,充分挖掘大数据中隐藏的信息,为临床诊断、治疗及疾病机制研究提供可靠的证据。
-
数据预处理保证数据质量。三大维度预处理,保证高可靠、高质量数据[6]。
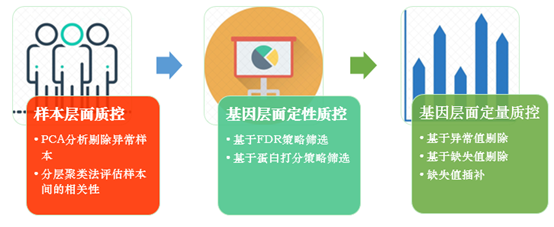
三大维度数据质量控制,确保数据的高质量
-
分子分型助力精准诊疗。蛋白质层面的分子分型可以帮助临床医生更准确地识别不同类型的肿瘤,确定精准的治疗方案,更加适合指导肿瘤患者用药、治疗,预后评估,并通过功能分析以及生存分析发现在通路富集和总体生存率层面蛋白分子水平分型是否存在显著差异,进一步证实根据蛋白质进行分类的科学性。是肿瘤分子分型的又一大热点[7]。
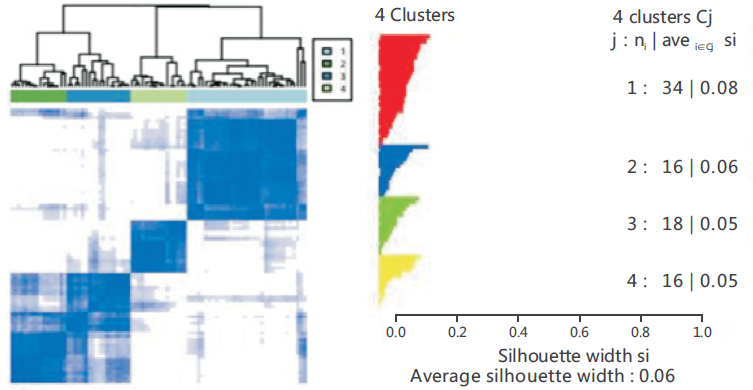
共识聚类的凭据共识矩阵和轮廓距离确定最佳分类数
-
多组学整合分析揭示病理机制。尽管目前的研究结果显示转录组和蛋白质组表达趋势相关性较差,但mRNA和蛋白作为基因表达的共同产物,在某种程度上必然存在因果关系或相关关系。我们通过分子分型结果,对两组学数据进行进一步细化、关联,从而得到常规关联分析所不能获得的信息,并结合差异表达分析,深入挖掘关键功能模块,探索疾病病理机制。除此之外,我们也开发了CNV/SNP对蛋白质表达/功能影响的相关算法,旨在研究基因层面突变对蛋白功能的影响[8]。
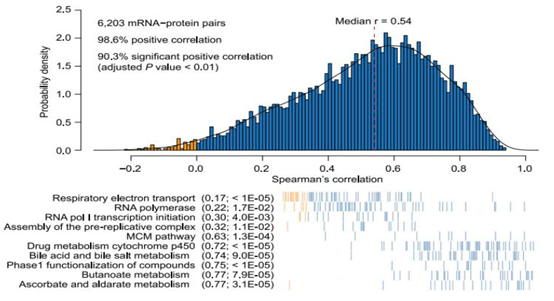
蛋白质组和转录组表达水平相关性分析
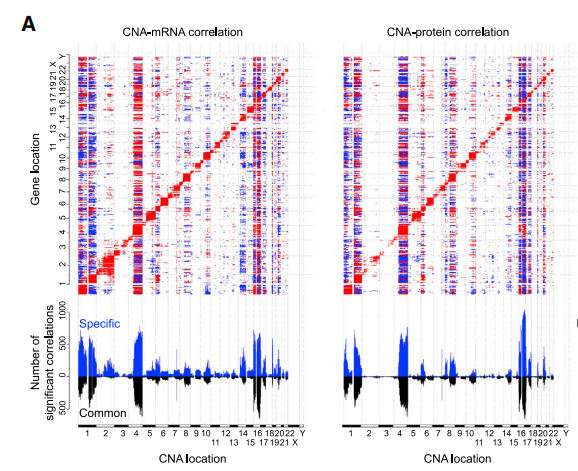
CNV和蛋白质/mRNA表达水平相关性分析
-
预后标志物筛选实现精准诊断。使用合理的描述性统计学和相关性分析等手段,经过严格的筛选标准,最终通过Cox回归模型分析影响患者生存预后的因素,结合变化倍数,可挖掘出针对肿瘤不同分子型的特异性表达蛋白,并通过KM生存曲线分析判断是否为预后不良病例的特异性蛋白标志物[8]。
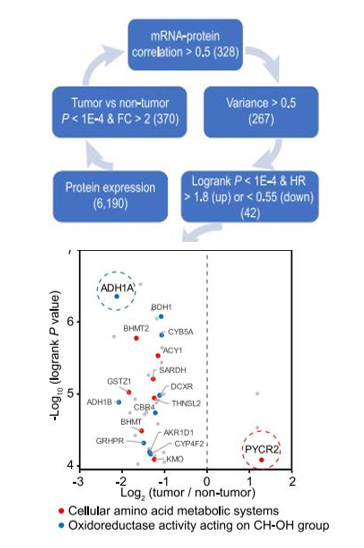
标志物筛选的基本流程
-
候选药物靶点提名实现精准用药。基于蛋白质组学及蛋白质组学分型结果,结合是否为已知临床药物靶点,可以针对肿瘤或特定分子型筛选具有药物靶点潜能的显著差异蛋白,从而达到精准用药[9]。
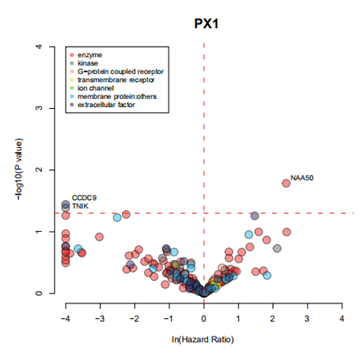

3. 标志物验证和确证
蛋白质标志物的鉴定往往需要经过四个阶段:a) 发现阶段,通过大队列样本蛋白质组学的Discovery 策略,结合数据的深度挖掘,最终选定上百种候选标志物蛋白进行进一步验证;b) 差异表达验证,经过此阶段,一般最终筛选到几十种蛋白符合预期;c) 概念阶段验证,进而实现临床疾病诊断、治疗的医学转化。金开瑞可提供多种蛋白质定性、定量验证手段。
-
基于质谱PRM验证。通过高分辨质谱对靶蛋白-肽段的特异识别检测,可实现蛋白的精确定量,具有通量高、定量准确的优势,一次可同时验证上百种蛋白标志物;
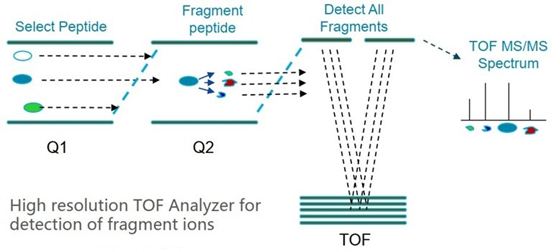
PRM验证的基本原理
-
基于Western blot验证。制备候选靶点蛋白的单多克隆抗体,基于抗原抗体的特异性反应实现对样本中目标蛋白的定性/半定量检测。验证过程中可选择多例表型差异的样品进行平行检测,通过识别信号的强弱及灰度分析值进一步判断靶点蛋白作为候选靶标的准确性。
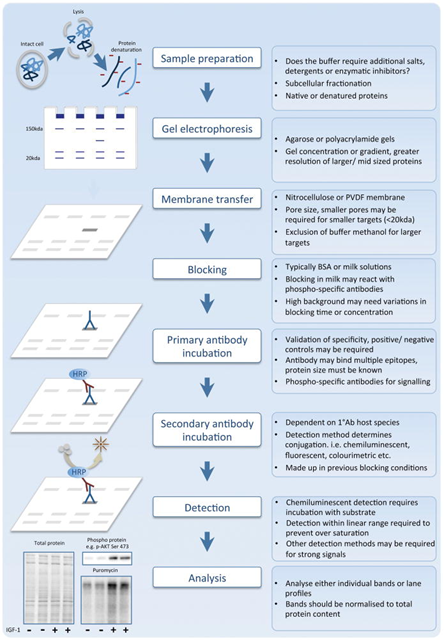
Western blot验证的基本原理
-
基于IHC验证。制备候选靶点蛋白的单多克隆抗体,基于抗原抗体的特异性反应实现对样本中目标蛋白的定性/半定量检测。区别于WB,IHC更侧重靶点蛋白的亚细胞定位,对特异性进一步做了补充,着色深浅跟目标蛋白的含量呈正相关。
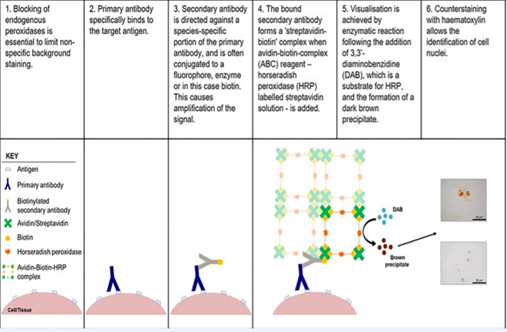
immunochemistry验证的基本原理
-
基于Sandwich ELISA验证。ELISA的基础是抗原或抗体的固相化及抗原或抗体的酶标记,受检标本加入后,与固相载体表面的抗原或抗体起反应,再加入酶反应的底物后,底物被酶催化成为有色产物,产物的量与标本中受检物质的量直接相关,根据呈色的深浅进行定性或定量分析。对于大分子的靶标蛋白检测,通常是基于夹心ELISA原理进行定量检测产品的开发,这一步主要是扩大测样通量,以满足诊断级别的样本检测例数,同时对靶标蛋白进行绝对定量。
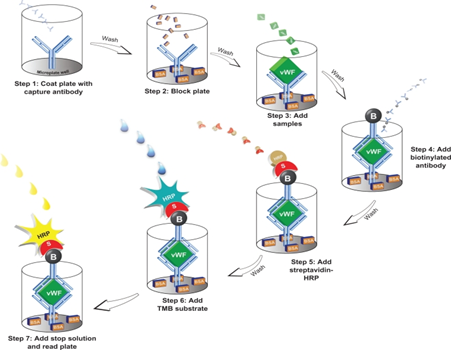
Sandwich ELISA验证的基本原理

1. Del Campo, M., et al., Facilitating the Validation of Novel Protein Biomarkers for Dementia: An Optimal Workflow for the Development of Sandwich Immunoassays. Front Neurol, 2015. 6: p. 202.
2. Broccardo, C.J., et al., Multiplexed analysis of steroid hormones in human serum using novel microflow tile technology and LC-MS/MS. J Chromatogr B Analyt Technol Biomed Life Sci, 2013. 934: p. 16-21.
3. Sun, R., et al., Accelerated Protein Biomarker Discovery from FFPE Tissue Samples Using Single-Shot, Short Gradient Microflow SWATH MS. J Proteome Res, 2020. 19(7): p. 2732-2741.
4. Needham, S.R., Microspray and microflow liquid chromatography: the way forward for LC-MS bioanalysis. Bioanalysis, 2017. 9(24): p. 1935-1937.
5. Distler, U., et al., Enhancing Sensitivity of Microflow-Based Bottom-Up Proteomics through Postcolumn Solvent Addition. Anal Chem, 2019. 91(12): p. 7510-7515.
6. Gillette, M.A., et al., Proteogenomic Characterization Reveals Therapeutic Vulnerabilities in Lung Adenocarcinoma. Cell, 2020. 182(1): p. 200-225 e35.
7. Xu, J.Y., et al., Integrative Proteomic Characterization of Human Lung Adenocarcinoma. Cell, 2020. 182(1): p. 245-261 e17.
8. Gao, Q., et al., Integrated Proteogenomic Characterization of HBV-Related Hepatocellular Carcinoma. Cell, 2019. 179(5): p. 1240.
9. Ge, S., et al., Author Correction: A proteomic landscape of diffuse-type gastric cancer. Nat Commun, 2018. 9(1): p. 1850.
最新动态
-
03.25
共筑“创新铁三角”:湖北中医药学会与生之源深化产学研创新
-
03.06
省经信厅副厅长郭波一行赴生之源调研 点赞企业“AI+生物”融合创新与全链条转化能力
-
01.16
新源地,共华章,开瑞景 ——武汉生之源生物科技股份有限公司暨子公司乔迁庆典圆满落幕
-
12.10
【直播】酵母双杂交技术:从原理逻辑到案例应用的系统精讲
-
10.24
【直播】荧光技术深度解析-双荧光素酶、BIFC、LCA的应用与选择
-
09.18
【直播】分子生物学核心技术详解
-
08.14
【直播】GST pull-down原理、应用与优化实战
-
07.24
【直播】解密基因调控:ChIP技术全攻略
-
06.19
【直播】免疫共沉淀(CoIP)实验流程和常见问题解决
-
05.15
【直播】EMSA技术全解析-助你攻克实验难点










