SWATH-MS定量蛋白质组学揭示了乳糖酸对耐甲氧西林金黄色葡萄球菌(MRSA)的多靶点抗菌机制
信息来源:金开瑞 作者:genecreate 发布时间:2020-06-01 16:47:13
热烈祝贺沈阳农业大学康教授及其团队研究成果荣登J. Agric. Food Chem.(IF=3.571, JCR 1 区)
题目:Label-Free Quantitative Proteomics Reveals the Multitargeted Antibacterial Mechanisms of Lactobionic Acid against Methicillin-Resistant Staphylococcus aureus (MRSA) using SWATH-MS Technology
期刊:Journal of Agricultural and Food Chemistry
影响因子:3.571
一、研究背景
耐甲氧西林金黄色葡萄球菌(MRSA)已成为一个严重的公共卫生问题,其能够定殖和感染人类和动物,导致相当高的发病率和死亡率。此外,MRSA对环境因素具有强烈的抗性,并且很容易污染乳制品、肉类和其他食品。一项新的研究表明,人类、动物和环境资源可能与 MRSA在整个生产链中对乳制品的污染有关,这对乳制品安全以及食品从业者和消费者的健康构成了严重威胁。因此,迫切需要防止和控制MRSA扩散的新型抗菌剂。
新的研究发现乳糖酸(LBA)表现出与乳链菌肽和百里酚对单核细胞增生李斯特菌的协同抗菌作用以及对耐甲氧西林金黄色葡萄球菌(MRSA)的抗菌活性。然而,目前还没有有关LBA对MRSA的抗菌活性和作用机理的相关报道。
在这项研究中,作者运用基于SWATH的定量蛋白质组学以及扫描电子显微镜(SEM)和透射电子显微镜(TEM)的超微结构观察,系统的研究了LBA在蛋白质组水平上对MRSA的抗菌机制。进一步通过基于PRM的靶向质谱技术和实时定量PCR(qRT-PCR)技术验证了几种差异表达蛋白的蛋白表达水平和mRNA表达水平。这项研究为LBA对抗耐多药性致病菌的分子机制提供了重要见解,证明了其在食品安全和制药中的潜在应用价值。
二、技术路线

三、实验结果
1. LBA处理的MRSA细胞超微结构的变化
用扫描电镜(SEM)和透射电镜(TEM)观察LBA处理前后MRSA细胞超微结构的变化。未经处理的细胞通过扫描电镜和透射电镜显示出正常、独立和均匀的细胞质(图1A,1D),1/2×MIC(9.375 mg/mL)作用2h,细胞出现不规则皱褶,胞质变薄,聚集,粘附(图1B和1E)。在1×MIC(18.75 mg / mL)条件下孵育2小时的MRSA细胞因极稀疏的细胞质、细胞内物质泄漏、细胞壁消失和细胞膜破裂而变形(图1C和1F)。此外,在处理过的细胞的TEM图像中观察到的致密颗粒或紧密凝结的物质(红色箭头)被认为是DNA凝缩和蛋白质沉淀异常的结果。因此,作者推测LBA不仅可能破坏细菌的细胞壁和细胞膜,也会影响细胞内的蛋白质和DNA。
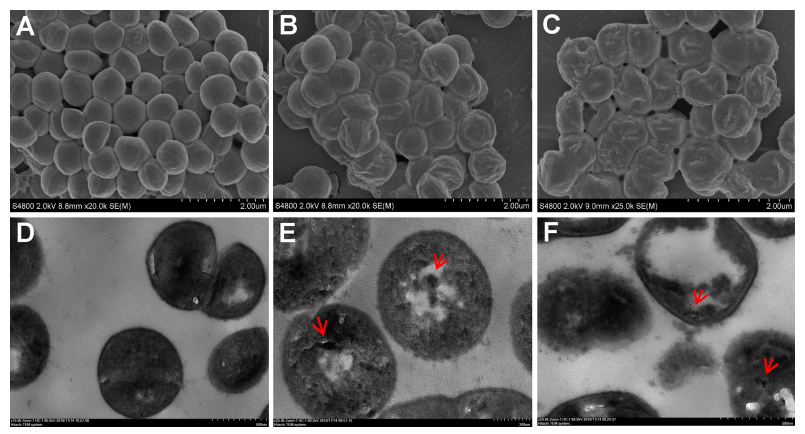
图1 LBA处理的MRSA细胞超微结构的变化
2.SWATH定量蛋白质组学
作者利用SWATS-MS技术研究了LBA处理后MRSA细胞的蛋白质组学改变。共定量到1147种蛋白质,其中100为显著差异蛋白 (|FC|≥1.2, P<0.05)(图 2A)。图2B显示了差异表达蛋白(DEP)的层次聚类热图。作者使用Uniprot数据库分析了DEP的功能,并将其分为几类,包括蛋白质生物合成(10%),细胞表面蛋白质和毒力因子(8%)等(图2D)。另外,亚细胞定位预测结果表明,在100个DEPs中,有81个位于细胞质中,有13个位于细胞外基质中,有6个定位在细胞膜上(图2C)。
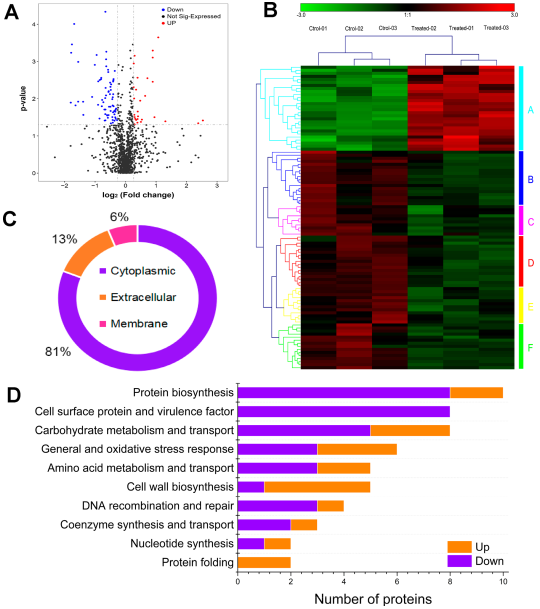
图2 SWATH-MS揭示了对照组和LBA处理组之间差异表达的蛋白质(DEPS)
3.差异表达蛋白分析
3.1氧化应激和DNA修复相关的DEPs
图3显示,LBA通过积累细胞内ROS并抑制内源性抗氧化剂MsrB和类胡萝卜素的活性来引发MRSA的氧化应激反应。过量的ROS也可能引起DNA氧化损伤,从而引起DNA双链断裂,从而影响任何细胞大分子。
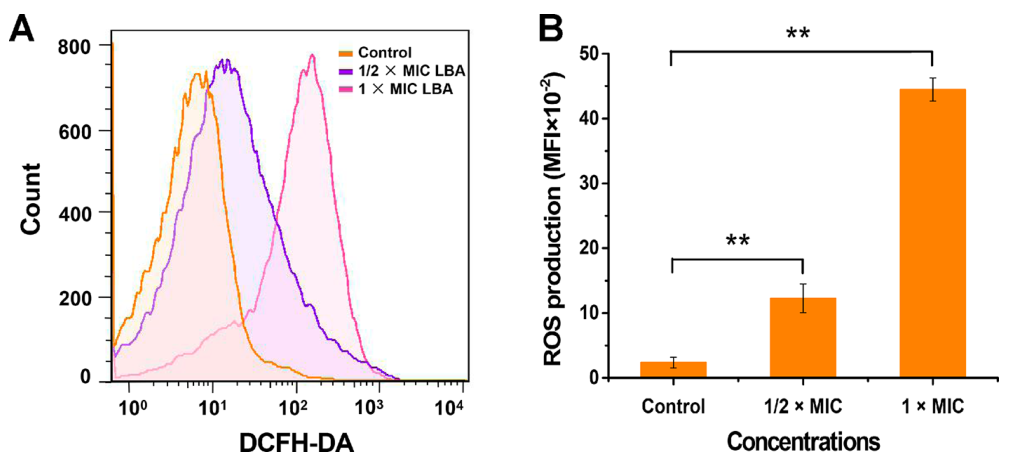
图3 LBA处理后ROS积累
3.2 细胞表面蛋白和毒力因子
LBA处理2 h后,细胞表面蛋白和毒力因子均下调。并且qRT-PCR分析表明这些基因的表达降低了,与蛋白质组学分析结果一致(图4)。
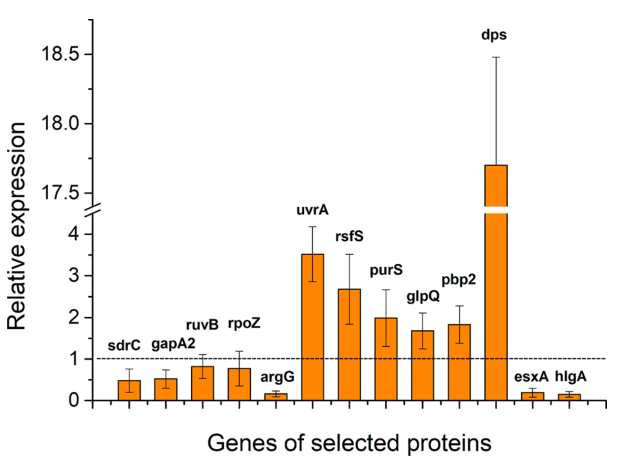
图4 LBA处理后MRSA转录表达水平
3.3 DEPs的蛋白质-蛋白质相互作用网络
PheT与DnaK,GroEL,ArgH,ArgG和PurL的连接表明,翻译过程中涉及的蛋白质可能触发蛋白质折叠和降解系统,从而影响核苷酸合成途径。此外,AhpC与DnaK,GroEL,OdhB,GpmA和GapA2的连接表明,参与氧化应激反应的蛋白质也可能触发蛋白质折叠和降解系统并抑制碳水化合物的代谢途径。
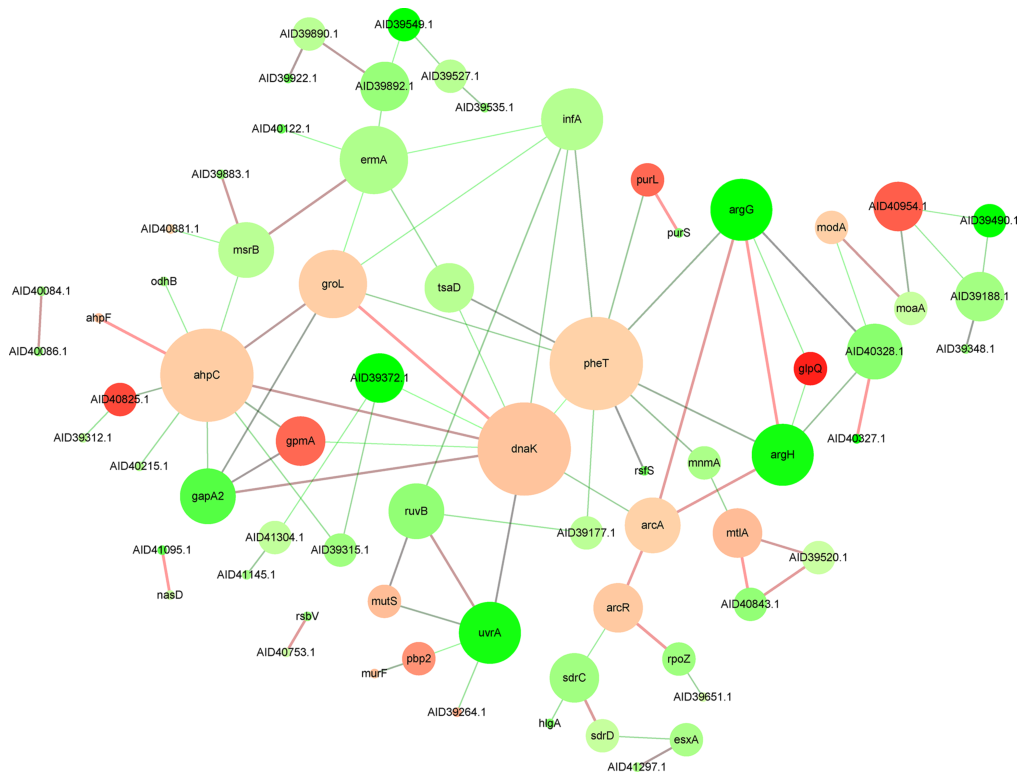
图5 DEP的蛋白质-蛋白质相互作用网络
3.4其他生物学功能
对其他差异蛋白的分析,我们发现LBA处理MRSA发挥抗菌作用还会影响碳水化合物和氨基酸转运与代谢,核苷酸、辅酶合成和运输,细胞壁生物合成,蛋白质生物合成以及MRSA的防御体系等相关功能方面。
四、实验验证
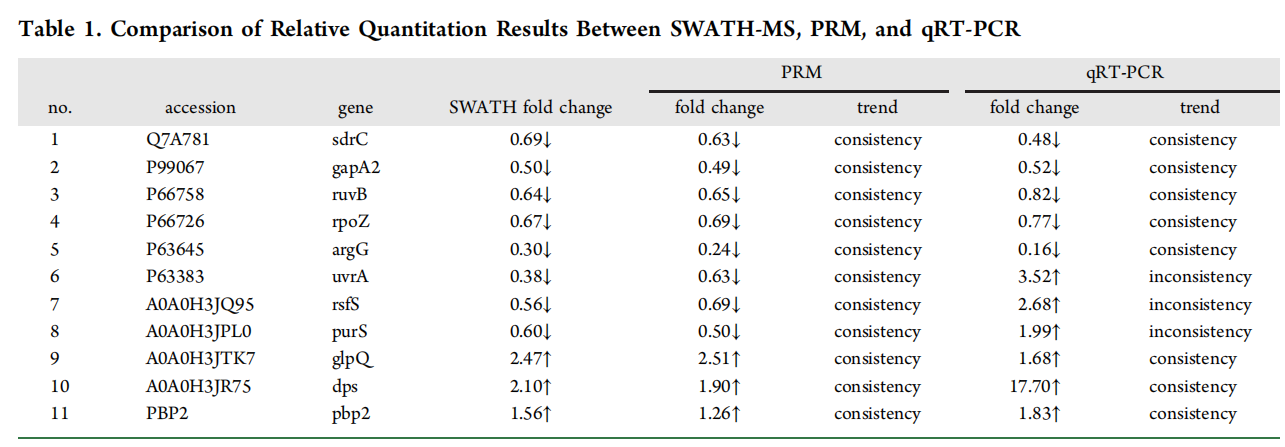
作者使用PRM和qRT -PCR对差异蛋白进行验证。其中PRM验证的所有靶蛋白与SWATH定量结果趋势一致(表1)。qRT-PCR验证的靶蛋白中8个基因的mRNA表达水平与相应的蛋白表达水平呈一致趋势(图4和表1),而其余3个基因则与相应的蛋白质表达水平不一致,这可能是由于这些基因的转录后调控所致。基于SWATH-MS、PRM和qRT-PCR定量方法的结果总体一致性,表明SWATH定量结果的可靠性。
表1 SWATH-MS、PRM和qRT-PCR相对定量结果比较
五、小结
通过超微结构观察发现LBA处理后的MRSA在表型上发生了细胞膜褶皱的现象,基于这种表型进一步支持了LBA能作为MRSA的一种抗菌剂。为了阐述这种作用机制,作者基于SWATH-MS的蛋白质组学分析了正常MRSA细胞和LBA处理后的MRSA在蛋白表达水平上的差异,找到了一些差异表达的蛋白,进一步对差异蛋白进行分析,从而阐述了LBA抗MRSA的作用机理。为了验证组学定量结果的准确性,作者进一步运用基于质谱的PRM技术和qRT-PCR技术,从蛋白和基因层面对差异蛋白进行了验证,验证了实验结果的准确性和一致性。
总的来说,本文在蛋白质组水平上系统地阐述了LBA对MRSA的作用模式。考虑到LBA对MRSA的多靶点作用,作者也提出LBA在食品和制药防腐剂方面可能具有潜在的应用价值。
最新动态
-
03.11
同为抗体,为什么一抗看“抗原种类”,二抗却看“一抗种属”?
-
03.11
J Nanobiotechnology(IF=12.6):蔓越莓“纳米邮差”递送麦角甾醇,重启早衰卵巢功能!
-
02.27
没有抗体?不是模式植物?DAP-seq照样搞定你的TF靶基因!
-
02.27
高分研究的共同选择:三篇权威文献背后的ChIP实验工具解析
-
02.27
表观遗传学进入“多维验证”时代,这些疾病机制再也藏不住了!
-
02.27
“药食同源”顶刊思路(IF=10.5)!来源鉴定+活性追踪+体内验证,全面解析无花果来源外泌体抑制乳腺癌骨转移的双重机制!
-
02.27
千年古方,纳米新生:科学家破解半夏如何“指挥”免疫细胞对抗肺癌!
-
01.29
技术跨界联用:表观遗传学进入“多维验证”时代,这些疾病机制再也藏不住了!文末有惊喜活动!
-
01.29
机制研究的金标准:金开瑞RIP/RNA pull-down试剂盒获多篇顶刊研究认可!
-
01.29
想测结合常数,但样本太珍贵?来试试MST技术










