J NANOBIOTECHNOL (IF:12.6) | 白术衍生的细胞外囊泡样颗粒通过重塑肠道微生态平衡促进溃疡性结肠炎的恢复
白术(Atractylodes macrocephala)是菊科苍术属多年生草本植物,在中国传统医学中占有重要地位。在《神农本草经》中白术被描述为具有健脾胃、消除水肿、增强免疫力等多种功效的药用植物。白术的根茎,经晒干和研磨后,是制作中药的主要成分。但是传统水煎剂受限于成分复杂、生物利用度低及靶向性差,制约临床转化,近些年兴起的植物外囊泡样颗粒(PELNs)为破局提供可能:它作为天然纳米载体(50-200 nm),可以高效荷载母源活性物质(核酸、脂质、代谢物), 靶向递送至炎症部位;具备低免疫原性与高生物相容性。
今年6月发表在《Journal of Nanobiotechnology》期刊上一篇题为“Atractylodes macrocephala-derived extracellular vesicles-like particles enhance the recovery of ulcerative colitis by remodeling intestinal microecological balance”的综合性研究文章,该研究就主要聚焦于白术细胞外囊泡样颗粒(AMEVLP)。
作者从传统中药白术(Atractylodes macrocephala, AM)中分离出细胞外囊泡样颗粒,证实其通过重塑肠道菌群平衡、调节色氨酸代谢和抑制Th17细胞分化通路,显著缓解溃疡性结肠炎(UC)。AMEVLP可增加肠道有益菌(如拟杆菌门)、减少有害菌(如变形菌门),提升菌群α多样性,促进吲哚衍生物生成,修复肠屏障并抑制炎症。临床前研究(细胞/小鼠模型)及初步临床试验(2例UC患者)均验证其疗效,为UC治疗提供新策略。

一、创新点
首提"草本囊泡"治疗UC新范式:创新性从白术中提取AMEVLP,兼具中药多组分协同优势与纳米载体靶向性,克服传统中药提取物生物利用度低的问题。
揭示"菌群-代谢-免疫"调控轴:阐明AMEVLP通过调节菌群结构→改变色氨酸代谢→增加吲哚衍生物→抑制Th17通路→减轻炎症的完整机制。
确证微生物依赖性疗效:抗生素清除菌群后AMEVLP失效,证明其疗效依赖于肠道微生物重塑。
多组学整合验证机制:结合16S rDNA测序、代谢组学、转录组学,发现AMEVLP特异性富集单萜、甾体等活性成分,并调控色氨酸代谢通路。
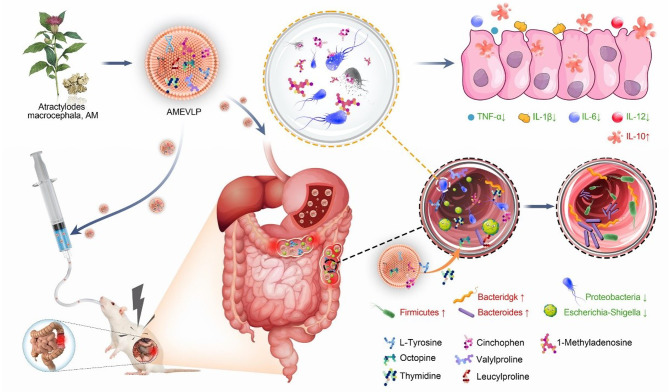
AMEVLP 在缓解 UC 中的作用和作用机制的图表
二、研究思路
1、AMEVLP的分离和表征
通过榨汁、差速超速离心和过滤成功分离出 AMEVLP,其平均粒径为 90.61 ± 19.66 nm,蛋白质浓度达 8330 μg/mL。透射电镜显示其呈杯状形态,TritonX-100破膜实验表明,分离的AMEVLP的纯度达到近80%。AMEVLP 富含核酸、脂质及白术特异性代谢物(如苍术内酯、单萜和甾体衍生物),且在模拟胃肠液中保持稳定性(粒径变化 <20%),为口服递送奠定基础。
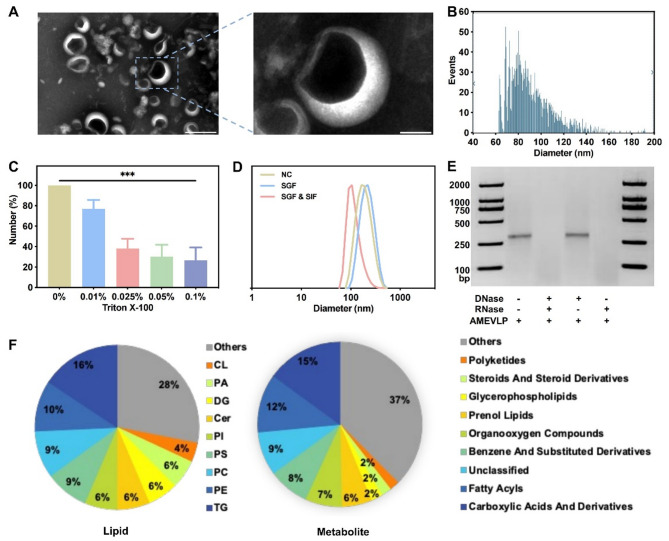
图1. AMEVLP 的鉴定
2、AMEVLP的体外抗氧化和抗炎作用
"AMEVLP 可被 RAW264.7 巨噬细胞高效内化(8 小时摄取率 >99%)。在 LPS 诱导的的RAW264.7细胞炎症模型中,AMEVLP 显著上调抗炎因子 IL-10 的基因表达,并抑制促炎因子 IL-1β、IL-6、IL-12 和 TNF-α 的表达(呈浓度依赖性)。同时,AMEVLP 降低 H₂O₂ 诱导的活性氧(ROS)水平,证实其抗氧化能力。
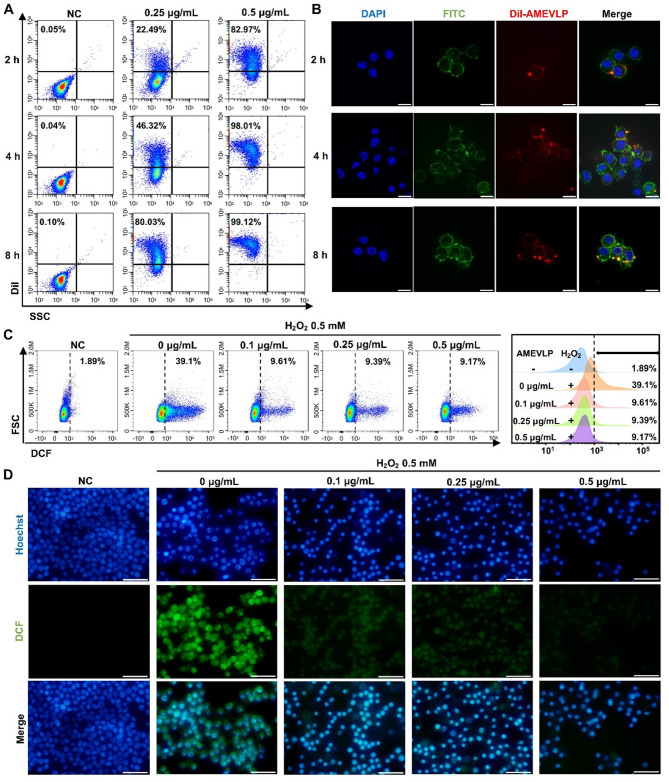
图2. AMEVLP的体外抗炎和抗氧化作用
3、体内治疗溃疡性结肠炎的功效
在 DSS 诱导的 UC 小鼠模型中,AMEVLP(2 mg/kg/d)显著改善疾病活动指数(DAI)、恢复结肠长度、减少黏膜溃疡和炎性浸润。通过免疫荧光染色证实,AMEVLP 上调紧密连接蛋白(Occludin, ZO-1, Claudin)表达,并通过阿尔新蓝染色修复杯状细胞结构,表明其重建肠道屏障功能的能力。
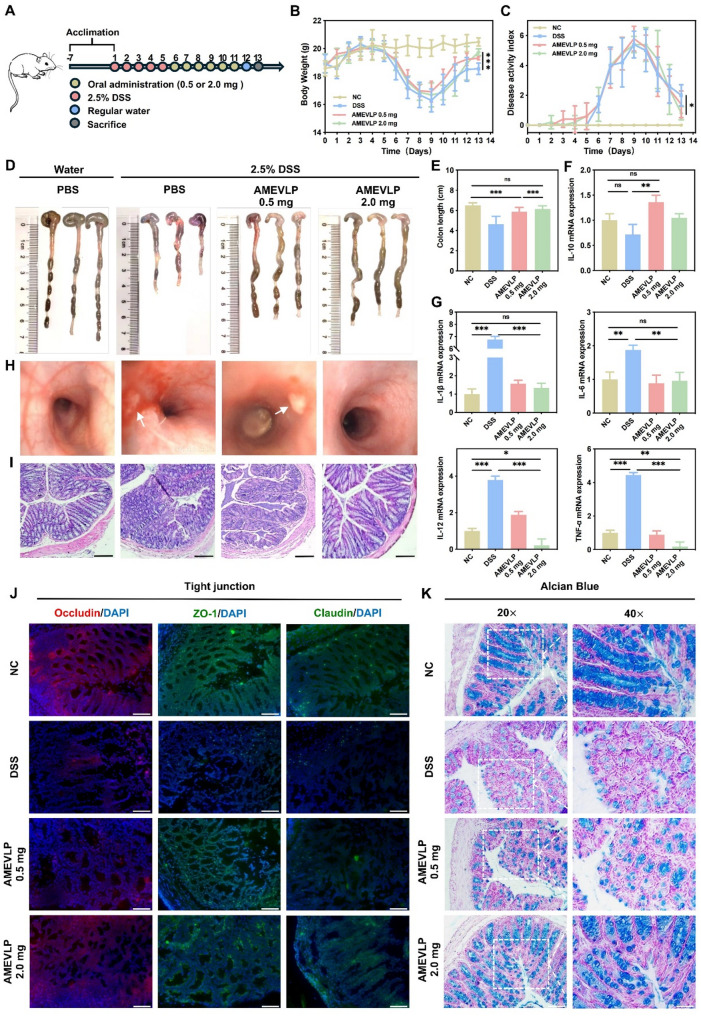
图3. AMEVLP 可缓解小鼠的 DSS-UC 并修复结肠屏障功能
4、AMEVLP调节UC小鼠的肠道菌群和代谢物组成
为了阐明AMEVLP如何调节UC小鼠肠道菌群的组成,对小鼠粪便中的肠道菌群进行了分析,结果表明,样品的群落组成在组间相似。随后通过比较门水平和属水平的肠道菌群,发现,AMEVLP 增加肠道菌群 α 多样性(Shannon 指数提升),促进有益菌门(拟杆菌门 Bacteroidota、厚壁菌门 Firmicutes)增殖,抑制有害菌门(变形菌门 Proteobacteria),这表明表明,AMEVLP可以在门水平和属水平上降低有害细菌的丰度,增加有益细菌的丰度。非靶向代谢组学分析表明,AMEVLP可以通过调节肠道菌群的变化来改变色氨酸代谢,进而增加肠道中的吲哚衍生物,从而在AMEVLP给药后对肠道屏障产生保护和抗炎作用,协同缓解 UC。
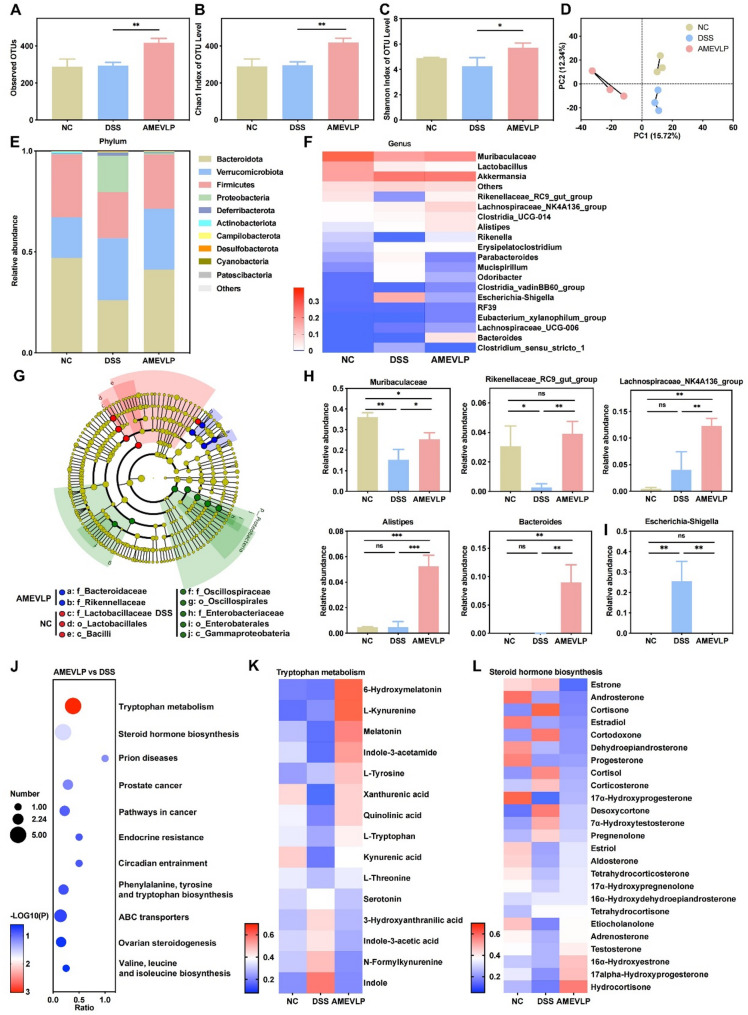
图4. AMEVLP 对肠道微生物和代谢物组成的调节
5、微生物依赖性及免疫通路验证
通过给小鼠口服抗生素,发现抗生素清除肠道菌群后,AMEVLP 对 DSS 结肠炎的治疗作用完全消失,证明其疗效依赖于肠道微生物重塑。多组学联合分析(代谢组-转录组-菌群)揭示,AMEVLP 通过调节 '菌群-代谢-免疫轴' 发挥作用:其特异性代谢物(如 L-酪氨酸)与益生菌(如 Bacteroides)显著正相关,并富集于 Th17 细胞分化信号通路。免疫组化证实,AMEVLP 下调结肠组织促炎因子(IL-1β, IL-21, TNF-α),上调抗炎因子 IL-10 的表达。这些结果表明,AMEVLP通过Th17细胞分化信号通路治疗小鼠UC。
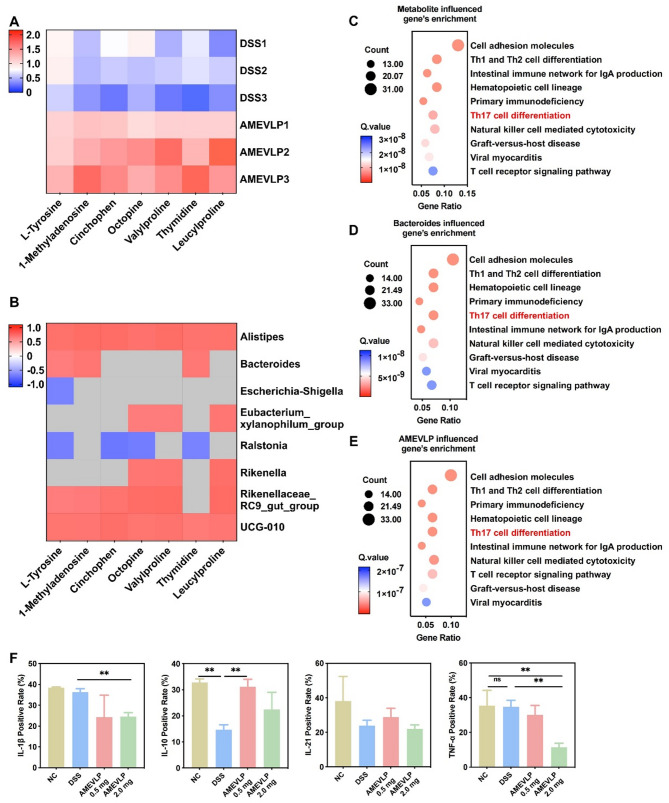
图5. AMEVLP 通过调节 Th17 细胞分化信号通路来缓解小鼠的 UC
6、临床疗效与转化价值
初步临床试验中,2 例 UC 患者口服 AMEVLP 后,结肠镜显示直肠黏膜糜烂和溃疡显著改善,组织病理学提示隐窝脓肿和淋巴细胞浸润减轻。该研究首次证明 AMEVLP 作为一种新型天然纳米药物,兼具调节肠道微生态平衡与抗炎双重功效,为 UC 治疗提供创新策略。
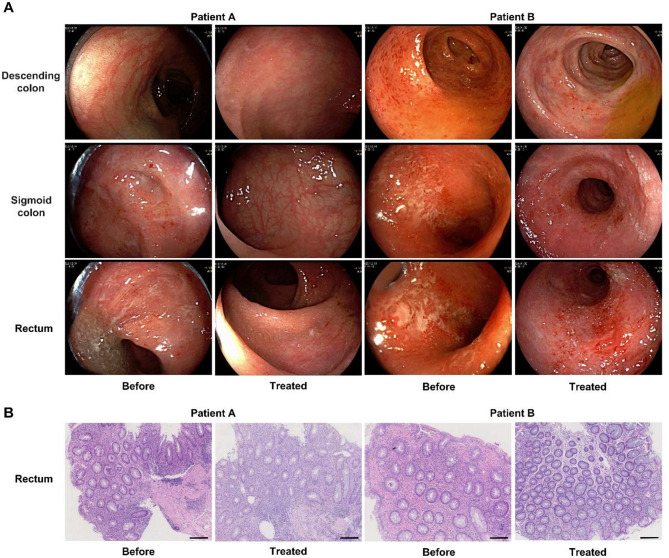
图6. AMEVLP的临床疗效
AMEVLP作为AM活性成分的浓缩精华,不仅继承了其源中药的特性,而且在离体和体内实验中表现出显著的抗炎、抗氧化和肠道屏障修复能力。通过调节肠道菌群、代谢物和免疫反应,AMEVLP 为 UC 治疗提供了新的途径和机制理解。更重要的是,AMEVLP的作用机制是通过微生物依赖发挥治疗作用。本研究有助于开发一种具有调节肠道微生态和抗炎双重功效的新型天然UC治疗药物,具有巨大的临床转化潜力,为草药囊泡的临床应用奠定基础。
三、局限与展望
临床转化挑战:初步临床试验样本量小(n=2),需扩大样本、延长随访,并探索最佳给药方案(剂量/频次)。
机制深化方向:AMEVLP中关键活性分子(如特异性miRNA或脂质)未明确,需通过蛋白质组学/功能缺失实验进一步解析。
Th17通路下游效应分子(如RORγt)的调控细节需深入探索。
生产工艺优化:提取工艺的批次间一致性、规模化生产及标准化质控体系亟待建立。
拓展应用场景:探索AMEVLP在其他炎症性疾病(如克罗恩病、关节炎)中的疗效,或与现有药物(如美沙拉嗪)联用的协同效应。
文献:Tan X, Gao B, Xu Y, Zhao Q, Jiang J, Sun D, Zhang Y, Zhou S, Fan JB, Zhang M, Zhao K. Atractylodes macrocephala-derived extracellular vesicles-like particles enhance the recovery of ulcerative colitis by remodeling intestinal microecological balance. J Nanobiotechnology. 2025 Jun 10;23(1):433.
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










