【客户文献分享】Advanced Science(IF=15.6)| Irisin调控ENO1泛素化改善肺动脉高压肺血管重构
肺动脉高压(PAH)是一种以肺动脉压力升高和肺血管重构为特征的临床综合征,目前临床治疗手段有限,患者预后较差。研究发现,肺动脉平滑肌细胞(PASMCs)增殖和肺血管重构是PAH进展的核心环节。Irisin是一种运动诱导的肌动蛋白,近年来因其在抗炎、抗氧化应激和代谢调控中的保护性作用备受关注。然而,Irisin是否参与了PAH的发生发展和作用机制尚未明确。
2025年6月25日,哈尔滨医科大学附属第二医院心内科研究团队在Advanced Science杂志发表题为“Irisin Attenuates Pulmonary Vascular Remodeling in Pulmonary Arterial Hypertension via Ubiquitin-Mediated Regulation of ENO1”的研究论文,首次揭示了运动诱导因子irisin在PAH中的保护作用及其分子机制,为PAH的治疗提供了新的靶点。

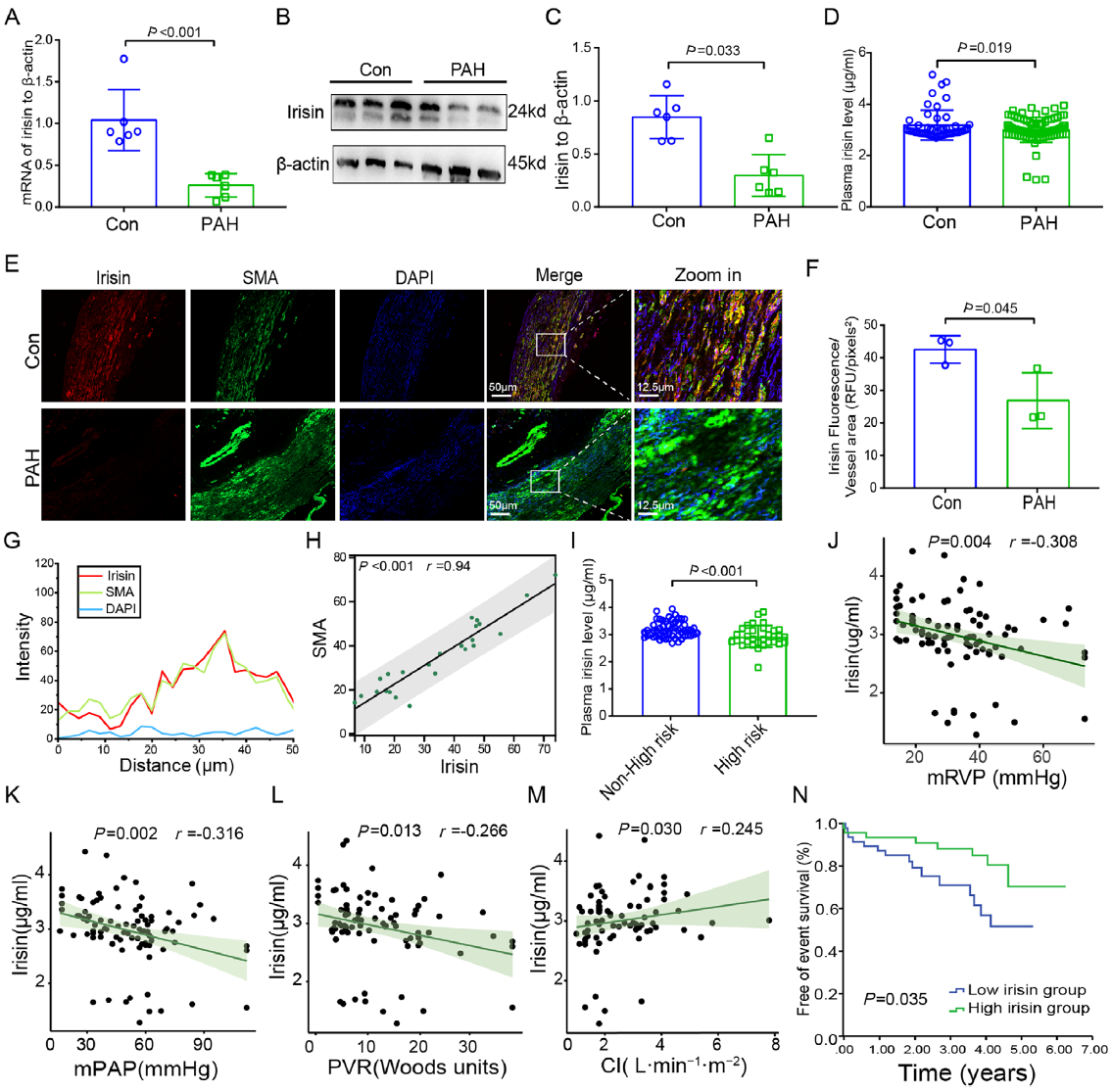
首先,研究团队通过对93例PAH患者和50例健康对照的对比研究发现,PAH患者血浆和肺动脉组织中的irisin表达呈现显著下调趋势,且免疫荧光结果显示irisin与肺动脉平滑肌标志物SMA存在共定位现象。进一步分析显示,血浆irisin水平与平均肺动脉压和肺血管阻力呈负相关,而与心指数呈正相关。值得注意的是,低irisin水平的PAH患者预后较差,其临床恶化事件发生率显著升高。多因素分析证实irisin可作为PAH危险分层和预后的独立预测因子。这些重要发现共同提示,Irisin不仅是PAH的生物标志物,更是疾病进展的关键调控因子。
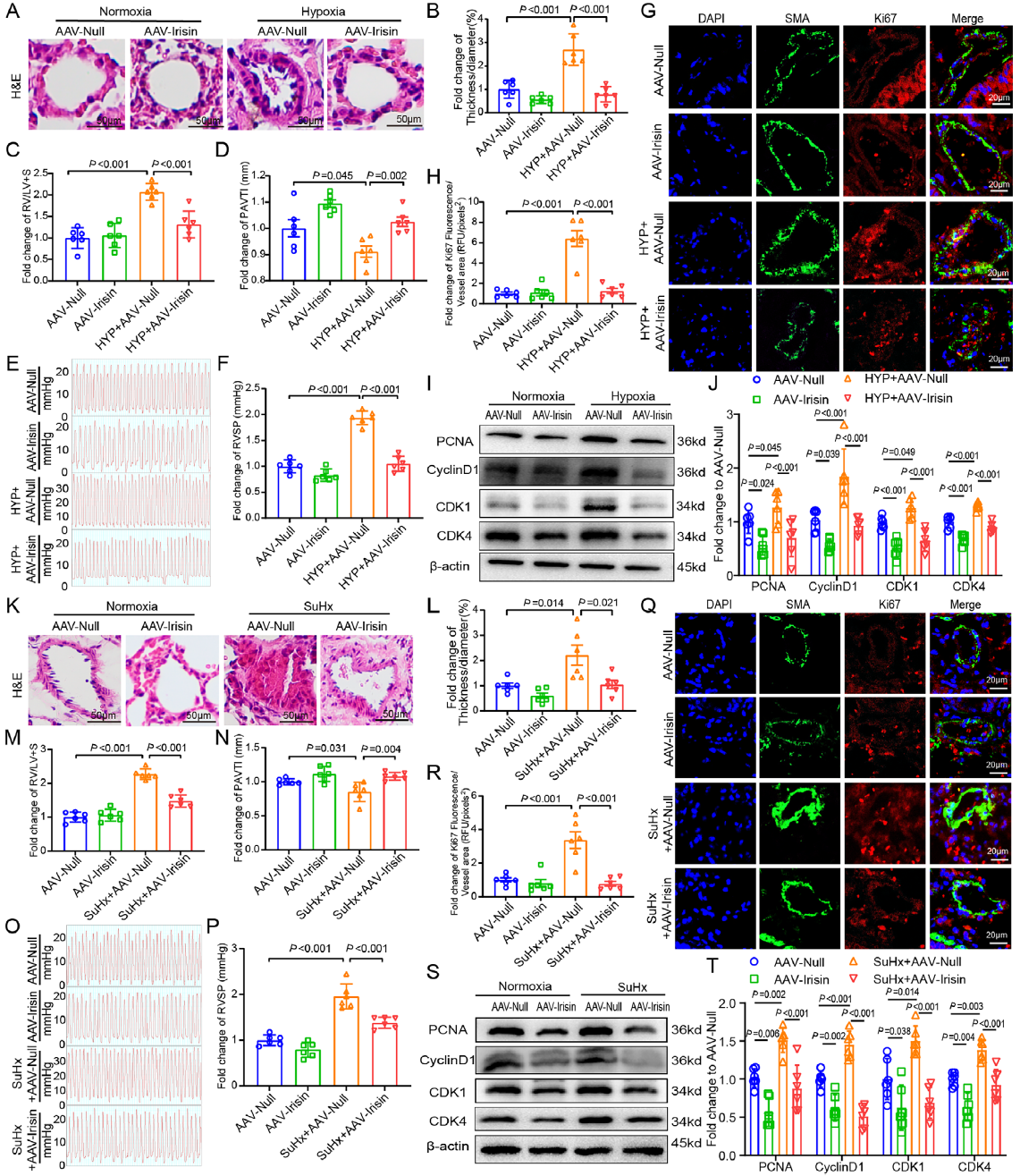
为了探究irisin在PAH中的治疗作用,在低氧和SuHx诱导的PAH小鼠模型中,通过AAV5载体过表达irisin或每周注射250μg/kg外源性irisin,发现irisin过表达显著改善了PAH病理特征:肺动脉壁厚度明显减轻,右心室与左心室加室间隔的质量比(RV/LV+S)降低,肺动脉流速时间积分(PAVTI)增加,右心室收缩压(RVSP)下降。机制研究表明,irisin通过下调增殖标志物PCNA、Ki67以及细胞周期调控蛋白CyclinD1、CDK1和CDK4的表达,有效抑制肺动脉平滑肌细胞的异常增殖。这些重要发现为探究靶向干预PAH肺血管重构的新型治疗策略提供了坚实的理论基础。
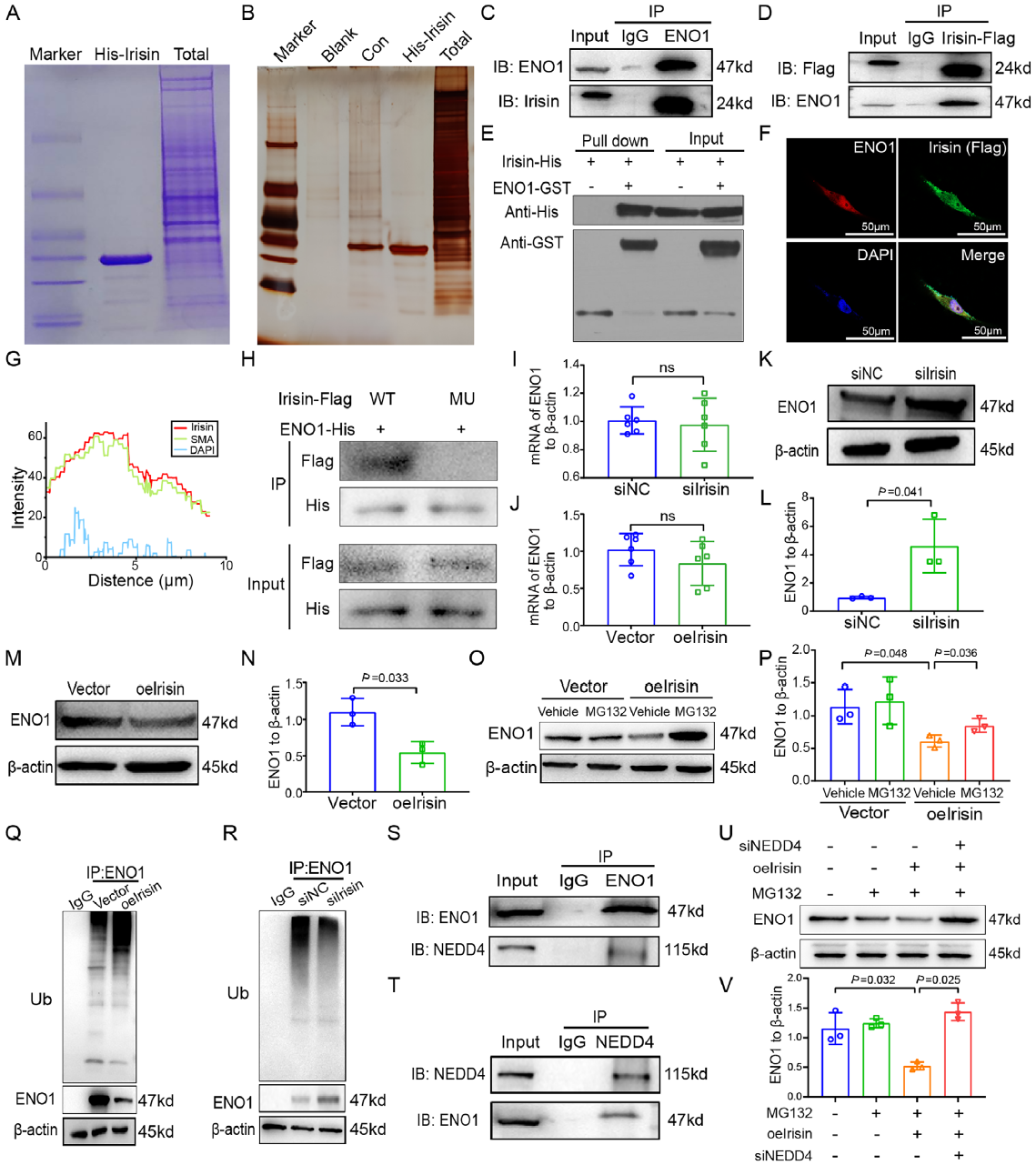
研究团队通过质谱分析和分子对接技术,首次在分子水平证实了Irisin与糖酵解关键酶ENO1的特异性结合,深入研究发现,Irisin作为分子支架,能够精准招募E3泛素连接酶NEDD4,形成"Irisin-ENO1-NEDD4"三元复合物,促使ENO1发生泛素化降解。这一过程依赖蛋白酶体途径,MG132实验证实,抑制蛋白酶体可阻断ENO1的降解。机制研究表明,Irisin通过下调ENO1蛋白水平,显著抑制PASMCs的增殖和细胞周期进程,为PAH的靶向治疗提供了新思路。
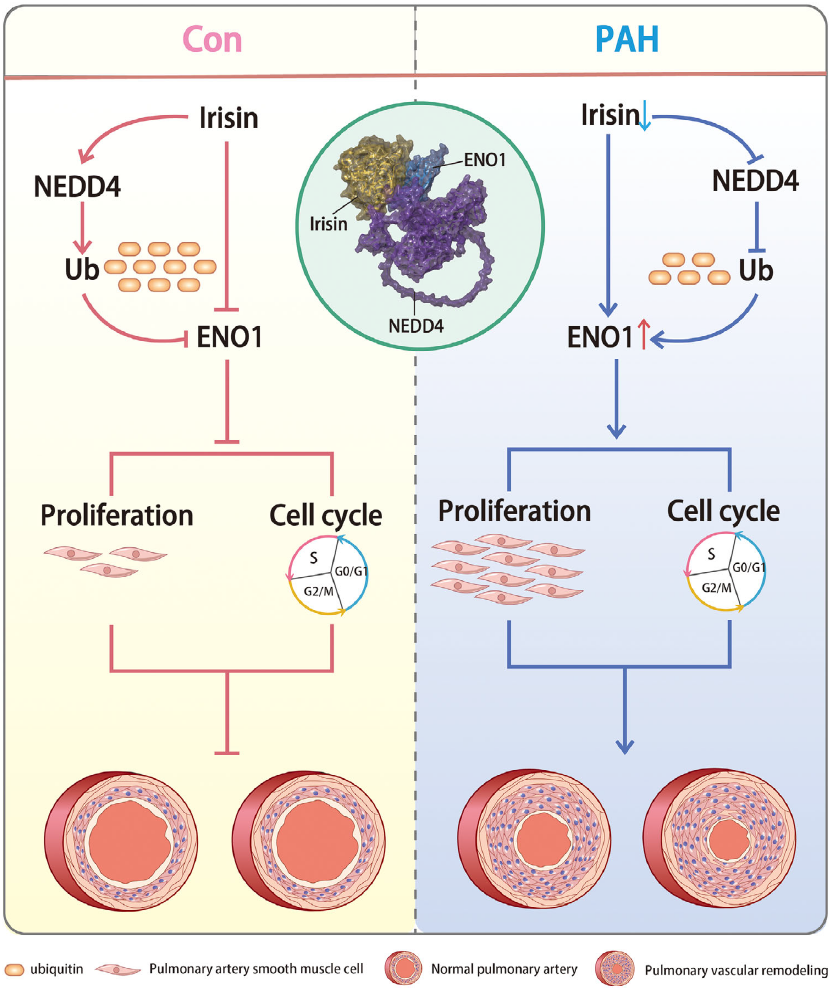
综上所述,在正常生理状态下,irisin能够募集E3泛素连接酶NEDD4,促进其相互作用蛋白ENO1的泛素化降解,而在PAH病理条件下,irisin表达水平下降导致NEDD4募集减少,造成ENO1蛋白累积,进而促进PASMCs的异常增殖,加速细胞周期进程。
这项研究揭示了Irisin-ENO1调控轴可作为PAH的新型治疗靶点;其次,研究证实外源性补充Irisin能有效逆转PAH的病理进程,这为开发重组Irisin蛋白或其模拟肽类药物奠定了实验基础;另外,Irisin表达水平与疾病严重程度显著相关,可作为PAH诊断和预后评估的新型生物标志物。Irisin具有较好的临床转化价值,有望成为潜在PAH治疗新靶点。
金开瑞合作实验:构建过表达载体,融合蛋白,pull down实验


备注:构建了irism 过表达载体、His-Irisin和FLAG-ENO1融合蛋白 ,并通过pull down 实验证明了irism和ENO1的相互作用
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










