分子互作只做Co-IP?试试分子对接+SPR+降解验证
为什么别人的分子对接能发高分文献,你的却总被审稿人质疑?
从“静态照片”到“动态电影”,从“随机发现”到“理性设计”,只差这一步。
做过蛋白-小分子或蛋白-蛋白互作研究的你,一定遇到过这些场景:
●分子对接打分特别漂亮,3D图也画得花团锦簇,结果SPR一做,亲和力弱到怀疑人生;
●细胞实验效果明显,但Co-IP就是拉不下来,想不通到底哪里出了问题;
●想验证某个关键结合位点,凭感觉做了一堆点突变,花费几个月,结果大部分都是阴性。
问题出在哪?不是方法不对,而是工具用错了阶段。
1、痛点:为什么你的互作实验经常“翻车”?
场景一:对接漂亮,SPR打脸
你用分子对接找到了一个化合物与靶蛋白“看起来很美”的结合姿势——关键的氢键、合适的疏水口袋、打分也比较理想。
于是你信心满满地去做SPR/BLI,结果:解离飞快,结合能远不如预期。
为什么?
分子对接提供的是“静态照片”,只能说明“这一刻可能碰到了一起”。而真实世界是“动态电影”——蛋白在持续晃动,结合口袋开合变化,水分子和离子也在参与。因此,单纯依赖对接结果,极易落入“假阳性”或“假阴性”的陷阱。
场景二:细胞有效,对接对不上
细胞实验显示化合物有效,分子对接却预测出奇怪的结合模式,甚至与已知关键残基不符。
原因分析:
细胞环境中靶蛋白可能呈现多种构象状态,可能存在磷酸化、泛素化等翻译后修饰,也可能结合辅因子或其他蛋白,而分子对接基于静态晶体结构,难以反映上述动态变化。此外,化合物的表型效应可能源于间接机制(如调控信号通路或蛋白稳定性),无需直接结合靶点即可发挥作用。
解决思路:当对接预测与细胞实验结果不一致时,可采用DARTS、CETSA等靶点解卷积技术直接鉴定化合物的真实结合靶点。
场景三:点突变靠感觉,大海捞针
想验证关键结合位点,凭感觉设计点突变,耗时数月,结果多为阴性。
原因分析:
典型靶蛋白包含数百个氨基酸残基,随机选择突变位点的成功率通常低于20%。盲目突变不仅效率低下,还可能误伤结构关键残基导致蛋白折叠异常。
解决思路:开展点突变实验前,应先通过分子对接预测关键结合残基(如形成氢键、疏水作用、π-π堆积的残基)。进一步可结合分子动力学模拟与MM/GBSA能量分解,定量评估各残基对结合自由能的贡献,实现精准设计。
2、闭环思路:分子对接+分子动力学+实验验证
一个好的分子互作研究,应该是这样的三段式:
| 阶段 | 技术方法 | 解决的问题 | 一句话概括 |
| 初筛 | 分子对接 | 寻找可能的结合模式 | “能不能碰上” |
| 精筛(进阶) | 分子动力学模拟 | 考察结合是否稳定 | “结合的紧不紧” |
| 验证 | SPR/点突变/Co-IP | 实验证实计算结果 | “用事实说话” |
3、核心文献拆解:一篇完整的“干湿结合”闭环研究
下面,我们就以2026年3月24日北大詹启敏院士、张维敏教授团队在线发表于《Advanced Science》(IF=15.1,中科院一区)的论文 《Halofuginone is a Molecular Glue Degrader of Integrin β4》为范例,拆解分子对接和湿实验验证是如何串联成一条完整的闭环证据链的。
研究问题:常山酮(Halofuginone, HF)能否作为分子胶降解剂靶向降解整合素β4(ITGB4),从而抑制食管鳞癌进展?
第一步:靶点发现:高通量筛选 + DARTS质谱 → 锁定整合素β4
研究者首先对173个天然产物进行MTS高通量筛选,在9种食管鳞癌细胞系中测试其杀伤效果。初筛获得44个抑制率超过50%的候选分子,进一步剂量依赖性验证后,常山酮(HF)脱颖而出,其IC50值在0.25-24.77 μM之间,展现出最强的细胞毒性。
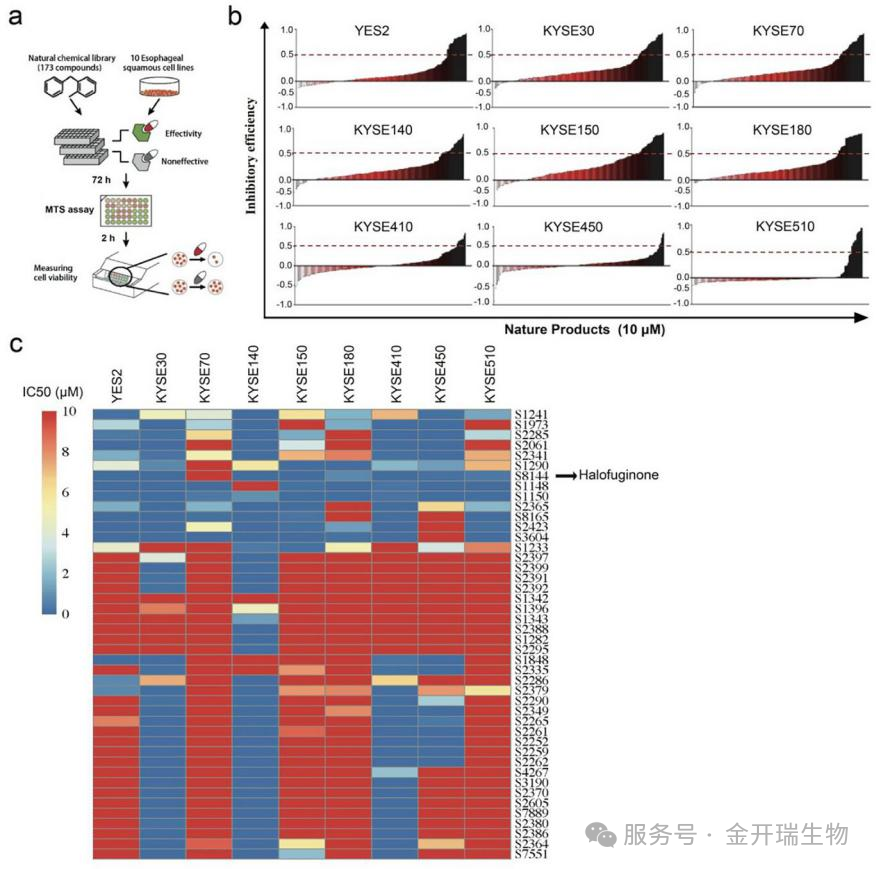
图1.候选天然产物的高通量筛选
接下来要回答的问题是:HF的靶点是谁?
研究者采用DARTS技术——该技术利用药物结合后保护靶蛋白免受蛋白酶K降解的原理——将不同浓度的HF与细胞裂解液共孵育,随后加入蛋白酶K进行消化。银染显示存在差异蛋白条带,质谱鉴定后结合人类蛋白图谱数据库筛选,最终从16个膜蛋白中锁定了整合素β4。DARTS-Western Blot进一步确认,HF剂量依赖性地保护整合素β4免受蛋白酶K降解。
为明确整合素β4的临床相关性,研究者对包含107例食管鳞癌组织和72例癌旁组织的芯片进行IHC染色,发现整合素β4在癌组织中显著高表达,且高表达组患者的总体生存期显著更差,Cox回归分析提示其可作为独立预后因素。
核心发现:HF结合整合素β4并降低其蛋白水平,整合素β4高表达与食管鳞癌不良预后显著相关。
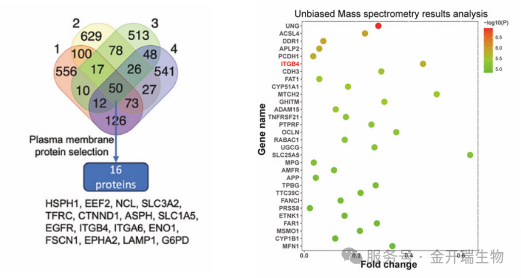
图2. DARTS-MS结果图
第二步:结合验证:分子对接(预测关键残基)+ SPR(实测亲和力)
关键问题:HF如何结合?
研究者采用分子对接(AutoDock) 预测HF与整合素β4的结合模式:
发现HF与整合素β4的Ser1325和Ile1326形成两个氢键,距离分别为2.1 Å和3.2 Å(<5 Å满足稳定物理相互作用标准)结合口袋位于整合素β4的C2结构域(第一个FNIII结构域对)
这一步的作用:给出“HF与整合素β4如何结合”的可视化证据,预测了关键结合残基,为后续点突变验证指明了方向。
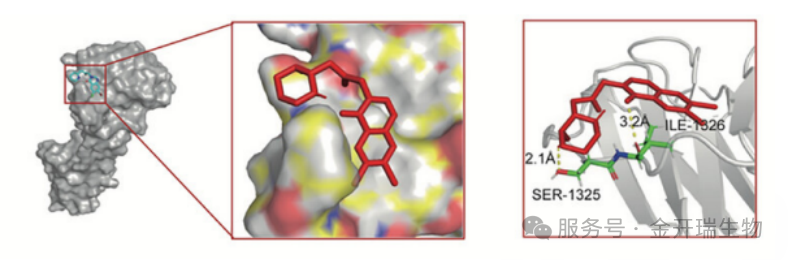
图3. 分子对接结果图
接下来,研究者进一步验证HF与整合素β4是否直接结合。
用表面等离子体共振(SPR)实验直接验证HF与整合素β4的结合,结果显示解离常数(KD)= 5.855 ± 0.75 μM,证实HF与整合素β4存在中等强度的直接相互作用。
分子对接预测了结合模式和关键残基→ SPR实验验证了确实有结合 → 两者相互印证!
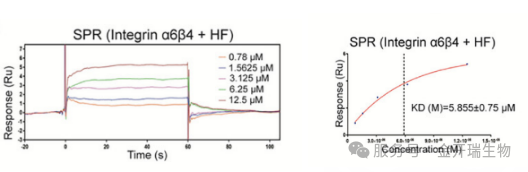
图4. SPR结果图
第三步:分子胶机制探索——降解实验 + 泛素化
HF不仅是结合,更关键的是:它作为一个分子胶降解剂,促进整合素β4通过CRL4B^WDR18 E3泛素连接酶复合物被降解。
| 实验方法 | 发现 | 机制发现 |
| CHX实验 | HF加速整合素β4降解(半衰期缩短) | 提示是翻译后修饰调控 |
| 蛋白酶体抑制剂Mg132 | 阻断HF诱导的降解 | 确认是泛素-蛋白酶体途径 |
| 泛素化IP | HF剂量依赖性地增强整合素β4泛素化 | 进一步确认降解途径 |
| siRNA筛选 | CUL4B、DDB1、WDR18是必需蛋白 | 锁定CRL4B^WDR18复合物 |
| Co-IP | HF增强WDR18与整合素β4的结合 | “胶水”功能验证 |
第四步:关键结合位点定位——从结构域到氨基酸的逐级锁定
干实验预测:分子对接显示HF结合在整合素β4的C2结构域(包含Ser1325/Ile1326)
湿实验验证:
❖构建C1、C2、C3截短体 → HF选择性降解C2结构域
❖Co-IP显示HF特异性地增强C2与WDR18的相互作用(C3无效应)
❖Ser1325A/Ile1326A双突变→完全废除HF的结合和降解功能
对接预测“HF结合C2结构域的Ser1325和Ile1326” → 截短体验证“C2结构域是功能所必需”→点突变验证“这两个位点突变后功能完全丧失” → 干湿结论完全一致!
4、总结
如果你的文章目前还停留在:
只做了分子对接→ 容易被审稿人质疑“为什么不验证?”
只做了Co-IP/SPR → 解释力有限,缺乏分子层面的细节
不妨学学我们解析的这篇Advanced Science的研究思路
“干湿结合”的最高境界,不是简单堆砌数据,而是:
1.先用计算预测(对接找出可能的结合位点和关键残基)
2.再用实验验证(SPR测亲和力、点突变验证关键残基、截短体定位功能域)
3.最后形成闭环(预测与验证一致,且预测指导了实验设计)
但如果想进一步回答“这个结合在动态环境下是否稳定”“结合自由能到底是多少”这类问题,可以在对接之后加入分子动力学模拟——
通过RMSD曲线判断复合物在纳秒到微秒级别下是否稳定
通过MM/GBSA计算定量评估结合自由能,并分解到每个氨基酸残基
这种“对接 + MD + 实验验证”的三位一体策略
上述研究中所使用的SPR表面等离子共振、分子对接、蛋白表达纯化、siRNA、小分子Pull-down、Co-IP等实验技术,金开瑞生物均可提供一站式服务,助您轻松复现高分文献的研究思路。
核心参考文献:Gong W, Yang D, Tang J, Chen Y, Yang T, Zhang W, Zhan Q. Halofuginone is a Molecular Glue Degrader of Integrin β4. Advanced Science, 2026. DOI: 10.1002/advs.202515970.
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










