国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
在准备国家自然科学基金申请时,几乎每个生命科学和医学领域的课题都绕不开一个核心问题:蛋白质之间是如何“对话”的?
蛋白-蛋白互作是细胞功能的执行单元,阐明其机制是研究深度的直接体现。但面对各种各样的研究技术,如何选择、搭配,才能让你的“故事”逻辑严密、无懈可击,从而打动评审专家?
我们为你梳理了8种在国自然申请中极具分量的蛋白互作研究技术。不仅告诉你“是什么”,更关键的是帮你理清“怎么用”和“为什么这样用”,让你的研究方案瞬间“亮”起来!
在展开技术图谱前,先掌握几个让研究方案更严谨的“重要规则”:
❖第一,干湿结合原则。
除湿实验方法外,干实验预测已成为重要佐证。分子对接可模拟结合模式,AlphaFold等多结构预测工具可评估互作结构基础,二者均可增强研究方案的立体感。
❖第二,功能定位区分。
不同技术在互作研究中扮演不同角色:有的适用于筛选未知互作蛋白(如酵母双杂交),有的适用于验证已知互作关系(如SPR、ITC),有的则可同时承担筛选与验证功能(如Co-IP搭配不同检测手段)。明确技术定位有助于合理分配实验资源。
❖第三,多维度验证原则。
蛋白互作的确证需满足:细胞体系验证(体现生理相关性)与非细胞体系验证(证明直接结合)相结合。细胞内实验如Co-IP不能排除桥梁分子的介导作用,细胞共定位仅为支持性证据,因此需结合体外纯化蛋白实验(如GST pull-down、SPR)形成完整证据链。
❖第四,定性定量递进。
从定性描述(是否互作)到定量分析(结合亲和力、动力学参数、热力学特征),证据强度的递进体现了研究深度的提升。
基于上述原则,以下对8种技术进行系统解析。
一、酵母双杂交系统(Y2H)[预实验筛选工具⭐⭐⭐]
1. 核心原理
基于真核转录因子的模块化结构:DNA结合域(BD)可识别特定DNA序列,转录激活域(AD)可启动转录,二者分离时无活性,空间靠近时可重构为功能性转录激活因子。将目标蛋白X与BD融合构建诱饵载体,候选蛋白Y与AD融合构建猎物载体,共转化酵母细胞。若X与Y发生互作,则BD与AD被拉近,重构的转录激活因子驱动报告基因(如HIS3、LacZ、ADE2)表达,通过营养缺陷型筛选或酶活检测判断互作发生。
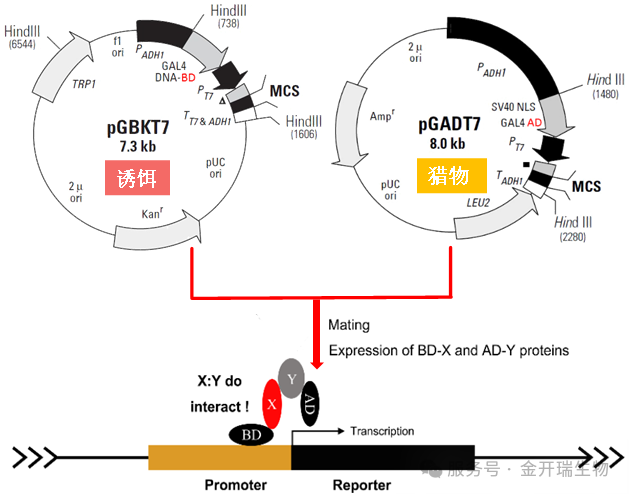
2. 技术流程
✦构建诱饵载体(BD-X)和猎物文库或特定猎物载体(AD-Y);
✦共转化酵母感受态细胞;
✦涂布选择性培养基,培养2-4天;
✦筛选阳性克隆,提取质粒测序鉴定;
✦通过回转验证排除假阳性。
3. 技术特点与定位
优势:高通量,可筛选cDNA文库或突变体文库;灵敏度高,可检测弱/瞬时互作;活细胞体系,接近真核环境。
局限:假阳性率较高(需验证);限于核内互作(除非修饰);转录自激活活性需排除
国自然定位:适用于项目初期寻找新互作蛋白,为研究确定新靶点。
二、免疫共沉淀(Co-IP)[核心必需技术⭐⭐⭐⭐⭐]
1. 核心原理
在非变性条件下裂解细胞,细胞内蛋白复合物得以保留。利用目标蛋白特异性抗体结合固相载体(如Protein A/G琼脂糖珠),从细胞裂解液中免疫沉淀目标蛋白及其互作蛋白。根据猎物蛋白是否已知分为:
CoIP-WB(验证):验证已知蛋白之间在体内是否存在互作关系
CoIP-MS(筛选):高效筛选体内互作蛋白
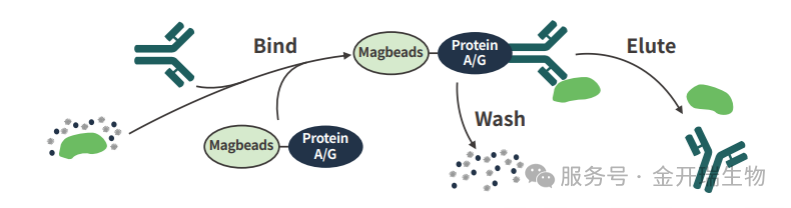
2. 技术流程
✦细胞培养与处理,收集细胞;
✦加入非变性裂解液(含蛋白酶抑制剂),冰上裂解30 min;
✦4℃离心去除细胞碎片,取上清;
✦加入目标蛋白抗体,4℃孵育2-4 h或过夜;
✦加入Protein A/G琼脂糖珠,4℃孵育2 h;
✦离心收集珠子,洗涤3-5次去除非特异结合;
✦加入SDS上样缓冲液,煮沸5 min洗脱复合物;
✦SDS-PAGE分离,Western blot检测或质谱鉴定。
3. 技术特点与定位
优势:细胞内近生理条件,结果最具生物学意义;可验证已知互作,也可联合质谱筛选未知互作。
局限:不能区分直接结合与间接结合;受抗体质量影响大;低亲和力或瞬时互作可能漏检。
国自然定位:作为细胞内互作的核心证据,几乎是所有蛋白互作研究的“标配”。
三、GST pull-down[一般必需技术⭐⭐⭐]
1. 核心原理
GST pull-down技术是一种用于研究蛋白质相互作用的分子生物学方法。该技术通过基因重组将目标探针蛋白与谷胱甘肽S-转移酶(GST)融合表达,形成融合蛋白。利用GST与谷胱甘肽(GSH)的特异性结合特性,将融合蛋白固定在偶联有GSH的琼脂糖微球上。当含有潜在相互作用蛋白的样品通过该亲和层析系统时,能够与融合蛋白特异性结合的靶蛋白会被选择性捕获,从而实现蛋白质互作复合物的分离与鉴定。
2. 技术流程
✦构建GST-X融合表达载体,转化表达菌株;
✦IPTG诱导表达,裂解菌体,获得GST-X融合蛋白;
✦GSH琼脂糖珠与GST-X孵育,4℃结合2 h;
✦制备含候选蛋白Y的样品(细胞裂解液或纯化Y蛋白);
✦将结合GST-X的珠子与Y样品孵育,4℃过夜;
✦洗涤珠子去除非特异结合,SDS上样缓冲液洗脱;
✦Western blot检测Y蛋白,或用考马斯亮蓝染色/质谱鉴定。
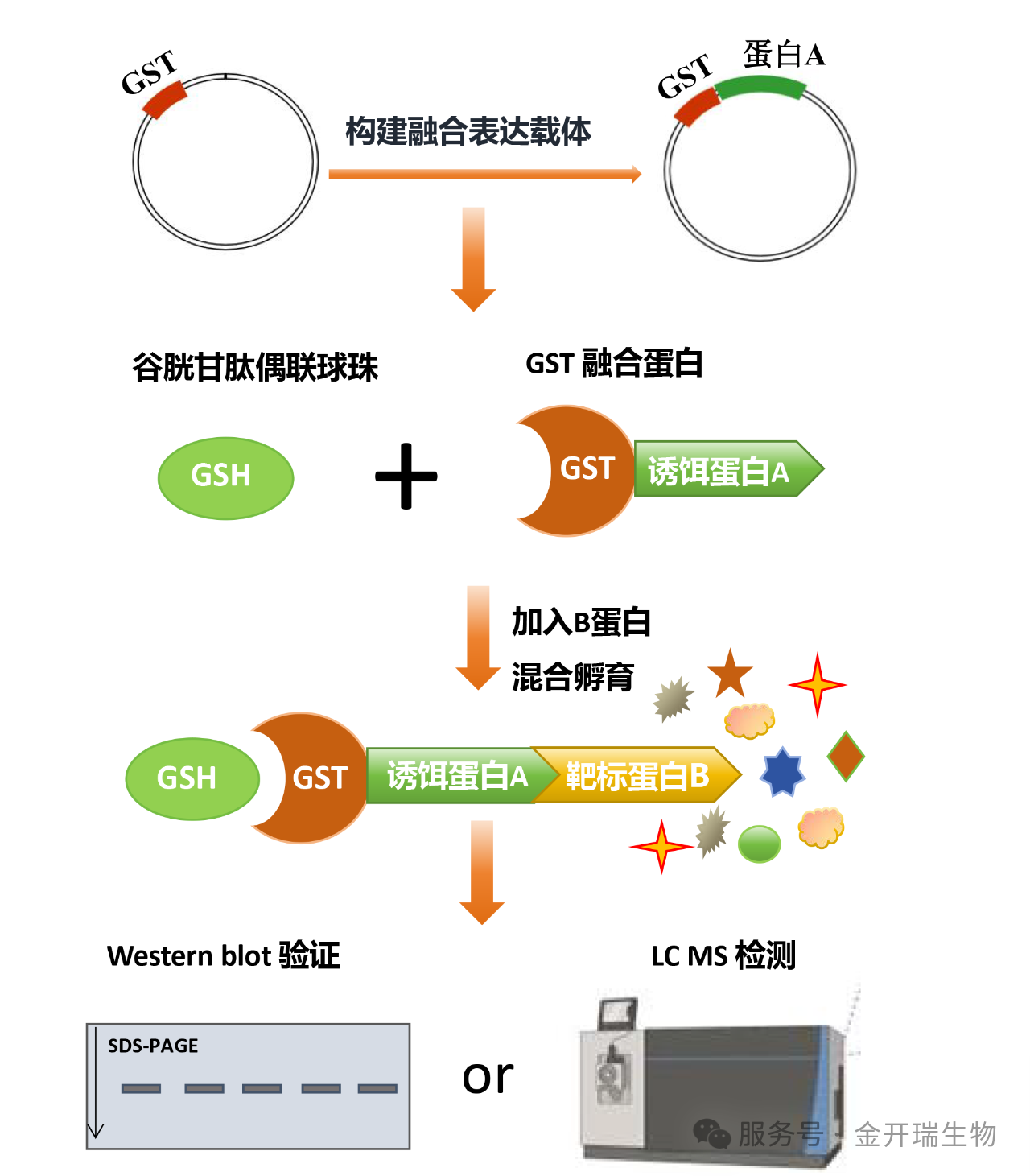
3. 技术特点与定位
优势:可验证直接互作(使用纯化蛋白时);不受细胞内环境影响;可结合质谱进行未知互作筛选。
局限:蛋白需可溶性表达;GST标签可能影响蛋白构象;体外环境与生理状态有差异。
国自然定位:可与Co-IP形成“细胞-体外”互补证据链,证明互作的直接性。
四、免疫荧光共定位[一般必需技术⭐⭐⭐]
1. 核心原理
利用特异性抗体(或融合荧光蛋白)分别标记两种目标蛋白,通过荧光显微镜观察二者在细胞内的空间分布关系。若两种荧光信号在亚细胞结构上高度重叠,提示二者可能在该区域发生互作。
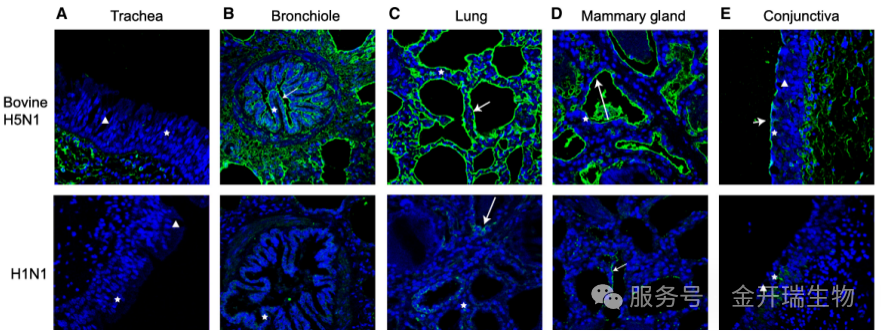
来源:doi:10.1016/j.cell.2025.01.019
2. 技术流程
✦细胞接种于共聚焦专用培养皿,培养至适宜密度;
✦转染荧光蛋白融合表达载体,或进行免疫荧光染色(固定、通透、封闭、一抗孵育、荧光二抗孵育);
✦激光共聚焦显微镜采集图像,多通道采集;
✦图像分析软件计算共定位系数(Pearson系数、Manders系数等);
✦统计分析共定位程度。
3. 技术特点与定位
优势:提供互作的空间信息;可视化直观;可用于活细胞动态观察(荧光蛋白标记)
局限:共定位不等于互作(分辨率限制);受抗体特异性和荧光串色影响;定性为主。
国自然定位:作为互作的空间支持证据,为机制研究提供细胞定位线索。
五、表面等离子共振(SPR)[加分亮点技术⭐⭐⭐⭐⭐]
1. 核心原理
基于光的全内反射现象,当偏振光以特定角度入射至金属膜(通常为金膜)表面时,金属中的自由电子与光波发生共振,导致反射光强度在特定角度(SPR角)显著降低。SPR角对金属膜表面介质的折射率极其敏感。当溶液中的分子与固定在芯片表面的分子结合时,局部折射率改变,引起SPR角实时偏移,通过监测角度变化跟踪结合与解离全过程。
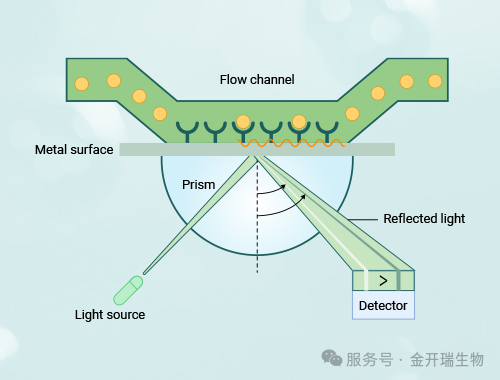
2. 技术流程
✦将配体分子(如蛋白A)共价偶联于传感器芯片表面;
✦基线稳定后,注入含分析物(如蛋白B)的溶液,记录结合曲线(结合速率ka);
✦切换为缓冲液,记录解离曲线(解离速率kd);
✦软件拟合数据分析,计算结合常数KA(ka/kd)和平衡解离常数KD(kd/ka);
✦不同浓度分析物重复实验,进行动力学拟合芯片再生,进行下一轮分析。
3. 技术特点与定位
优势:实时监测,无需标记;提供动力学参数(ka、kd)和亲和力常数(KD);样品消耗少;可进行多循环动力学分析。
局限:需纯化蛋白且质量高;固定化可能影响蛋白活性;设备昂贵,操作需专业培训。
国自然定位:提供结合亲和力的定量数据,是验证互作最可靠的体外证据之一。
六、双分子荧光互补(BiFC)[加分技术⭐⭐⭐⭐]
1. 核心原理
原理是将荧光蛋白分割成两个不具有荧光活性的分子片段(N-fragment和C-fragment),然后将这两个荧光蛋白的片段分别融合到两个目标蛋白上。实验中需要设置Nyfp和cyfp的两个空载对照。
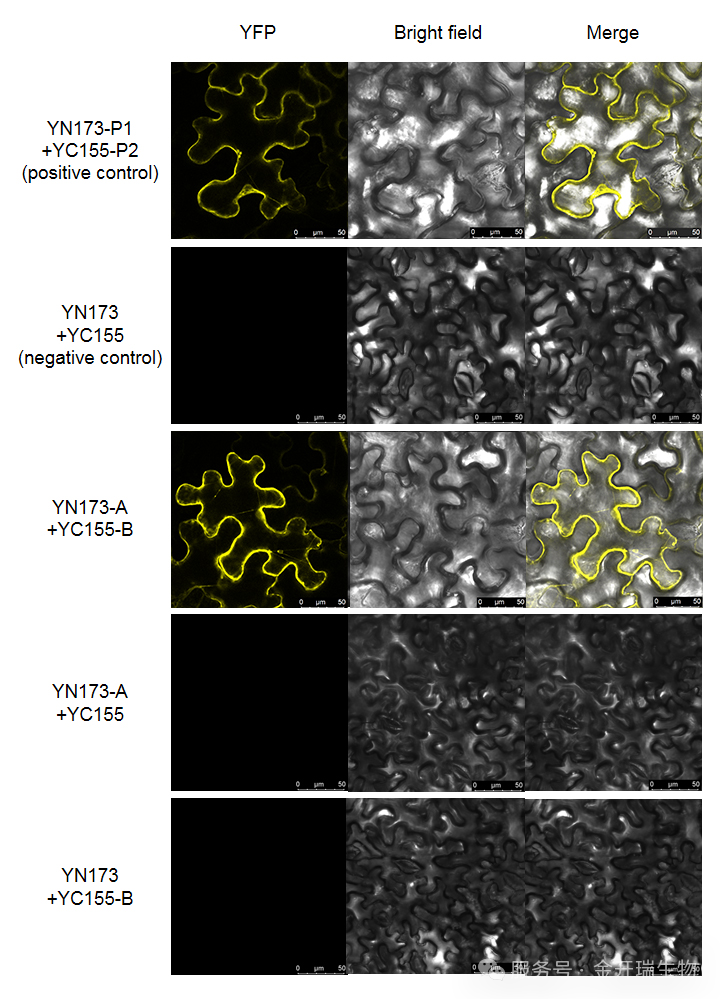
2. 技术流程
✦构建目标蛋白的BiFC载体(VN-A和VC-B)。
✦将质粒共转染HEK293T细胞。
✦37℃培养24-48小时后,通过共聚焦显微镜观察荧光信号。
✦定量分析荧光强度(ImageJ或Flow Cytometry)。
3. 技术特点与定位
优势:活细胞检测,实时原位;灵敏度高;可定位互作发生位置;可用于高通量筛选
局限:荧光片段互补不可逆,无法监测解离;荧光成熟需时间(数十分钟至数小时);易产生假阳性(自发互补)
国自然定位:提供活细胞中互作的可视化证据,体现技术前沿性。
七、萤光素酶互补(LCA)[加分技术⭐⭐⭐⭐]
1. 核心原理
是在BiFC基础上发展出来的一种研究蛋白互作的技术,是将萤光素酶切成N端和C端两个功能片段,并分别与待检测的目标蛋白融合。如果两个目标蛋白有相互作用,则N端片段和C端片段在空间上靠近并互补,从而发挥萤光素酶活性,催化底物产生光。
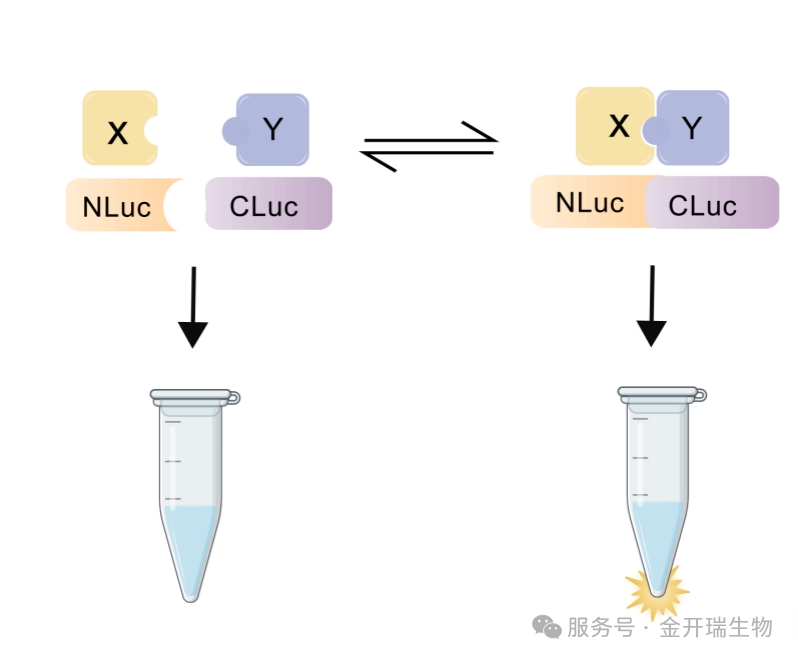
2. 技术流程
✦构建融合载体:X-NLuc和Y-CLuc(或其他片段组合);
✦共转染目的细胞,培养24-48 h;
✦裂解细胞,加入荧光素酶底物;
✦化学发光仪检测发光强度;
✦通过发光值定量评估互作强度,可进行药物处理或突变影响分析。
3. 技术特点与定位
优势:灵敏度高,动态范围宽;定量准确;背景低(无自发荧光);适用于药物筛选和互作调控研究
局限:片段互补有一定不可逆性;需严格对照排除假阳性;无法提供空间定位信息(如需定位,可结合成像系统)
国自然定位:适用于需要定量比较(如突变体效应、药物抑制效应)的互作研究。
八、等温滴定量热分析(ITC)[加分亮点技术⭐⭐⭐⭐⭐]
1. 核心原理
直接测量生物分子结合过程中释放或吸收的热量。在恒定温度下,将一种分子(配体)通过注射器逐次滴入含有另一种分子(受体)的样品池中。每次注射后,分子结合引起的热量变化由仪器记录,随着配体浓度增加,结合逐渐饱和,热量变化逐渐减小。通过分析热量变化与配体浓度的关系,获得结合常数(Ka)、化学计量比(n)、结合焓变(ΔH)、结合熵变(ΔS)和结合自由能(ΔG)。
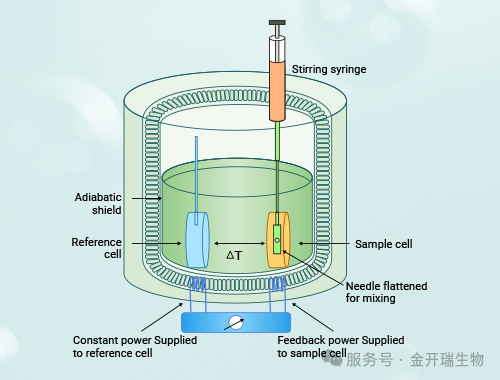
2. 技术流程
✦样品准备:受体蛋白置于样品池,配体蛋白置于注射器,缓冲液高度匹配;
✦仪器平衡至设定温度,基线稳定;
✦进行空白滴定(配体滴入缓冲液)扣除稀释热;
✦正式滴定:逐次注射,每次注射后记录热功率变化至基线;
✦积分每次注射的热量峰,获得结合等温线;
✦软件拟合至合适结合模型(如单点结合模型),计算热力学参数。
3. 技术特点与定位
优势:唯一可直接测定结合焓的技术;无标记,溶液体系;一次实验获得完整热力学信息;揭示结合驱动力(焓驱动/熵驱动)。
局限:蛋白需求量大(毫克级);蛋白需高纯度且缓冲液高度匹配;数据分析需专业知识;低亲和力结合检测受限。
国自然定位:揭示互作的热力学本质,体现研究的深度和系统性。
技术组合策略建议
基于上述技术定位,结合研究阶段和证据强度需求,建议如下组合策略:
|
研究阶段 |
推荐技术组合 | 解决的问题 | 证据强度 |
|
筛选阶段 |
Y2H + Co-IP/MS | 发现新互作蛋白,初筛验证 | 中等 |
|
验证阶段 |
Co-IP + GST pull-down + 共定位 | 细胞内存在+直接结合+空间定位 | 较高 |
|
深化阶段 |
+ BiFC/LCA + SPR | 活细胞可视化+亲和力定量 | 高 |
| 机制解析阶段 |
+ ITC |
热力学特征+结合驱动力 | 最高 |
蛋白互作研究已从单一的“是/否”判断,发展为集筛选、验证、定位、定量、热力学分析于一体的多层次证据体系。合理选择和科学组合上述技术,构建从现象到本质、从定性到定量、从体外到细胞内的完整证据链,将使您的国自然申请更具竞争力和说服力。
金开瑞在分子互作领域深耕多年,可以提供从实验设计、样品处理、数据分析到结果解读的全方位定制化服务,满足您的各种个性化需求;同时,我们也自主研发了各种分子互作相关的试剂盒,可以提供实验前的咨询和实验过程中的技术指导,帮助您更好地理解实验过程和结果。
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










