IF:12.6首报!黄芪来源外泌体样纳米颗粒三重机制协同治疗前列腺癌
前列腺癌(PCa)是全球男性泌尿系统最常见的恶性肿瘤之一,尤其在晚期阶段,不仅治疗手段有限,且容易产生耐药。近年来,植物来源的类外泌体纳米颗粒(plant-derived exosome-like nanoparticles, PELNs)因其天然的纳米结构和生物活性,正逐渐成为肿瘤治疗领域的新兴工具。其中,源自中药的PELNs在多种癌症模型中展现出良好的治疗潜力,然而,目前尚缺乏将其应用于前列腺癌的相关研究。黄芪(Astragalus membranaceus)作为一味经典中药,虽已被证实具有免疫调节和抗肿瘤活性,但其活性成分的递送效率低下和作用机制不明确,始终是限制其临床转化的关键瓶颈。
2026年3月12日,华中科技大学同济医学院附属同济医院王少刚、夏启东团队在《Journal of Nanobiotechnology》发表了一篇题为“Therapeutic translation of traditional Chinese medicine Huangqi derived exosome like nanoparticles: targeting prostate cancer through ferroptosis activation, immune reprogramming, and microbiome modulation”的创新研究,从新鲜黄芪中提取出外泌体样纳米颗粒(HELNs),并通过单细胞测序、16S rDNA测序和转录组学多组学整合分析,系统揭示了HELNs通过“直接杀伤+免疫重塑+菌群调控”三重机制抑制前列腺癌的作用。
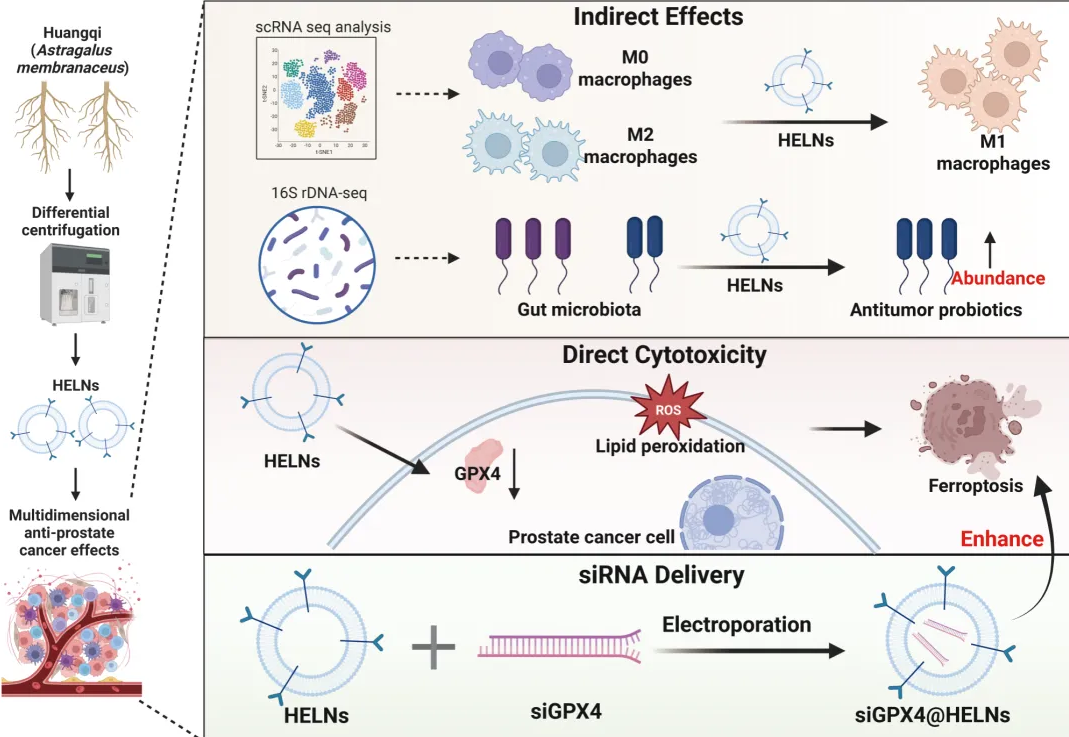
一、研究创新点
❖填补PELNs在前列腺癌治疗领域的空白
本研究是首个将中药来源外泌体样纳米颗粒应用于前列腺癌治疗的系统性研究,为PELNs在前列腺癌领域的应用开辟了新方向。
❖多组学整合揭示三重抗肿瘤机制
研究首次将单细胞测序、16S rDNA测序和bulk RNA-seq相结合,全面解析HELNs在体内外的作用机制:
直接诱导铁死亡:HELNs下调GPX4蛋白表达,诱导脂质过氧化和Fe²⁺积累;
免疫重塑:逆转M2型TAMs向M1型极化,增强抗肿瘤免疫;
菌群调控:显著富集抗肿瘤益生菌Akkermansia muciniphila,并通过粪菌移植实验证实其抗肿瘤作用可传递。
❖构建siGPX4@HELNs纳米载药系统,实现协同增效
利用可逆电穿孔技术将靶向GPX4的siRNA装载入HELNs,构建siGPX4@HELNs。该纳米颗粒在体内外均显著增强铁死亡诱导效果,抑瘤效果优于单独使用HELNs,且未引起明显器官毒性。
❖为中药现代化研究提供新范式
本研究展示了从“中药活性成分”到“天然纳米囊泡”再到“靶向递送系统”的完整研究路径,为传统中药的现代化转化提供了可借鉴的研究策略。
二、研究思路
1、HELNs的提取与表征
研究团队通过差速离心法从新鲜黄芪根中成功提取出HELNs。透射电镜(TEM)显示其为典型球形囊泡结构,纳米颗粒追踪分析(NTA)测得粒径主峰为112 nm,Zeta电位稳定,批间一致性良好(CV < 2%)。脂质组学分析揭示HELNs的主要脂质成分为神经酰胺(Cer, 29.7%)、磷脂酸(PA, 16.2%)等,其中高含量的Cer(一种由长链脂肪酸和鞘氨醇脱水形成的酰胺化合物)提示其可能通过多泡体途径分泌,具有较强的生物活性和递送潜力。
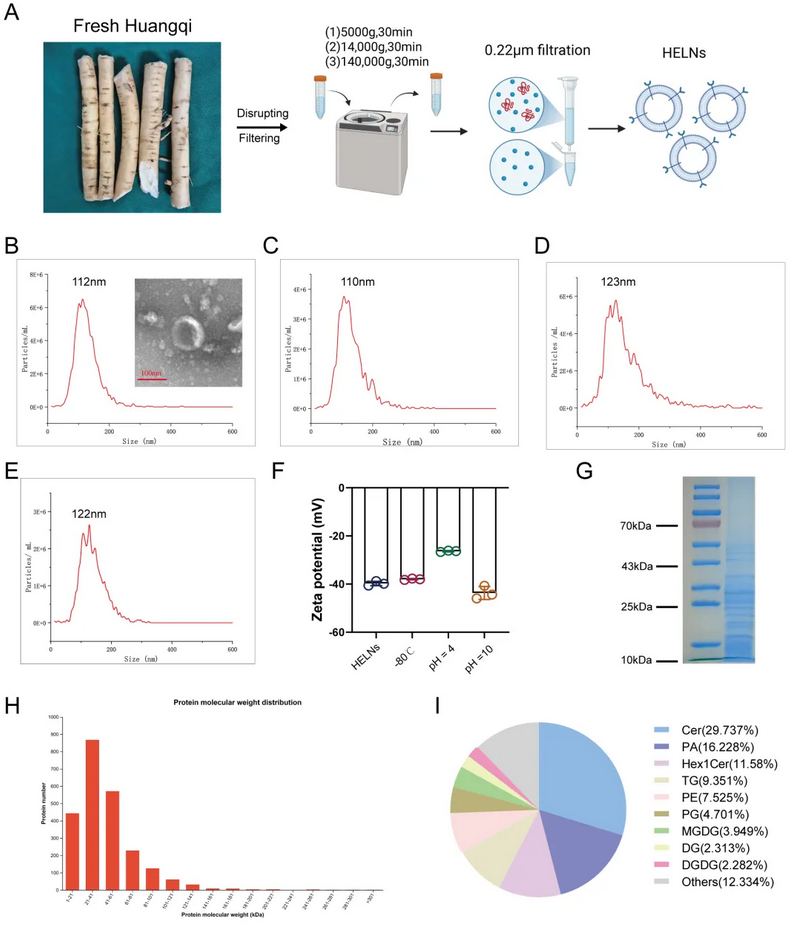
图1.HELNs的提取流程与表征
2、HELNs的体外摄取与抗肿瘤效果
PKH26标记的HELNs与四种前列腺癌细胞(22Rv1、LNCaP、PC-3、C4-2)共孵育后,流式细胞术显示细胞以时间依赖性方式高效摄取HELNs,其中C4-2摄取最快(12 h达98%)。CCK-8检测显示HELNs呈浓度和时间依赖性抑制四种前列腺癌细胞活力,总体而言,浓度为 32 至 64 µg/mL 时,细胞活力降低至约 50%。因此,在后续实验中,选择32μg/mL作为低浓度组,64μg/mL作为高浓度组来治疗前列腺癌细胞。同时,HELNs可诱导前列腺癌细胞凋亡、抑制克隆形成和Transwell迁移能力,且对正常前列腺上皮细胞RWPE-1毒性较低。体内实验比较了腹腔、静脉和灌胃三种给药途径,腹腔注射在有效抑瘤的同时对小鼠体重无明显影响,因此被选为后续主要给药方式。
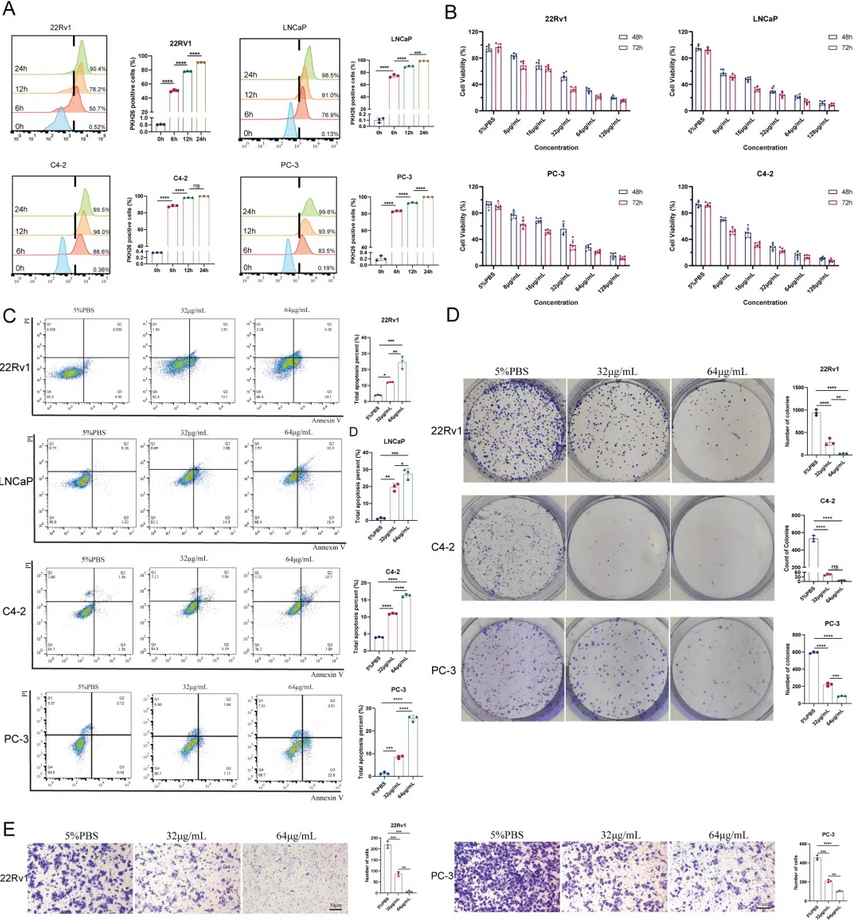
图2.前列腺癌细胞对HELNs的摄取及HELNs的体外细胞毒作用
3、单细胞测序揭示HELNs重塑肿瘤免疫微环境
对6例小鼠皮下瘤样本进行单细胞RNA测序(20个簇的36,424个高质量细胞),发现HELNs治疗组中免疫细胞比例显著增加,尤其是M1型巨噬细胞和中性粒细胞。细胞通讯分析显示HELNs 处理后,M1巨噬细胞与其他免疫细胞的相互作用增强,其功能基因(Nos2、Tnf、Il12)表达上调,而M2型巨噬细胞比例下降。KEGG分析显示M1巨噬细胞富集于IL-17信号通路、TNF信号通路和脂质代谢通路。总之,单细胞测序揭示,HELNs重塑了前列腺癌的肿瘤微环境,特别是通过提升抗肿瘤M1型巨噬细胞的比例和功能状态。
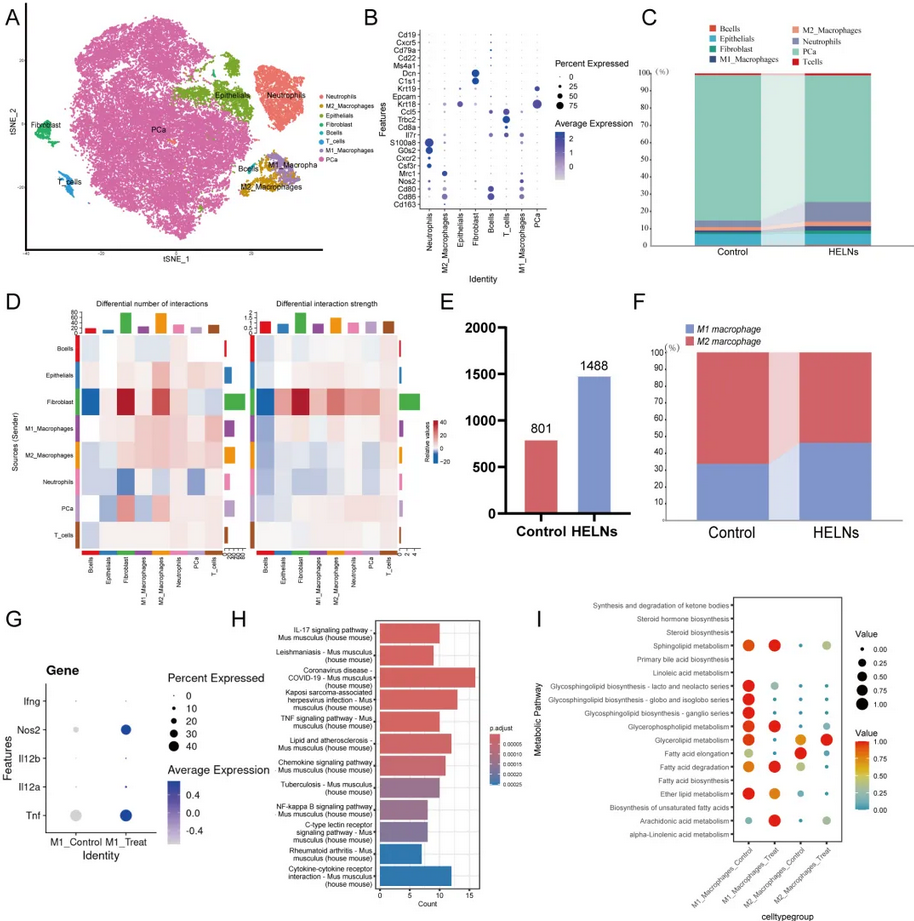
图3.单细胞测序揭示HELNs重塑瘤内免疫格局
4、HELNs逆转M2型巨噬细胞极化,诱导M1型极化
体外实验中,HELNs处理小鼠骨髓来源巨噬细胞(BMDMs)后,M0巨噬细胞中M1标志物(Nos2、Cd80、Tnfa)表达升高;在IL-4诱导的M2巨噬细胞中,HELNs显著上调M1标志物、下调M2标志物(Cd206)。WB证实HELN 增加了 M0 巨噬细胞中 iNOS(基因名称 Nos2)和 ARG1 的表达。此时,ARG1表达的轻微上调是巨噬细胞功能激活的正常表现,因为这种表达也可以在IFNγ诱导的M1巨噬细胞中检测到。体内实验进一步验证:HELNs腹腔注射显著抑制C57BL/6小鼠皮下RM-1肿瘤生长,流式细胞术和免疫荧光染色显示肿瘤内M1巨噬细胞比例增加、M2减少,且肝肾功无明显异常。
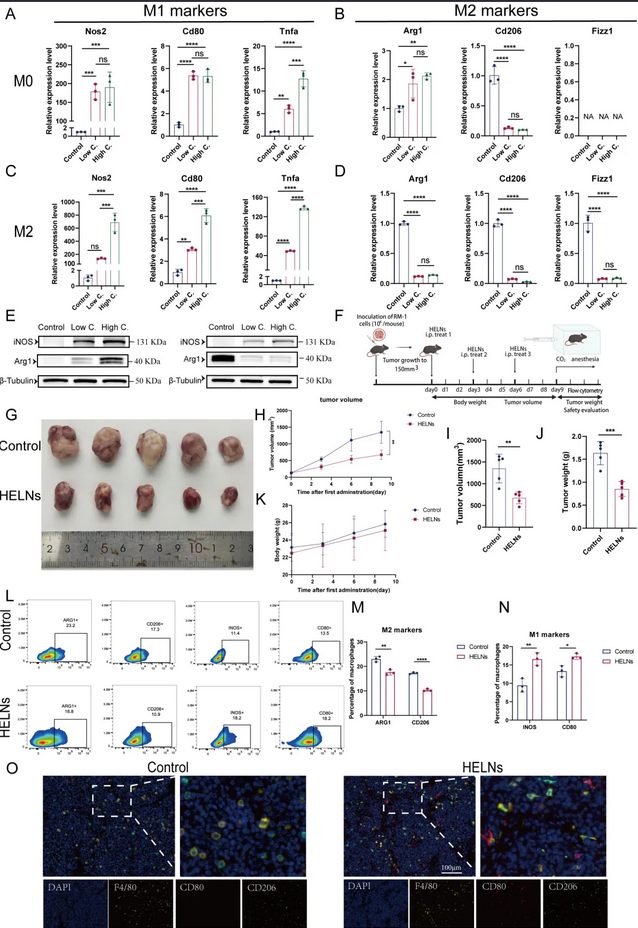
图4 . HELNs逆转M2型极化、诱导M1型极化
5、HELNs富集肠道抗肿瘤益生菌
DiR标记的HELNs体内分布显示其主要聚集于肠道、肝脏和脾脏,提示可能影响肠道菌群。16S rDNA测序发现HELNs处理组小鼠肠道中疣微菌门(Verrucomicrobia)、阿克曼氏菌属(Akkermansia)等抗肿瘤益生菌丰度显著升高,而总体α多样性无显著改变。粪菌移植(FMT)实验证实:移植了荷瘤小鼠粪便的受体小鼠肿瘤生长加快,而移植了经HELNs治疗小鼠粪便的受体小鼠肿瘤负荷显著减轻,证明 HELNs 对肠道微生物群的改变有助于其抗肿瘤作用。
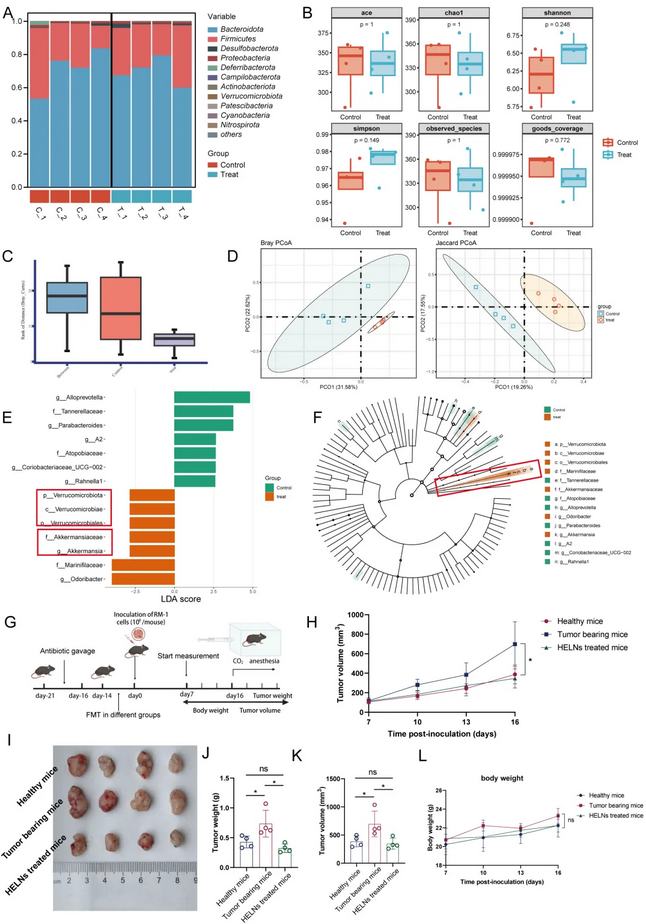
图5. HELNs通过改变肠道菌群发挥抗肿瘤作用
6、HELNs诱导前列腺癌细胞铁死亡
转录组测序显示HELNs处理22Rv1细胞后,“铁死亡”和“氧化应激”相关通路显著富集。透射电镜下观察到典型铁死亡线粒体形态(线粒体收缩、嵴消失、电子密度增高)。流式细胞术证实HELNs浓度依赖性地增加细胞内ROS、脂质过氧化物和Fe²⁺水平。WB显示GPX4蛋白表达下调,而SLC7A11、ACSL4、FSP1无明显变化,提示GPX4是HELNs诱导铁死亡的关键靶点。BALB/c裸鼠皮下22Rv1移植瘤模型中,HELNs腹腔注射显著抑制肿瘤生长,并减轻肿瘤重量。免疫组织化学染色证实HELNs 处理的肿瘤中 GPX4 表达降低,且肝肾功正常。
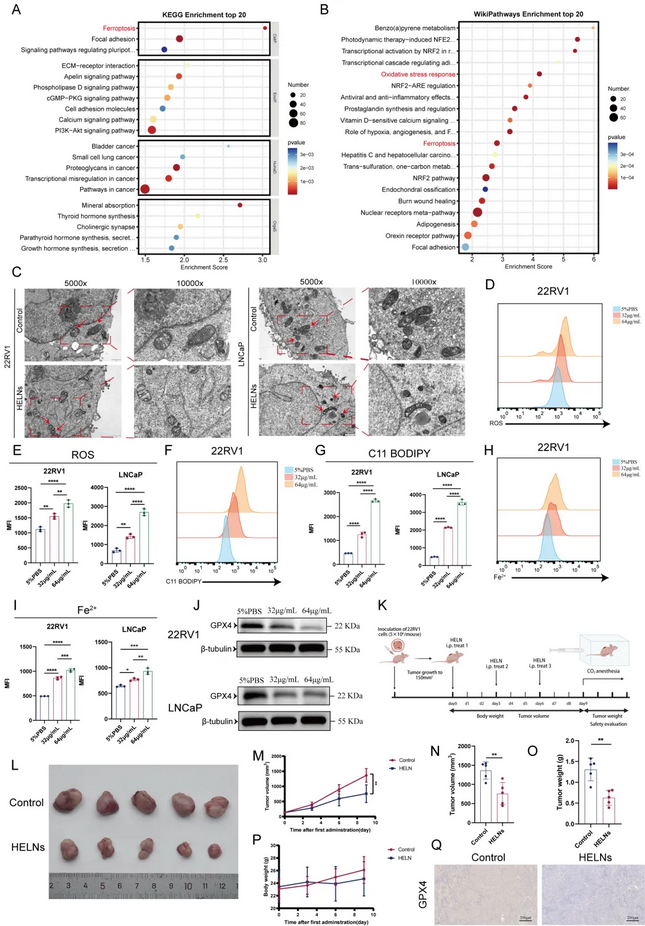
图6 . HELNs通过下调GPX4表达诱导前列腺癌细胞铁死亡
7、siGPX4@HELNs纳米载药系统增强铁死亡疗效
PELNs兼具双重功能:其本身可作为治疗药物,亦可作为天然载体递送特定药物穿越生物屏障、促进细胞摄取。与人工合成载体相比,PELNs体内滞留时间更长,且具有跨物种安全性和低免疫原性优势。基于HELNs本身可通过下调GPX4诱导前列腺癌细胞铁死亡,本研究选择装载siRNA与之协同,以进一步增强治疗效果。首先筛选出高效沉默GPX4的siRNA序列(si2),通过可逆电穿孔将其装载入HELNs,装载效率约50%。荧光显微镜显示siGPX4@HELNs能高效将siRNA递送入细胞。WB证实siGPX4@HELNs比单独HELNs或混合物更显著降低GPX4蛋白水平。功能实验显示siGPX4@HELNs诱导更强的Fe²⁺积累、脂质过氧化和细胞毒性。体内实验中,siGPX4@HELNs治疗组肿瘤体积和重量最小,免疫组化显示GPX4表达最低,且主要器官无明显病理损伤,肝肾功能正常。
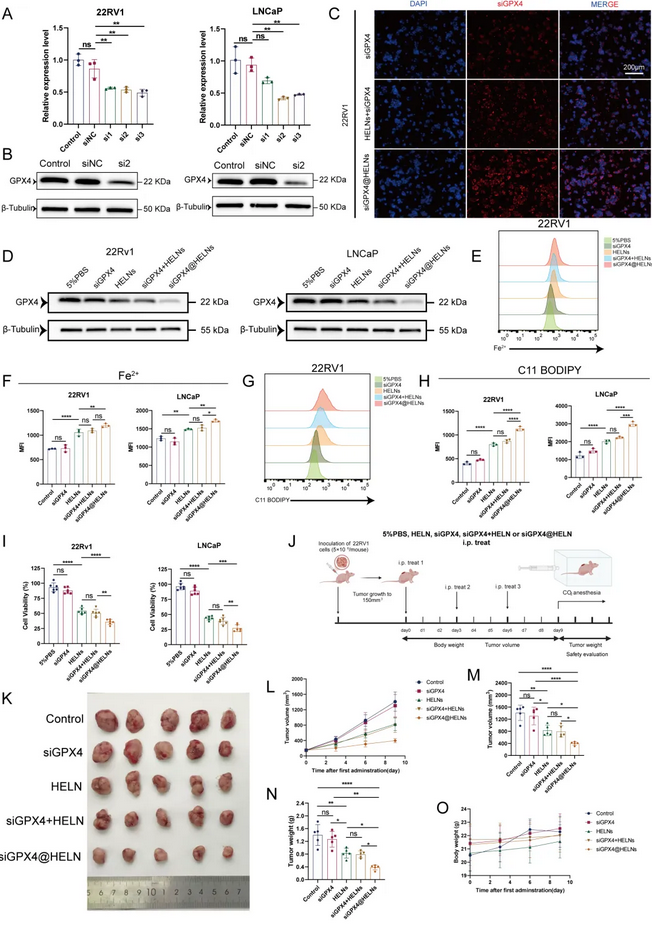
图7.siGPX4@HELNs在体内外对前列腺癌具有良好的治疗作用且安全性良好
三、总结
本研究首次系统揭示了黄芪来源外泌体样纳米颗粒(HELNs)通过以下三重机制治疗前列腺癌:
➤直接机制:下调GPX4,诱导铁死亡;
➤免疫机制:逆转M2巨噬细胞极化,激活抗肿瘤免疫;
➤菌群机制:富集抗肿瘤益生菌,调节肠道微生态。
此外,HELNs作为天然纳米载体,成功递送siGPX4,构建出更具疗效的siGPX4@HELNs纳米药物,展现出良好的安全性和协同治疗效果。
研究局限性
✦活性成分未完全解析:HELNs中具体哪些代谢物或脂质成分发挥核心作用尚未明确;
✦长期安全性需进一步验证:虽然短期未见明显毒性,但长期应用的安全性仍需系统评估;
✦铁死亡机制尚需深入:HELNs如何精准调控GPX4表达,是否涉及转录或翻译后修饰,仍需机制性研究;
✦杂质分离挑战:当前提取方法可能无法完全去除植物源性杂质,影响临床转化。
文献来源:An Y, Xu JZ, Ye GC, Sun JX, Xiang JC, Gong C, Zhang SH, Miao LT, Ma SY, Ding MX, Wang SG, Xia QD. Therapeutic translation of traditional Chinese medicine Huangqi derived exosome like nanoparticles: targeting prostate cancer through ferroptosis activation, immune reprogramming, and microbiome modulation. J Nanobiotechnology. 2026 Mar 11.
最新动态
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!
-
04.07
【客户文献分享】药用真菌槐耳(Huaier)来源外泌体样纳米颗粒:携带miRNA跨物种调控,精准抑制乳腺癌
-
03.24
IF:12.6首报!黄芪来源外泌体样纳米颗粒三重机制协同治疗前列腺癌
-
03.11
同为抗体,为什么一抗看“抗原种类”,二抗却看“一抗种属”?
-
03.11
J Nanobiotechnology(IF=12.6):蔓越莓“纳米邮差”递送麦角甾醇,重启早衰卵巢功能!










