【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
近日,重庆医科大学附属第一医院赵金秋教授团队在肝内胆管癌(iCCA)研究领域取得重要突破,其研究成果发表于国际肝病学顶级期刊 《Journal of Hepatology》:(题为:Distinct molecular pathways regulated by activated AKT and YAP signaling during intrahepatic cholangiocarcinoma progression: Roles of AKT and YAP during iCCA)。该研究首次系统解析了AKT和YAP两条关键致癌信号在iCCA进展中的不同分工,并揭示了YAP作为肿瘤免疫微环境核心调控因子的新功能。值得一提的是,研究团队使用金开瑞ChIP试剂盒,为证实YAP直接抑制靶基因RNF125的分子机制提供了关键性证据。

肝内胆管癌(iCCA)是一种恶性程度高、免疫治疗响应率低的难治性肿瘤。尽管AKT和YAP信号通路在iCCA中常被异常激活,但两者在肿瘤进展及肿瘤免疫微环境(TIME)调控中的具体作用尚不明确。
该研究通过构建两种可诱导的iCCA小鼠模型,首次系统揭示了AKT与YAP的功能分工:AKT主导肿瘤代谢与增殖,其抑制可诱导iCCA完全消退;而YAP是维持肿瘤身份及调控免疫微环境的关键。机制上,YAP通过直接抑制抑癌基因RNF125促进肿瘤进展,并通过排斥T细胞、招募中性粒细胞构建免疫抑制屏障。重要的是,抑制YAP可将免疫“冷”肿瘤转化为“热”肿瘤,增加CD4⁺和CD8⁺ T细胞浸润。然而,这些浸润的T细胞表达PD-1,导致抗肿瘤功能受限。进一步研究表明,YAP抑制联合抗PD-L1治疗可协同增强肿瘤消退。
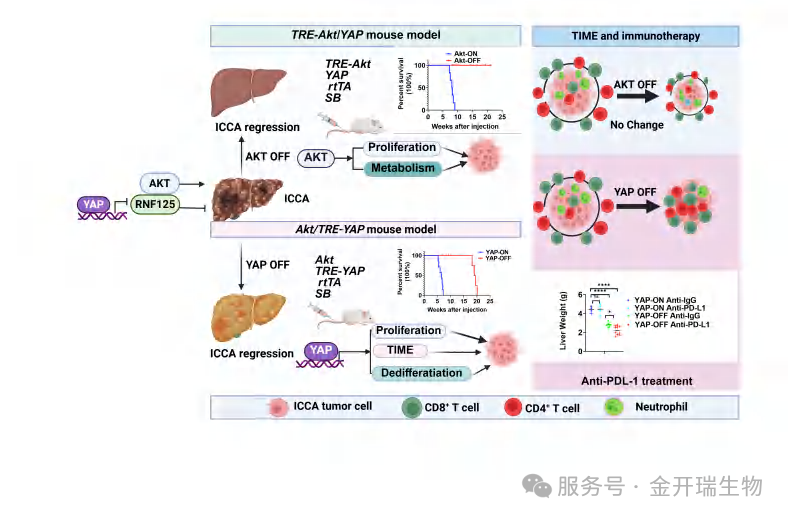
创新模型:可“开关”的双系统
团队巧妙构建了两个多西环素(Doxycycline)诱导的iCCA小鼠模型:
Akt/TRE-YAP模型:在恒定激活AKT的基础上,可随时“开关”YAP表达。
TRE-Akt/YAP模型:在恒定激活YAP的基础上,可随时“开关”AKT表达。
该模型设计使研究者能够在肿瘤形成后特异性关闭单一信号通路,实时追踪肿瘤的表型变化、细胞特性及微环境重塑,为明确 AKT 和 YAP 的独立功能奠定了实验基础。
核心发现一:AKT 与 YAP 存在共性作用,且功能分工明确
研究证实,AKT 与 YAP 并非完全独立的致癌通路,二者均是调控 iCCA 细胞增殖的关键因子,这是两条信号通路协同驱动 iCCA 发生的重要基础;同时,二者在 iCCA 进展中承担着截然不同的功能,存在明确的分工:
AKT主导代谢与增殖:关闭AKT信号(Akt-OFF)后,已形成的iCCA肿瘤几乎完全消退,小鼠获得显著的长期生存获益。RNA-seq 通路分析显示,AKT 主要调控肿瘤细胞的糖代谢、脂肪酸合成等代谢相关通路,其抑制会直接破坏肿瘤细胞的能量代谢平衡,导致肿瘤细胞增殖停滞、凋亡增加。
YAP维持肿瘤身份并塑造免疫微环境:关闭YAP信号(YAP-OFF)后,由于AKT信号持续存在,肿瘤虽缩小但逐渐转化为脂肪变性相关的肝细胞癌(steatosis-HCC),提示YAP是维持iCCA细胞身份的关键。同时,YAP-OFF显著增加了肿瘤内CD4⁺/CD8⁺ T细胞浸润,减少了Ly6G⁺中性粒细胞,表明YAP是构建免疫抑制屏障的“总工程师”。
核心发现二:YAP直接转录抑制抑癌基因RNF125
为进一步探究YAP调控免疫微环境的分子机制,团队通过RNA-seq筛选到在YAP-OFF后显著上调的基因——RNF125(图A)。公共数据库分析显示,RNF125在人类iCCA中低表达,且低表达与患者不良预后相关(图B-D)。那么,YAP是否直接结合RNF125启动子抑制其转录?
为回答这一问题,研究团队使用金开瑞生产的ChIP试剂盒进行了ChIP-qPCR实验。结果显示,YAP/TEAD转录复合物能够直接结合到RNF125基因启动子区域。这一证据确凿地证实了YAP对RNF125的转录抑制作用。后续Co-IP实验进一步揭示,YAP/TEAD通过招募NuRD复合物(含HDAC1、MTA2)实现转录抑制,揭示了YAP作为转录抑制因子的具体机制。
功能验证:在iCCA细胞系中敲低YAP/TAZ可上调RNF125表达(图E-F);过表达RNF125则显著抑制细胞增殖(图G-H)并在小鼠模型中延缓肿瘤形成(图J-L)。以上结果确立了RNF125作为YAP下游关键抑癌基因的地位。
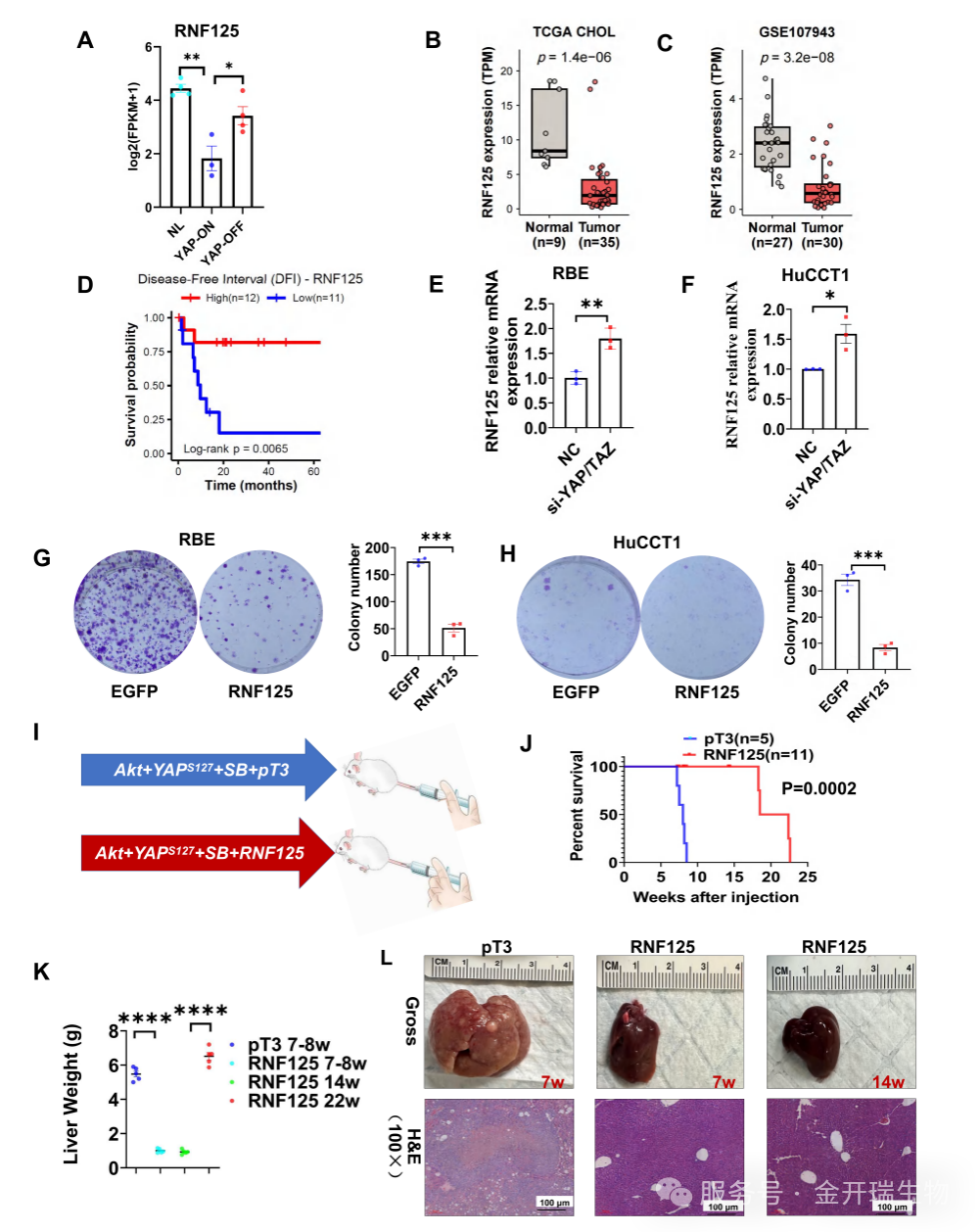
RNF125是YAP的直接靶点,YAP抑制肝内胆管癌(iCCA)的发展
核心发现三:YAP 调控免疫微环境的可逆性,且抑制 YAP 可将 “冷” 肿瘤转为 “热” 肿瘤
YAP 是调控 iCCA 免疫微环境的核心因子,其对免疫微环境的调控具有直接性和可逆性 —— 团队通过双向验证实验证实,YAP 抑制可显著增加肿瘤内 CD4⁺/CD8⁺ T 细胞浸润、减少 Ly6G⁺中性粒细胞,而重新激活 YAP 则会逆转该免疫重塑效应;同时结合 63 例人类 iCCA 组织 IHC 染色及 3 套 19 例患者的单细胞 RNA-seq 数据分析,验证了人类 iCCA 中 YAP/TAZ 激活与免疫抑制特征呈正相关,YAP 激活评分与 T 细胞浸润程度显著负相关。综上,YAP 激活是 iCCA 处于免疫 “冷” 状态的重要诱因,抑制 YAP 可有效打破免疫抑制屏障,将 “冷” 肿瘤转化为 “热” 肿瘤,为后续免疫治疗创造关键条件。
核心发现四:YAP抑制联合PD-L1阻断实现协同治疗
YAP-OFF虽能招募T细胞进入肿瘤,但这些T细胞高表达PD-1,处于耗竭状态(图A-B)这为联合免疫检查点阻断提供了理论基础。基于此,团队设计了联合治疗方案:YAP抑制(撤去多西环素)联合抗PD-L1抗体治疗。结果显示,联合治疗组小鼠肿瘤负荷显著低于单药组(图D-F),且肿瘤内CD4⁺/CD8⁺ T细胞浸润进一步增加(图G-H, J-K),提示YAP抑制可将“冷”肿瘤转化为“热”肿瘤,从而为免疫检查点抑制剂创造响应条件。
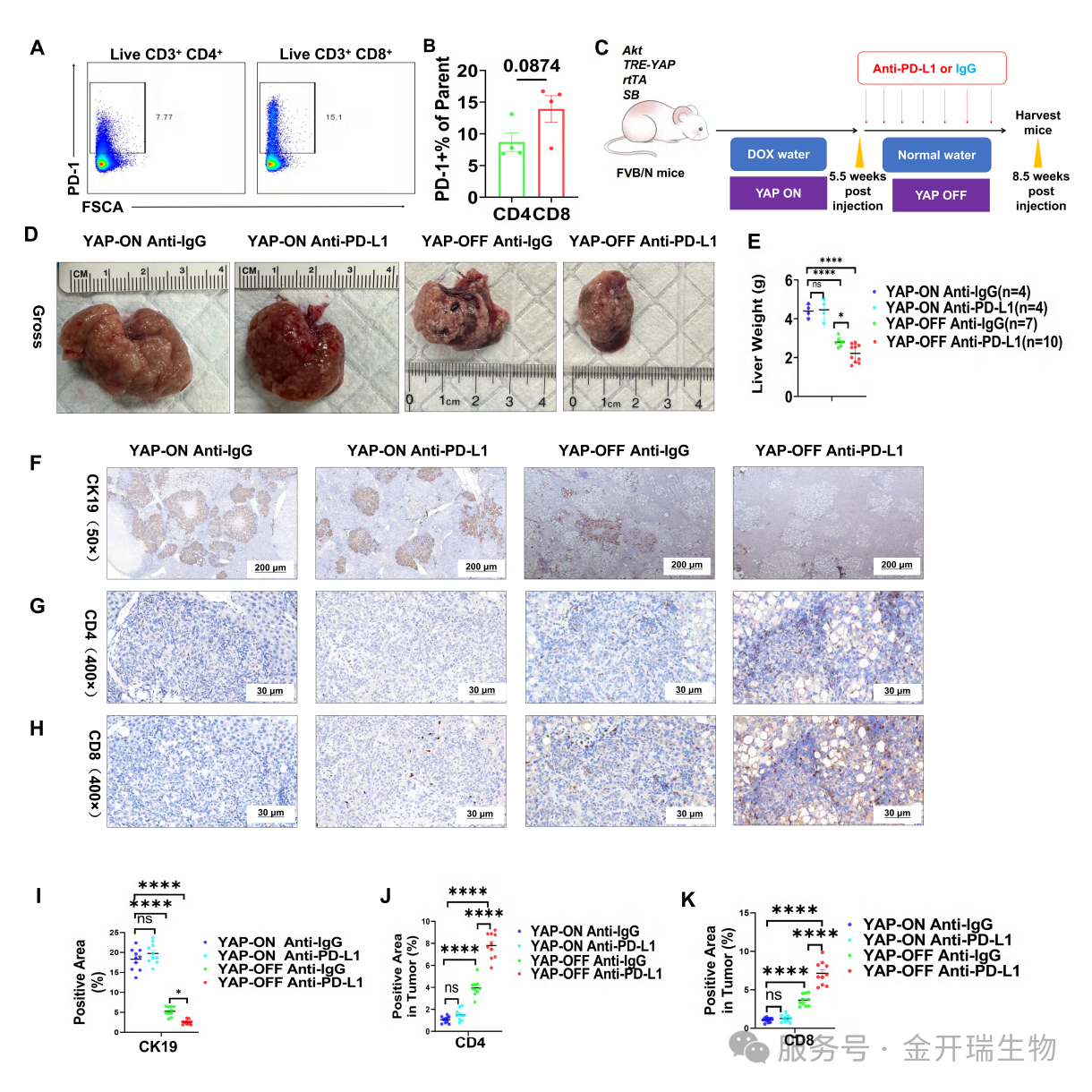
YAP抑制剂联合抗PD-L1免疫检查点阻断协同诱导肝内胆管癌肿瘤消退
研究意义与启示
本研究不仅厘清了AKT和YAP在iCCA中的独特分子通路,更确立了YAP作为肿瘤免疫微环境核心调节因子的地位。关键机制的阐明——特别是YAP直接抑制RNF125并招募NuRD复合物的发现——为开发YAP抑制剂联合免疫疗法提供了坚实的理论基础。
在这项突破性工作中,金开瑞ChIP试剂盒凭借其高灵敏度和特异性,成功助力研究者完成了关键的分子结合验证,使整个信号通路链条得以完整闭合。这正是高质量工具赋能基础研究的生动例证。
如果您正在开展转录调控或表观遗传学相关研究,欢迎来咨询。我们提供动植物专用双平台ChIP试剂盒,可针对不同样本类型提供更精准的解决方案,助力您的机制研究更加深入、数据更加可靠。
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










