分子对接从入门到进阶:“这5张图你必须看懂”!
分子对接(Molecular Docking)是药物设计、蛋白质工程、生命科学领域最常用的计算技术之一。但你真的看懂对接结果图了吗?有些做完对接为什么还要跑分子动力学(MD)?本文将基于典型科研案例,逐图拆解分子对接的“看图要点”与“技术边界”,帮助你从入门到进阶。
一、什么是分子对接?—— 电脑模拟的“锁与钥匙”
分子对接是一种基于计算机模拟的理论方法,旨在预测两个或多个分子(如小分子配体与蛋白质受体)之间的结合模式和亲和力。
用一个经典的比喻来理解:
●生物大分子(蛋白/酶) → “锁”
●小分子(药物/化合物) → “钥匙”
●分子对接→ 电脑算一算:钥匙能不能插进锁里、插得稳不稳、好不好用
换句话说,分子对接就是在原子尺度上,模拟分子之间的“识别”与“结合”过程。

二、分子对接的四大核心目的
| 目的 |
详细说明 |
|
确定结合位点与构象 |
确定配体(如药物小分子、底物)在受体(如蛋白质、酶、核酸)结合口袋中的三维空间位置、取向和构象。同时揭示两者之间的相互作用,如氢键、疏水作用、π-π堆积、静电作用等。 |
|
预测结合强度(亲和力) |
通过计算配体与受体的结合自由能,定量评估它们的结合强弱。结合自由能越负,亲和力通常越强。 |
|
研究生物大分子相互作用 |
研究蛋白质-蛋白质、蛋白质-核酸等大分子复合物的相互作用,为信号传导、酶催化、免疫反应等生命过程提供结构层面的解释。 |
|
指导药物设计与突变改造 |
基于对接结果,优化小分子结构(药物化学)或设计突变体以改变结合特异性。 |
三、分子对接结果图深度解读
很多人初次接触分子对接时,容易陷入一种简化认知:认为无非是将小分子放入蛋白结构,由软件给出一个评分,流程便结束了。
但分子对接真正回答的是:
✔️小分子到底对接在蛋白哪里?
✔️小分子靠什么力抓住蛋白?
✔️这个结合是不是“靠谱且稳定的”?
下面我们以一组典型对接结果图为例(部分图源自文献DOI: 10.1080/15548627.2023.2287930),逐图讲解“看图关键点”。
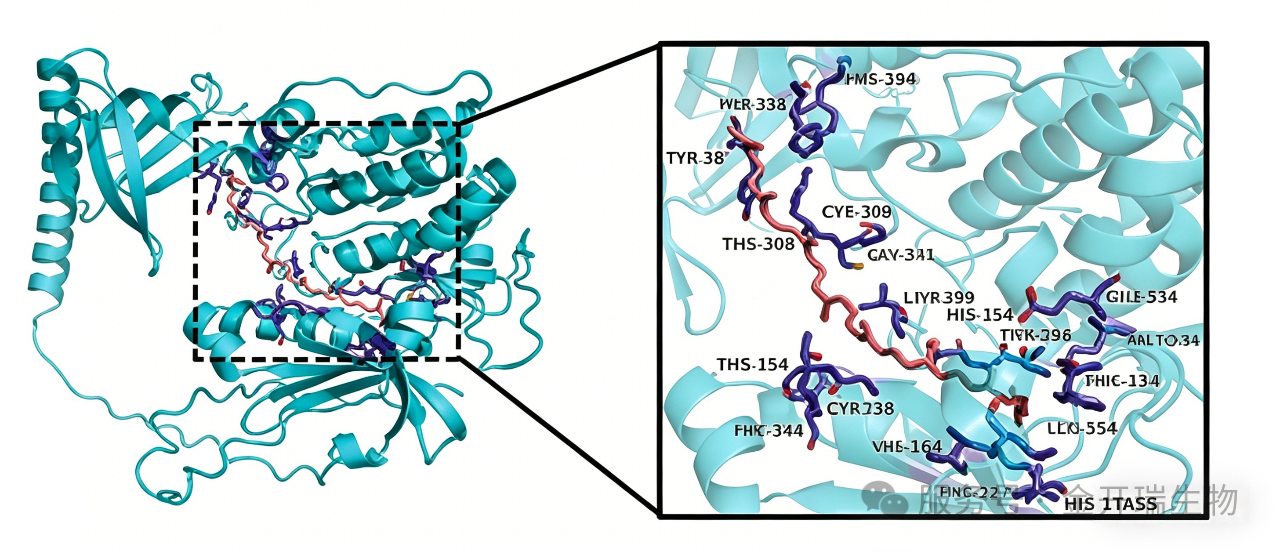
图1. LYC-AKT 分子对接的三维结构
看图第一件事:钥匙有没有插进锁孔里?如果小分子“飘”在蛋白表面之外,哪怕对接分数再高,也难以令人信服。
图中关键信息:使用带状模型(或表面模型)展示蛋白,小分子通常用球棍模型或棍棒模型显示。小分子位于蛋白的某一特定区域——即结合口袋。
这张图回答的是:小分子(LYC)与蛋白(AKT)整体结合的三维形貌。图右侧是结合位点的放大特写,重点展示小分子与蛋白质氨基酸残基之间的直接相互作用,特别是氢键。这张图回答“谁和谁在相互作用”。
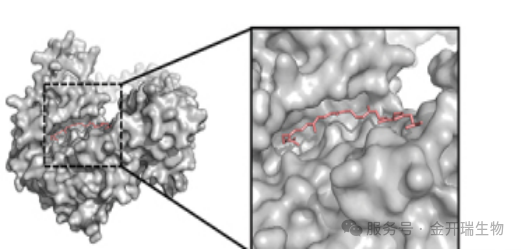
图2. LYC 位于 AKT 蛋白的分子口袋内
这张图中蛋白质表面是用空间填充模型(CPK模型)展示的,让我们看到小分子与蛋白质表面的接触程度——就像看一个模具和铸件的契合度。
看图关键点:
填充度:小分子是否被蛋白质表面紧密包裹?紧密包裹→ 良好契合
空隙:小分子与蛋白表面之间是否有明显缝隙?缝隙→ 可优化空间
接触面积:接触面越大,范德华力贡献越大,结合越稳定
口袋类型:深口袋(深埋)还是浅沟槽(表面)?深口袋通常更稳定
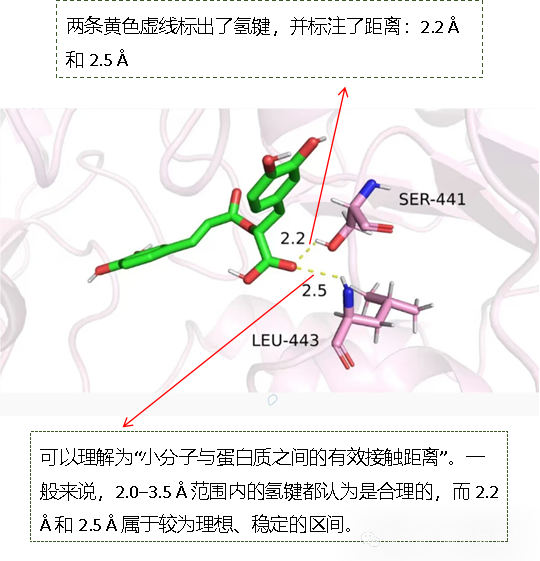
图3. LYC与AKT蛋白残基的氢键相互作用
这张图展示了分子对接中最常见也最重要的相互作用之一 ➔ 氢键。
这张图主要说明了两点:
✔ 小分子并非随意摆放
✔ 它与蛋白质的某些位点(如 SER-441 附近)形成了明确的相互作用
如何判断氢键质量?
在分子对接结果中,氢键是评估结合模式可靠性的关键指标之一。判断氢键质量可从以下四个维度入手:
◆距离:查看图中标注的Å(埃)值。理想情况下,氢键距离越接近 2.5–3.0 Å,作用越强。图中所示的 2.2 Å 和 2.5 Å 均属于优秀范围。
◆角度:虽然二维示意图中通常不标注角度,但在三维结构中理想氢键的供体‑氢‑受体夹角应接近 180°(即呈直线),此时氢键强度最大。
◆数量:多个氢键的协同作用可以显著增强配体与受体之间的结合稳定性。
◆残基类型:某些氨基酸残基因其侧链带有特定化学基团,特别容易形成键,例如:
Ser、Thr、Tyr(含羟基)
Asp、Glu(含羧基)
Lys、Arg(含氨基)
需要强调的是:氢键固然是分子对接中最受关注的相互作用类型,但它并非唯一决定因素。疏水作用、π‑π堆积、盐桥等相互作用同样对结合模式和亲和力具有重要贡献,分析时应综合考量。
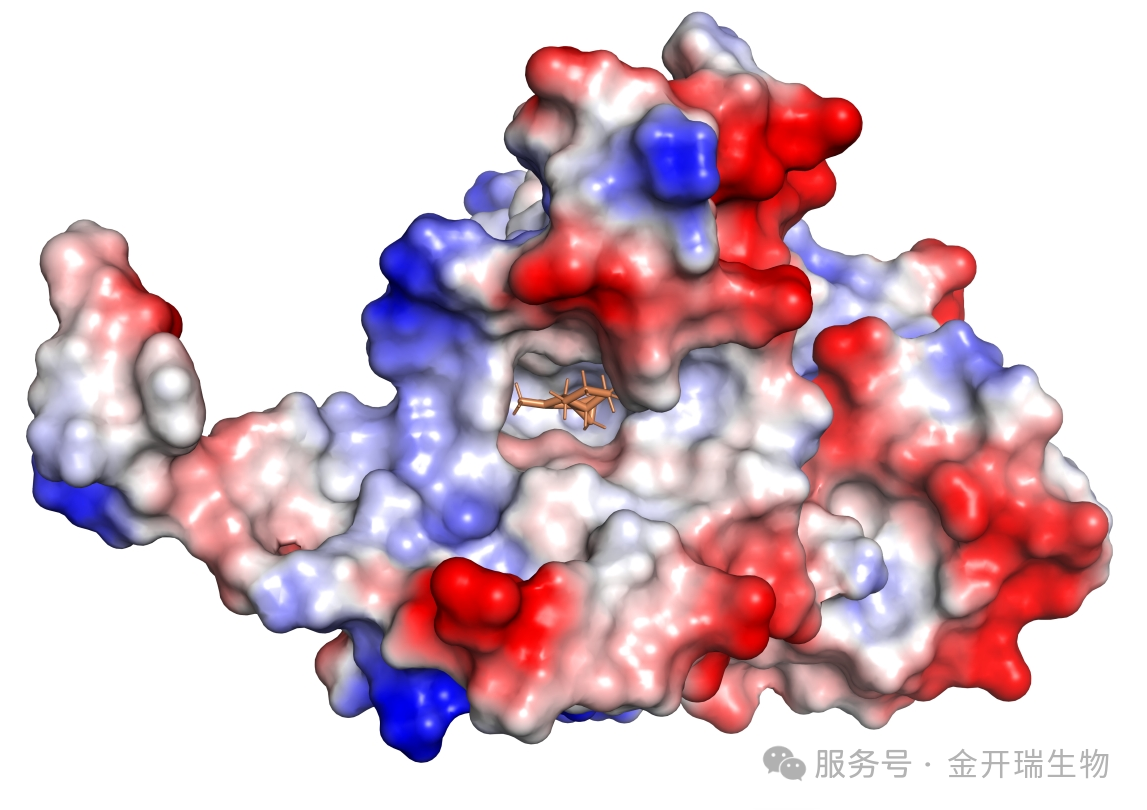
图4. 突变体蛋白与小分子复合体的静电势能表面图
小分子以棕色棍棒模式展示,位于蛋白结合口袋中,通过不同颜色直观呈现蛋白质表面的电荷分布,揭示静电相互作用如何影响分子识别和结合。
颜色含义(可用“异性相吸”概念理解):
红色代表负电,如酸性残基(如Asp、Glu)
蓝色代表正电,如碱性残基(如Lys、Arg)
白色代表中性,如疏水残基(如Leu、Val、Phe)
识别结合位点电荷:观察配体结合处的颜色,是红、蓝还是白?
评估电荷互补性:
配体正电部分→ 蛋白负电区域(红色) = 有利结合
配体负电部分→ 蛋白正电区域(蓝色) = 有利结合
配体疏水部分→ 蛋白中性区域(白色) = 疏水作用
寻找盐桥:红蓝区域相近处可能形成强烈的盐桥相互作用
考虑去溶剂化:结合时水分子被排出,带电区域的水合层变化影响结合能。
为什么静电势很重要?
静电势通过远程引导、电荷互补、强效稳定及pH敏感性四种机制,精准调控分子识别与结合的特异性和效率。而静电势图(如文中图4所示)正是将这些抽象的物理化学特性可视化为红、蓝、白三色分布的蛋白质表面图像,使研究者能够:
直观定位结合热点:一眼看出小分子结合区域是带正电、负电还是疏水环境,从而判断该口袋是否适合目标配体。
指导配体设计与优化:若配体带正电部分正好落在蛋白的红色(负电)区域,说明静电互补良好;反之则提示可能需要修改配体电荷分布。
解释突变或物种差异:当某个关键残基突变导致电荷反转(如从酸性变为碱性),静电势图可直接显示该变化如何破坏原有结合模式。
评估pH依赖性:某些结合事件只在特定pH下发生(如溶酶体、肿瘤微环境),静电势图可帮助预判组氨酸等可滴定残基的电荷状态变化对结合的影响。
简言之:静电势图把“看不见的电荷力”变成了“看得见的颜色块”,让分子对接分析从“猜一猜有没有静电作用”升级为“哪里吸引、哪里排斥,一目了然”。
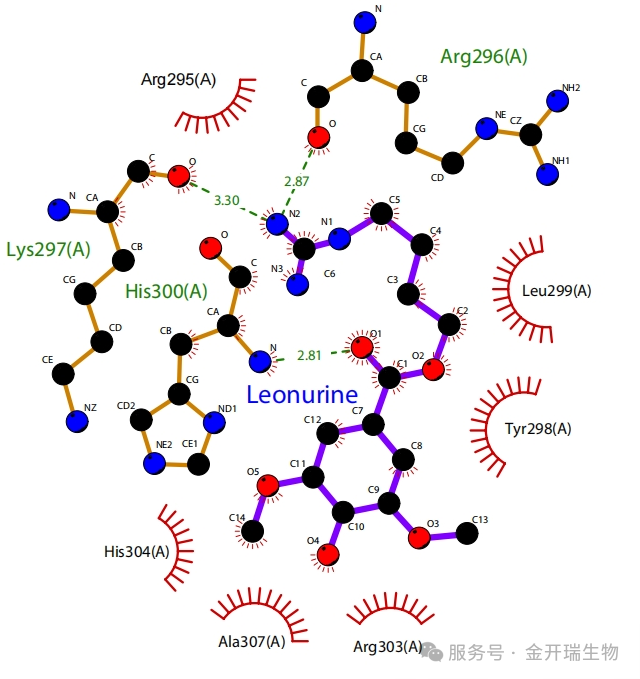
图5. LigPlot 生成的蛋白DNA结合结构域与小分子相互作用的二维示意图
本图为LigPlot 软件生成的 2D 拓扑图,将三维空间的复杂相互作用“摊平”成易读的二维示意图。
图形元素解读:
✔绿色虚线:氢键,并标注距离(Å)
✔红色弧形/ 睫毛状:疏水相互作用
✔参与相互作用的关键氨基酸残基均被清晰标注
这是理解分子对接最实用的一张图!它像一张“地图”,标注了配体与蛋白质的所有接触点,让你一眼看清:
哪些残基参与氢键?
哪些残基提供疏水环境?
配体的哪个化学基团对应哪种作用?
使用建议:在论文或报告中,LigPlot 图应配合三维结构图一起展示,前者负责“关系拓扑”,后者负责“空间真实感”。
四、做完分子对接之后,为什么还要做分子动力学模拟(MD)?
很多人做完对接后会有一种感觉:
“已经有结合构象了,也有对接分数了,还看到了氢键、疏水作用,图也做得很完整——是不是可以结束了?”
但很多研究不会停在这里,而是继续做分子动力学模拟(MD)。
原因很直接:分子对接给出的信息,往往还不够。
分子对接通常无法真正回答以下四个问题:
|
问题 |
说明 |
|
这个结合方式是不是稳定? |
对接只给出一个静态的“快照”,无法判断在热运动下是否会散开 |
|
这些相互作用能维持多久? |
氢键可能在几皮秒内断裂并重新形成,对接无法反映时间尺度 |
|
蛋白和配体会不会在后续发生调整? |
诱导契合效应——对接常假设蛋白刚性,实际蛋白会变形 |
|
这个复合物在动态环境里到底靠不靠谱? |
真实生理环境(水、离子、温度)下,结合模式可能改变 |
而这些,恰恰就是很多研究真正关心的内容。
MD 能补上 docking 没有给出的那部分信息:
✅ 动态稳定性:通过均方根偏差(RMSD)、均方根涨落(RMSF)等指标评估
✅ 结合自由能更精确计算:如 MM-PBSA / MM-GBSA 方法
✅ 构象变化轨迹:观察蛋白-配体复合物随时间的变化
✅ 水分子介导的作用:水桥氢键、水合层对结合的影响
所以,做完对接再做MD,不是为了“把流程做长”,而是因为 MD 能回答 docking 回答不了的那些科学问题。
五、总结
分子对接是分子模拟的起点,而不是终点。
它用“锁钥匹配”的直观逻辑,帮助我们快速筛选、可视化、预测分子间的相互作用。
对于绝大多数药物筛选、突变解释、结合模式确认等场景,分子对接本身已能提供充分、可靠的核心答案——它告诉您“钥匙能否插进锁里、插得稳不稳”。
而当您的研究提出更高要求时(例如:想验证复合物在真实动态环境下的稳定性、追踪构象变化、精确计算结合自由能),则可以在此基础上进阶到分子动力学模拟,让分析从“静态快照”走向“动态解析”。
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










