【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
结直肠癌(CRC)是全球高发的恶性肿瘤,其致死率高的主要“元凶”是极易发生肝转移。在转移过程中,癌细胞并非“孤军奋战”,而是与周围的肿瘤微环境(TME)中的各类细胞,特别是癌症相关成纤维细胞(CAFs),形成复杂的“同盟”关系。然而,驱动这种恶性同盟形成的深层机制——尤其是信号通路、代谢改变与微环境重塑如何被一个核心分子整合——一直是一个未解之谜。
2026年,武汉大学中南医院联合复旦大学上海医学院团队在国际顶级期刊《Advanced Science》(IF: 15.1)上发表了题为“ETV4 Promotes Colorectal Cancer Progression by Reprogramming Asparagine Metabolism to Remodel the Stromal Microenvironment”的研究论文,该研究揭示了一个以转录因子ETV4为核心枢纽的调控网络。ETV4通过同时激活MET正反馈信号回路与ASNS介导的天冬酰胺代谢重编程,实现信号放大与代谢输出的协同调控。肿瘤来源的天冬酰胺作为旁分泌信号分子,进一步诱导肝星状细胞向炎性CAF样表型转化,并重编程原代CAFs分泌HGF,从而形成一个“HGF/MET→ETV4→ASNS+MET→天冬酰胺(Asn)→iCAFs/HSCs→HGF”的双向闭环回路,持续驱动结直肠癌生长与肝转移。这项研究不仅阐明了信号转导、代谢重编程与微环境重塑三者之间的协同机制,也为联合靶向HGF/MET信号与天冬酰胺代谢提供了理论依据与实验证据。
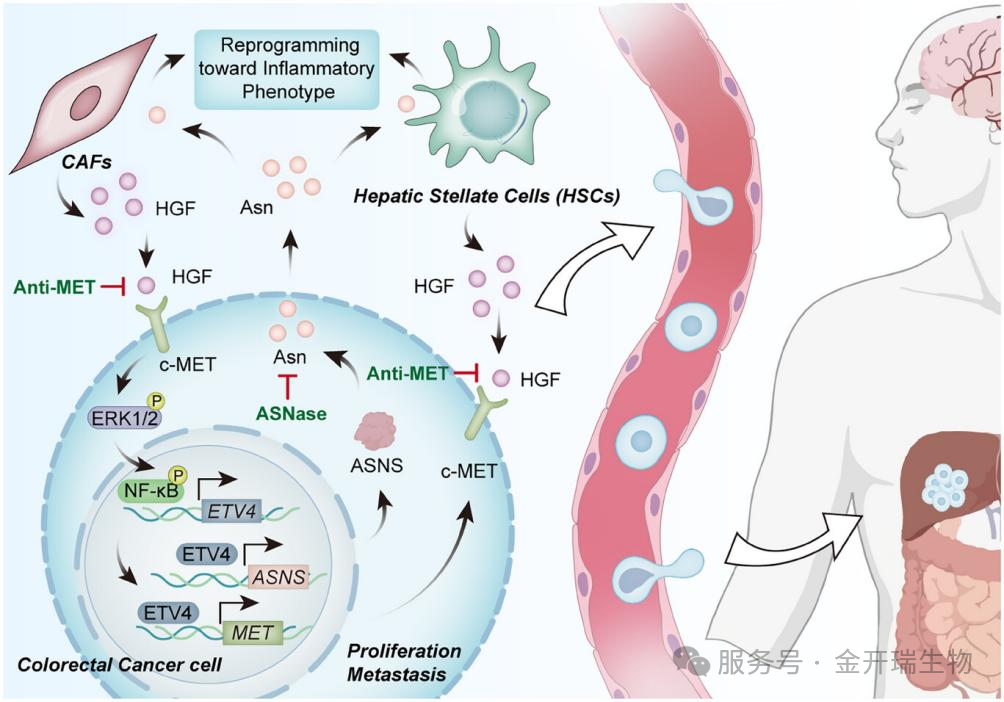
图1. 结直肠癌(CRC)中ETV4中心调控网络的示意模型
一、ETV4——被临床数据锁定的关键候选分子
研究者首先通过高通量筛选寻找与CRC进展相关的关键分子。
筛选策略:对3对CRC肿瘤/癌旁组织进行RNA-seq,锁定6个普遍上调的基因。
临床聚焦:在独立队列(GSE41568)中进一步筛选,发现只有ETV4在肝转移组织中的表达显著高于原发肿瘤,提示其与转移特异性相关。
预后价值:TCGA及多个GEO数据集验证了ETV4在肿瘤中高表达,且其高表达与CRC患者更差的总生存期(OS)显著相关。
细胞定位:单细胞RNA-seq数据显示,ETV4主要表达于恶性上皮细胞(癌细胞),而非微环境中的其他细胞。
结论:ETV4在CRC,尤其是肝转移中异常高表达,是驱动疾病进展和导致不良预后的潜在核心因子。
二、功能验证——ETV4增强体外及体内CRC生长及转移能力
研究者通过经典的细胞和动物功能实验,确证了ETV4的促癌功能。
1、体外功能:ETV4 敲低显著抑制了结直肠癌细胞的增殖、迁移和侵袭能力,而其过表达则产生了相反的效果。此外,ETV4 沉默可诱导细胞凋亡并逆转上皮-间充质转化表型,具体表现为 E-钙黏蛋白表达升高和波形蛋白表达降低;而在 ETV4 过表达时则观察到相反的变化。
2、体内功能:
异种移植瘤模型:敲低ETV4显著抑制肿瘤生长和增殖指数(Ki-67)。
肝转移模型(脾注射):敲低ETV4使肝转移结节数量显著减少、肝脏重量比下降。
在同种免疫健全模型(C57BL/6小鼠)中:MC38细胞中的ETV4沉默显著抑制了皮下肿瘤生长和肝转移形成。
表明ETV4是CRC生长和肝转移的重要驱动因子,且其作用不依赖于免疫背景。
三、机制深挖——ETV4直接转录激活两大关键基因:MET与ASNS
这是全文最核心的机制部分,解释了ETV4如何从分子层面发挥功能。研究者采用“组学整合+分子互作验证”的策略。
下游通路筛选:ETV4沉默的RKO细胞上进行了RNA测序,基因集富集分析(GSEA)显示,ETV4敲低后下调的基因在与恶性表型相关的通路中显著富集,包括NF-κB信号传导、凋亡和局灶粘连(见图2A–C)。
靶基因锁定:整合本研究发现、公共数据库和ChIPBase预测,筛选出8个候选直接靶基因(见图2D)。其中,ASNS(天冬酰胺合成酶)和MET(HGF受体)在mRNA和蛋白水平均随ETV4表达变化而显著改变(见图2E–G,L)。
直接结合验证——ChIP-qPCR的关键作用:
生物信息预测:生物信息学分析在ASNS和MET的启动子区域内发现了四个推定的ETV4结合基序。
双荧光素酶报告基因实验:ETV4过表达显著增强了这两个启动子的转录活性,而删除特定启动子区域(ASNS的−1223至−736 bp区域,MET的−247至−8 bp区域)则显著削弱了这一效应。进一步通过定点突变实验,鉴定出ASNS启动子中的第3个基序和MET启动子中的第1个基序是ETV4激活转录所必需的关结合位点(图2H, I)。
ChIP-qPCR(使用金开瑞ChIP试剂盒):这是证明直接结合的“金标准”。研究者使用ETV4抗体进行染色质免疫共沉淀,随后用qPCR检测预测的结合位点。结果显示,与对照组IgG相比,ETV4抗体能够显著富集ASNS启动子上的site3区域和MET启动子上的site1区域,直接证明了ETV4蛋白与这两个基因的调控区存在物理结合(图2J, K)。
功能回复:敲低ASNS或MET能模拟敲低ETV4的效应(抑制增殖、迁移等),而过表达ASNS或MET则能部分“拯救”由ETV4敲低引起的功能缺陷。
结论:ASNS和MET是ETV4的直接转录靶基因,ETV4通过上调ASNS重编程天冬酰胺代谢,通过上调MET形成信号正反馈,这两个事件共同介导了ETV4的促癌功能。
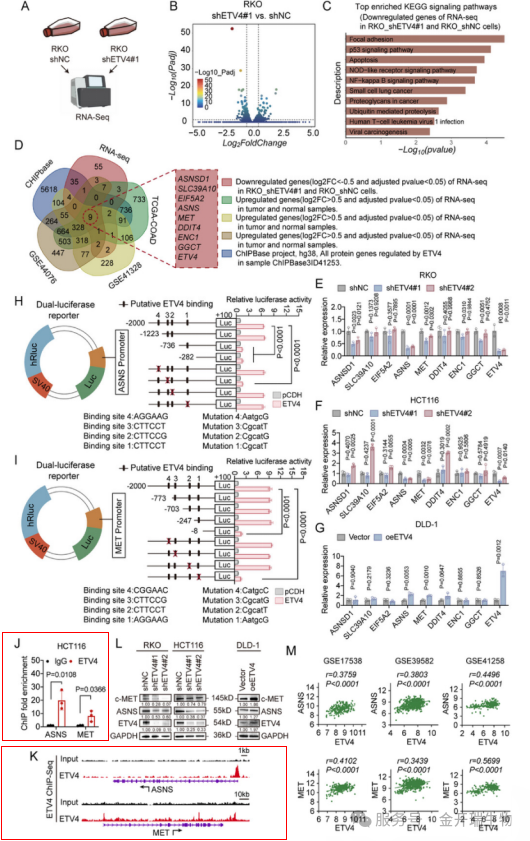
图2. 天冬酰胺合成酶(ASNS)和MET是结直肠癌(CRC)中ETV4的直接转录靶点
(A) 实验流程:比较敲低ETV4(shETV4)与对照(shNC)的RKO细胞RNA测序
(B) 火山图:ETV4敲低后显著变化的基因(|log2FC| > 0.5,校正p < 0.05)
(C) KEGG通路富集:ETV4敲低后下调基因主要富集的信号通路
(D) 韦恩图:本实验下调基因、公共数据上调基因、ChIPBase预测ETV4靶基因三者的交集
(E-G) RT-qPCR验证:在两种CRC细胞中敲低ETV4(E,F)或过表达ETV4(G)后,候选基因的表达变化(n=3)
(H-I) 双荧光素酶报告实验:ETV4过表达对ASNS(H)和MET(I)启动子的激活作用(n=3)
(J) ChIP-qPCR:显示HCT116细胞中ETV4在ASNS和MET启动子区域富集(n=3)(n=3)
(K) ChIP-seq轨迹图(ENCODE数据):显示ETV4在ASNS和MET启动子区的结合峰
(L) 蛋白免疫印迹:敲低或过表达ETV4后,ASNS和MET蛋白水平的变化
(M) 相关性分析:多个公共CRC数据集中ETV4与ASNS、MET mRNA表达的正相关性(Pearson相关)
四、HGF/MET信号通过ERK1/2–p65依赖机制激活ETV4表达,形成正反馈环
研究者继续溯源,探索ETV4本身是如何被上调的。
HGF以剂量依赖方式诱导ETV4的mRNA和蛋白表达,并增强其启动子活性。使用多种通路抑制剂筛选,仅ERK1/2抑制剂(ASTX029)能阻断HGF对ETV4的诱导。通过系统性敲低多个转录因子,发现仅敲低p65能显著抑制ETV4表达和启动子活性。Western blot显示HGF刺激增强了p-ERK、p-p65和ETV4蛋白水平;抑制MET或ERK1/2能阻断p-p65和ETV4的上调;敲低p65能抑制ETV4的表达和入核。
结合“ETV4直接激活MET”的发现,形成HGF→MET→ERK1/2→p65→ETV4→MET↑的正反馈回路。
五、重要发现——天冬酰胺(Asn)作为代谢信号重编程微环境
对人CRC肝转移样本进行scRNA-seq,发现HSC来源的CAFs是成纤维细胞主体,iCAF亚群高表达HGF,myCAF亚群则高表达ACTA2等收缩标记物。HGF-MET配体-受体对在iCAF与肿瘤细胞之间存在显著相互作用。空间转录组数据显示肿瘤与iCAF特征显著正相关。
直接Asn处理LX-2细胞(HSC系),特异性诱导iCAF标志物(IL1B、IL6、CXCL1等)和PDGFR-α表达,不影响myCAF标志物。HGF预处理肿瘤细胞后收集的条件培养基(富含Asn)同样能诱导LX-2向iCAF转化并分泌HGF,该效应可被ASNase逆转。与Asn诱导后的LX-2共培养,显著促进CRC细胞增殖和迁移,可被MET抗体Onartuzumab阻断。
结论:肿瘤细胞通过ETV4-ASNS轴产生并分泌的Asn,不仅是一类代谢物,更是一种旁分泌信号分子。它直接作用于微环境中的HSCs和CAFs,将其“重编程”为HGF高分泌的促癌iCAF状态,这些iCAF分泌的HGF反过来又滋养了肿瘤细胞。至此,一个完整的双向闭环形成:肿瘤细胞→ Asn → iCAFs/HSCs → HGF → 肿瘤细胞 (MET)
六、转化价值——联合靶向HGF/MET和Asn代谢协同抑癌
基于对机制的深刻理解,研究者提出了双管齐下的治疗策略。
(1)临床相关性:在CRC病人组织芯片(TMA)中,ASNS和MET蛋白水平均高于癌旁,且其表达与ETV4呈显著正相关。高表达ASNS或MET的患者预后更差。
(2)联合治疗策略:
靶点1:HGF/MET信号轴 → 使用Onartuzumab(抗MET单抗)。
靶点2:Asn代谢 → 使用ASNase(L-天冬酰胺酶,耗竭Asn)。
(3)体内疗效:
皮下模型:在ETV4过表达的DLD-1移植瘤中,单用Onartuzumab或ASNase均能一定程度抑制肿瘤生长,但联合治疗组的抑瘤效果最为显著。
肝转移模型:同样,在脾注射肝转移模型中,联合治疗使肝转移结节数量和肝脏重量比降至最低。
结论:同时阻断HGF/MET信号和剥夺Asn,能从根源上切断肿瘤细胞的内在驱动力和微环境的外部支持力,产生协同抗肿瘤效应,为CRC尤其是ETV4高表达的晚期患者提供了极具前景的联合治疗新方案。
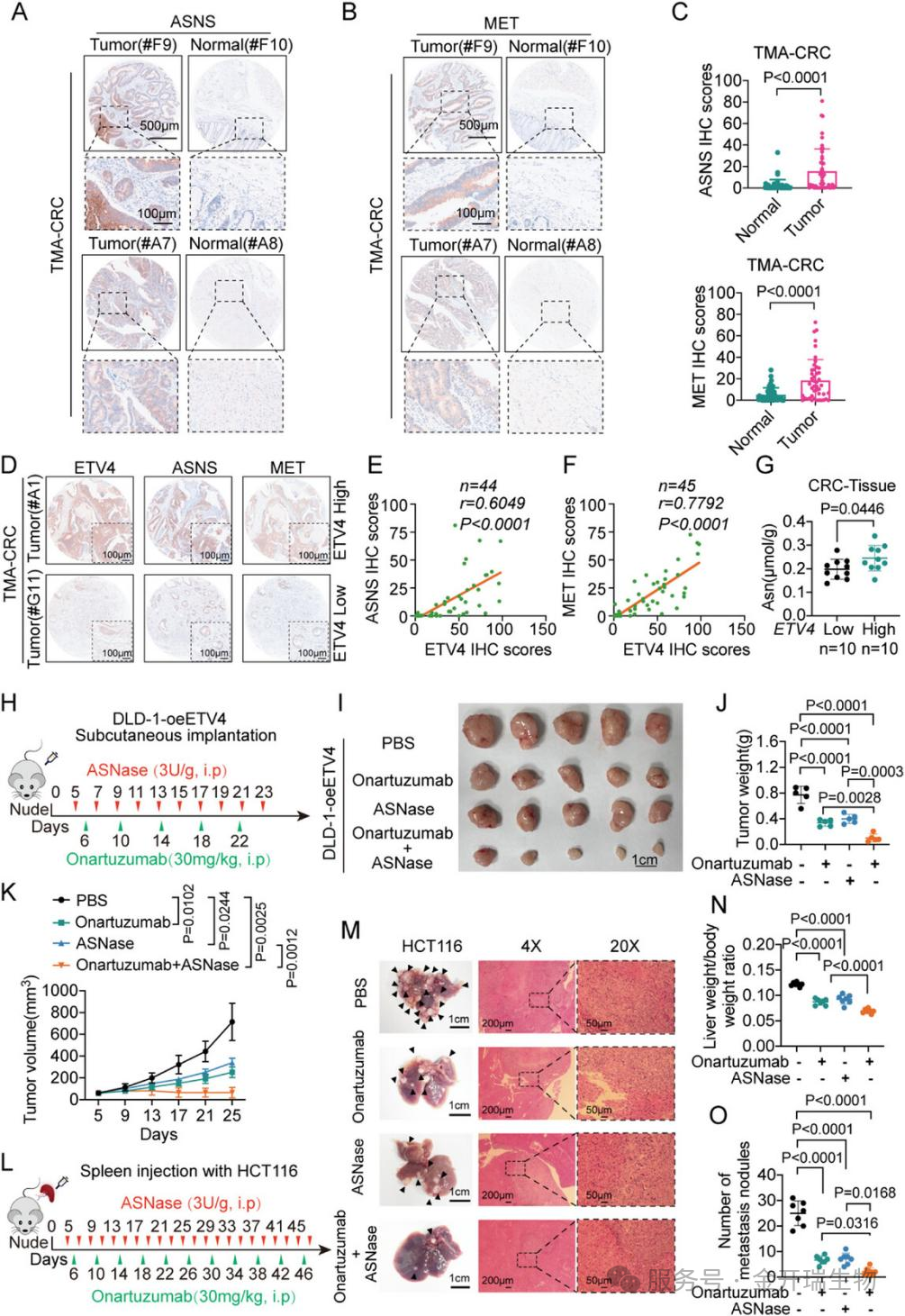
图3. 联合用Onartuzumab和天冬酰胺(Asn)阻断MET阻断可抑制结直肠癌(CRC)的生长和转移
本研究以严谨的逻辑层层递进,完整揭示了ETV4作为转录因子如何同时激活ASNS和MET,将信号放大、代谢重编程与微环境重塑串联为一个正反馈调控网络,为CRC肝转移提供了深刻的机制洞见,也为联合靶向治疗指明了新方向。
在这一机制解析过程中,染色质免疫共沉淀(ChIP)技术发挥了关键作用。正是通过ChIP-qPCR实验,研究者才直接证实了ETV4与ASNS、MET启动子区域的物理结合,为“ETV4是二者直接转录因子”这一核心结论提供了不可替代的证据。
这也正是金开瑞ChIP试剂盒所擅长的应用场景。目前,该试剂盒已助力多篇高水平SCI论文成功发表,其稳定可靠的性能在大量科研实践中得到了充分验证。无论您是专注于转录因子靶基因验证,还是从事表观遗传调控机制解析,金开瑞都能为您提供省心、高效、可信的技术支撑,助您产出高质量的研究成果。
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










