分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
一、技术背景概述
分子动力学(Molecular Dynamics, MD)模拟是研究蛋白质-配体复合物动态行为的强大工具,就像用计算机给原子和分子“拍动画片”——根据物理规则(比如原子间的吸引或排斥),计算每个原子每分每秒的位置和速度,把它们的运动过程连起来,就能看到微观世界里的“慢动作镜头”。通过MD模拟,我们可以了解:复合物是否稳定、关键相互作用是否持续存在、以及哪些氨基酸残基在结合中起核心作用。
二、应用方向
◆药物筛选与优化
研究药物与靶标蛋白的结合模式与亲和力,预测结合稳定性及耐药机制,指导药物开发。
◆蛋白质结构与功能研究
研究蛋白折叠、构象变化(如酶活性、信号传导、异常聚集等)及突变影响,揭示疾病机制与干预靶点。
◆核酸结构与功能研究
研究DNA/RNA构象变化、药物对核酸的干扰、核酸-蛋白互作(如转录因子、修复酶)、基因编辑机制及核酸药物可行性。
◆实验指导设计
基于分子动力学模拟,验证突变体设计及虚拟筛选分子的可行性。
三、核心结果图表解读
以下为分子动力学模拟中常见的分析图表及其解读方法。理解这些图表是判断模拟质量、提取生物学结论的关键。
1、均方根偏差(RMSD)曲线
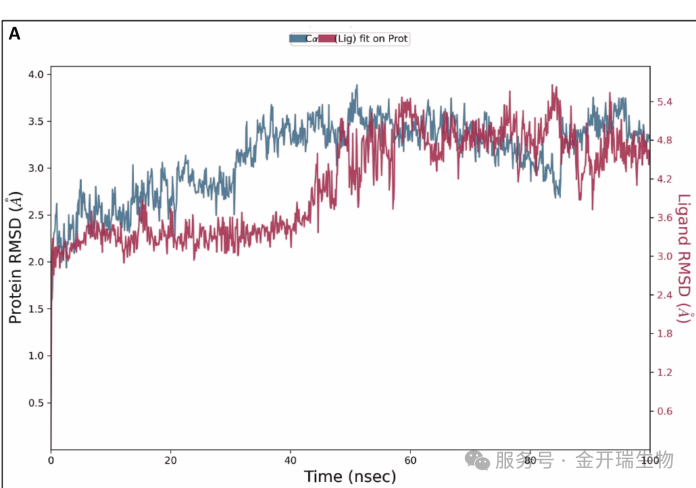
RMSD 的两条曲线
图表形式:横坐标为模拟时间(通常为纳秒),纵坐标为RMSD值(单位:Å或nm)。图中通常包含两条曲线:一条代表蛋白质主链(如Cα原子),另一条代表配体。
含义:RMSD衡量每一时刻的结构相对于初始参考结构的平均偏离程度。它是评估体系是否达到平衡稳定的首要指标。
如何看图?
|
RMSD 范围 |
稳定性评价 |
说明 |
|
< 2.0 Å |
★★★★★ 极度稳定 |
构象几乎无变化 |
|
2.0-3.0 Å |
★★★★ 稳定 |
正常波动,良好结合 → AP8ii (前 50ns) |
|
3.0-5.0 Å |
★★★ 可接受 |
有一定波动但整体稳定 → AP8ii (60-100ns) |
|
> 5.0 Å |
★★ 不稳定 |
构象显著变化或配体解离 |
平台期判断:当曲线在模拟后半段(如50 ns之后)围绕某一平均值小幅波动,不再持续上升,说明体系已收敛至稳定构象。
数值范围:对于蛋白质,RMSD稳定在2‑3 Å以内通常认为结构稳定;若超过5 Å,提示可能发生了较大的构象变化或部分去折叠。
配体曲线:配体RMSD应保持在3 Å以内,表示其在结合口袋中稳定结合。若配体RMSD持续上升并远离蛋白曲线,提示配体可能发生脱离或结合模式改变。
曲线对比:若蛋白与配体RMSD同时升高但保持同步,可能表示整体构象重排而非结合丧失。
示例解读:在100 ns模拟中,前60 ns蛋白RMSD逐步上升至2.5 Å,在 60 和 100 ns 之间的轨迹中 RMSD 突然增加,可能是由于初始蛋白-配体相互作用后的构象变化。值得注意的是,没有观察到实质性的结构改变,肽的构象在 CCR8 活性位点内保持一致取向。
2、均方根波动(RMSF)图
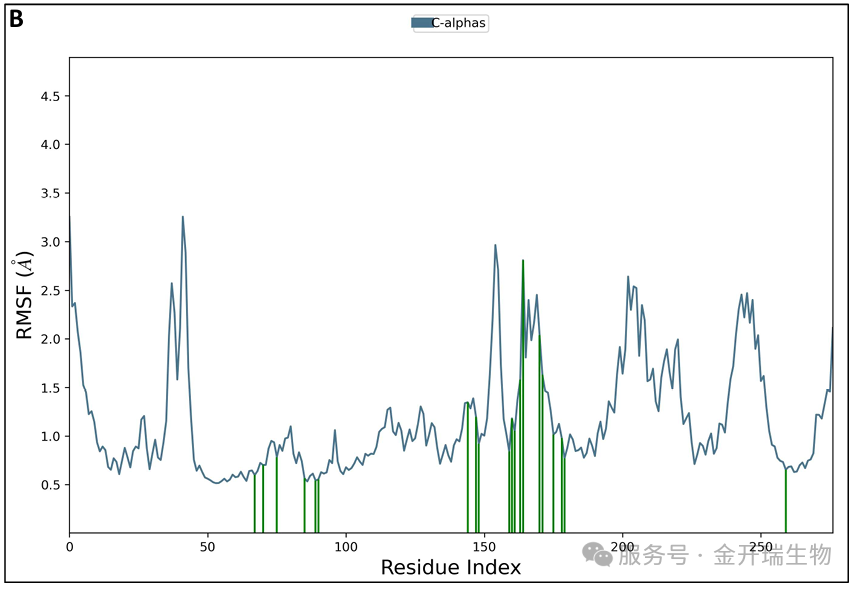
100 ns分子动力学模拟中CCR8蛋白的RMSF图
图表形式:横坐标为氨基酸残基序号(按序列顺序),纵坐标为每个残基的RMSF值(Å)。图中可能用绿色竖线标记与配体有接触的残基。
含义:RMSF (Root Mean Square Fluctuation, 根均方波动) 测量单个残基在模拟过程中的柔性/波动程度。与 RMSD 测量整体偏移不同,RMSF 关注每个氨基酸的“活跃度”。
如何看图?
识别柔性区域:峰值通常出现在loop区、末端(N端/C端),这是正常现象。α螺旋和β折叠区域的RMSF一般较低。
活性位点特征:与配体结合的关键残基通常表现为低RMSF(刚性),因为结合限制了其运动。若活性位点残基RMSF异常高,可能提示结合不稳定或模拟设置问题。
突变影响评估:比较野生型与突变体的RMSF图,若突变导致活性位点附近RMSF显著升高,可能削弱结合亲和力。
绿色竖条:图中标记的绿色竖条表示与配体有接触的残基。观察这些残基的RMSF值是否普遍较低,可验证结合界面的稳定性。
示例解读:
活性位点残基 (Glu286, Tyr113) 等:RMSF 值较低,表明在 AP8ii 结合后保持刚性
Loop 区域 RMSF 较高,这是正常现象,表明活性位点的低 RMSF 支持 AP8ii 稳定结合的结论。
3、回转半径(Rg)曲线
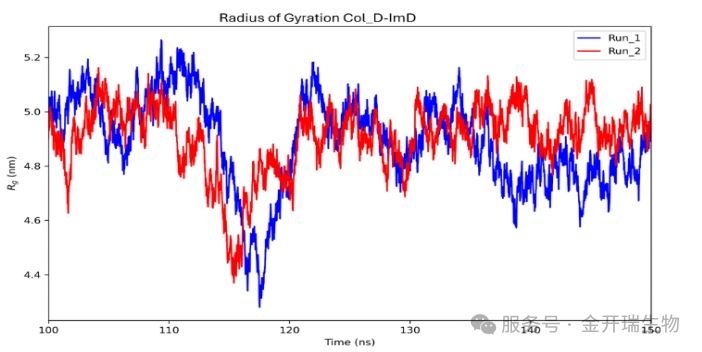
回转半径(Rg)曲线
图表形式:横坐标为模拟时间,纵坐标为Rg值(nm)。
含义:Rg衡量分子整体的紧凑程度,即所有原子质量中心到各原子的平均距离。Rg越小,结构越紧密;Rg越大,结构越松散或展开。它可以帮助我们理解分子在模拟过程中的折叠和展开行为。
如何看图?
趋势判断:若Rg在模拟过程中保持稳定,说明蛋白整体结构紧凑;若Rg逐渐增大,提示蛋白可能发生展开或构象松弛。
事件关联:当RMSD显示大幅波动时,若同时伴随Rg升高,可能表示蛋白发生了明显的构象重排或部分去折叠。
配体结合影响:配体结合后若Rg较未结合状态略有降低,提示结合可能诱导蛋白变得更加紧密。
4、溶剂可及表面积(SASA)曲线
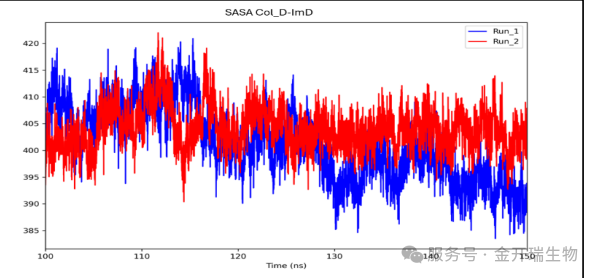
溶剂可及表面积(SASA)曲线
图表形式:横坐标为模拟时间,纵坐标为SASA值(nm²或Ų)。
含义:SASA表示分子表面可被溶剂分子(通常为水)接触的面积。它反映分子的疏水包埋程度及配体结合导致的表面变化。
如何看图?
结合事件:当配体结合到蛋白上时,配体占据部分表面,通常会导致蛋白SASA轻微下降(配体遮挡了原本暴露的区域)。
构象变化:若SASA在模拟中持续增加,提示蛋白可能正在展开,疏水核心暴露。
稳定性判断:稳定的SASA曲线(小幅波动)说明蛋白表面状态平衡。
5、自由能主成分分析图
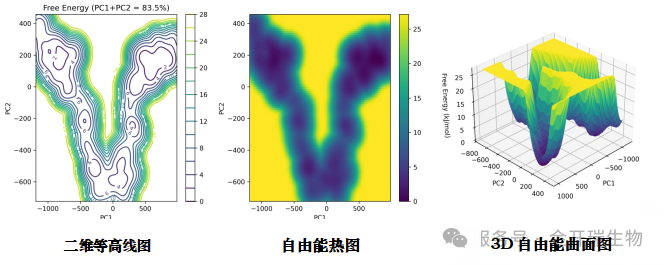
本组合图属于分子模拟与构象分析领域,是基于主成分分析(PCA)降维处理后得到的自由能可视化组合图。三张图采用不同可视化方式展示同一套二维降维后的自由能数据,所有子图统一以降维得到的第一主成分(PC1)为X轴,第二主成分(PC2)为Y轴,核心用途是分析目标分子体系不同构象的稳定性与能量分布特征。
标准解读流程:
第一步:交叉验证定位最稳定构象
需要结合三张图的特征交叉定位能量最低点:在等高线图中查找最中心的闭合等高线区域,在热图中查找颜色
最深的区域,在3D曲面图中查找谷底位置,三者重合的位置对应的构象就是体系的最稳定构象。
第二步:分析能量分布与构象状态
根据低能量区域的分布特征判断体系构象状态:
1.如果整个投影平面中只有一个连续的深色低能量区域,说明该体系仅存在单一稳定构象状态
2.如果投影平面中存在多个相互分离的深色低能量区域,说明体系存在多个可相互转换的稳定构象状态,不同构象之间存在可观测的能垒分隔。
第三步:验证结果可靠性
解读完成后需要核对左上角标注的累计贡献率:若数值<50%,说明当前降维结果无法很好代表体系真实结构变化,所得结论可能不可靠,需要调整PCA分析参数或改进降维方法重新计算。
6、自由能地貌图(FEL)状
图表形式:
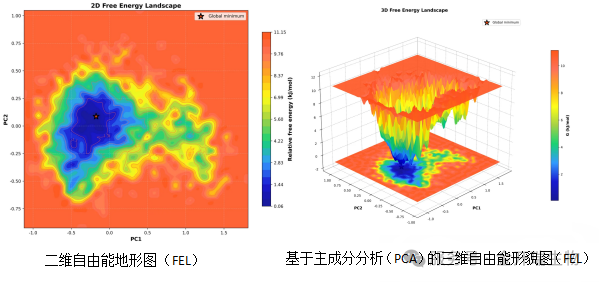
分析对象:基于主成分分析(PCA)的自由能地形图(FEL),包括二维等高线投影图与三维曲面图。
横坐标:第一主成分(PC1),反映模拟轨迹中最大的构象变化模式。
纵坐标:第二主成分(PC2),反映次大的构象变化模式。
颜色映射:从深蓝/紫色(低能量,稳定)到红/黄色(高能量,不稳定)。
标注信息:图中标有“Global minimum” (全局最小值),对应最低自由能区域。
含义:将模拟轨迹中所有构象投影到低维空间,计算每个区域的自由能,直观展示体系可能采用的稳定构象簇。
二维等高线图解读:
深蓝色区域(颜色条最低值约1.00)为全局最小值,对应最稳定构象。
等高线呈单一闭合椭圆,无其他分离的蓝色低谷→ 构象分布集中,无竞争性稳定态。
从深蓝向外颜色渐浅,能量梯度明显→ 稳定构象具有热力学优势,自发跳出盆地的概率低。
三维形貌图解读:
三维曲面中全局最小值处为一个明显凹陷的盆地,周围能量隆起(颜色转红/黄)。
盆地深度大、水平宽度窄→ 构象刚性较强,涨落幅度小。
无其他深度相近的盆地→ 体系在模拟时间内保持单一构象簇,未发生开闭运动或折叠/去折叠。
7、结合自由能分解(MM/PBSA残基分解)柱状图
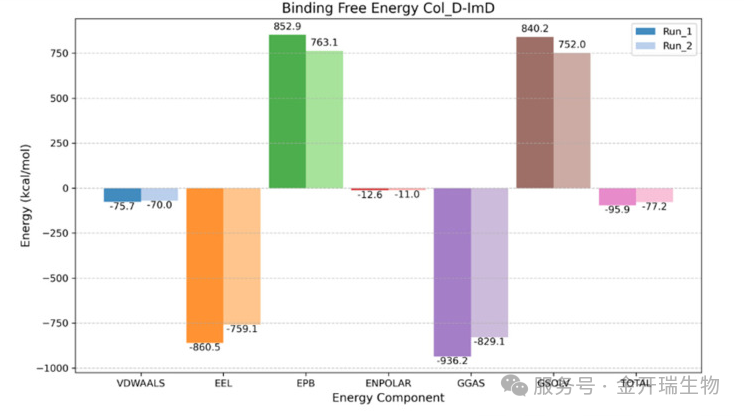
MM/PBSA 能量分解- 结合能柱状图
图表形式:
横坐标:能量组分,包括范德华能(VDWAALS)、静电相互作用能(EEL)、极性溶剂化能(EPB)、非极性溶剂化能(ENPOLAR)、气相总能量(GGAS)、溶剂化总能量(GSOLV)以及总结合自由能(TOTAL)。
纵坐标:能量值(单位:kcal/mol),正值表示不利贡献,负值表示有利贡献。
数据分组:两组独立模拟(Run_1 和 Run_2),每组用不同颜色柱状条并排显示。
含义:将总结合自由能分解到每个残基上,识别哪些氨基酸对结合起主要驱动作用。
如何看图?
该图展示了蛋白‑配体复合物结合自由能的总量及各能量项的分解。其中:
GGAS = VDWAALS + EEL,代表气相中分子间的相互作用(有利结合通常为负值)。
GSOLV = EPB + ENPOLAR,代表溶剂化效应(通常为正值,表示去溶剂化惩罚;但图中GSOLV为负值,说明溶剂化整体有利于结合,较为少见,需结合体系极性判断)。
TOTAL = GGAS + GSOLV,即总结合自由能,负值越大表示结合越强
该图表明两次独立模拟的总结合自由能分别为‑85.3和‑80.0 kcal/mol,结合主要依赖极强的静电相互作用(EEL约‑800 kcal/mol),范德华能起辅助作用,溶剂化效应整体仍促进结合;结果重复性良好,表明该复合物具有稳定且高亲和力的结合模式。
四、典型分析流程示例
以100 ns的蛋白‑配体复合物模拟为例,常规分析顺序及判断逻辑如下:
➤查看RMSD曲线:确认体系是否在合理时间内(如60 ns后)达到平台。若一直上升,需延长模拟时间或检查初始结构是否合理。
➤查看RMSF图:确认活性位点残基RMSF较低;若偏高,怀疑结合不稳定。
➤查看氢键分析:统计关键氢键的占据率,若低于30%,结合可能较弱。
➤计算MM/PBSA:获得总结合自由能及残基分解,识别热点残基,与RMSF
低值区域对比验证。
➤查看自由能地貌图:确认轨迹是否集中在低能区域,并提取代表性构象。
➤检查二级结构变化:确认关键功能区域未发生非预期结构转变。
五、模拟质量控制的常见考量
重复模拟:建议进行至少3次独立重复模拟(不同初始速度),以评估结果的统计方差。重复次数及分析深度可根据客户研究目标及期刊要求进行定制。
模拟时长:100 ns适用于多数柔性较小的体系;对于loop区丰富或构象变化大的体系,建议延长至250‑500 ns或更多。
力场选择:根据体系类型选择合适的力场(蛋白常用AMBER ff14SB、CHARMM36m;小分子用GAFF等)。
六、总结
分子动力学模拟提供的不仅是静态结构,更是一套描述分子动态行为的定量数据。正确解读RMSD、RMSF、Rg、氢键、自由能分解等图表,是判断模拟可靠性、提取生物学结论的基础。在实际应用中,应结合多个指标交叉验证,避免单一指标的误判。
金开瑞生物凭借专业的生物信息学分析平台和技术团队,可提供从分子对接、分子动力学模拟、结合自由能分析以及综合分析及课题整体打包服务,无论您是只需分子对接完成快速筛选,还是需要完整的“对接+MD+自由能”深度解析,我们都能灵活匹配您的需求,助力科研高效推进。
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










