最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
我们每天都在吃苹果,但可能从未真正理解它。
苹果是全球消费最广泛的水果之一。我们都知道它富含多酚、果胶和抗氧化剂,常被推荐为健康饮食的一部分。但一个根本性的科学问题长期被忽视:
我们吃下去的苹果,除了提供维生素和膳食纤维,是否还在以一种我们完全不知道的方式,与我们的神经系统对话?
过去十年,科学家发现植物会释放一种纳米级的脂质囊泡——植物来源细胞外囊泡(PDEVs)。这些囊泡包裹着蛋白质、RNA、代谢物和抗氧化分子,能够抵抗消化道的降解,被哺乳动物细胞摄取,并在跨物种层面发挥生物调控作用。
换句话说:我们吃水果,可能不只是吃营养,还在「接收」植物发出的生物信息。
那么,苹果来源的细胞外囊泡(以下简称ADEVs),是否能够通过最近大热的「肠-脑轴」影响我们的神经免疫系统?
2026年4月21日,意大利费拉拉大学的研究团队在《Phytomedicine》(IF=8.3)上发表了题为“Apple Derived Extracellular Vesicles as Positive Modulators of Glial Inflammation and Gut–Brain Axis Signaling”的研究论文,针对这一问题给出了明确答案。该文章发现苹果来源的细胞外囊泡(ADEVs)能够通过重编程肠道微生物代谢(促进糖酵解转变)、增强肠道屏障完整性并特异性调节胶质细胞炎症反应,从而作为肠-脑轴的正向调节剂发挥作用。
一、研究思路
从物理结构到动物体内,层层递进。
这项研究的设计非常严谨,采用了从结构到功能、从体外到体内、从短期到长期的递进式策略:
➤先看ADEVs长什么样、含有哪些成分(NTA、电镜、拉曼光谱)
➤看它是否安全——会不会破坏血脑屏障?
➤看它作用谁——是作用于神经元,还是胶质细胞?
➤看它能否抗炎——在炎症状态下能否抑制胶质细胞释放炎症因子?
➤看它能否当药物载体——能不能把神经药物送进目标细胞?
➤看它如何影响肠道菌群——短期和长期分别发生了什么变化?
➤最后在动物身上做探索性验证——IBD犬的血浆神经化学指标是否改变?
二、核心结论
1、ADEVs是装载多种活性分子的天然纳米囊泡
通过超速离心法获得的苹果来源细胞外囊泡(ADEVs),使用纳米颗粒追踪分析(NTA)进行物理表征(图1A),结果显示,ADEVs直径主要分布在184 nm左右,在105-200 nm区间高度富集,与已知植物来源细胞外囊泡(PDEVs)的典型尺寸一致。
扫描电子显微镜(SEM)进一步证实,ADEVs呈完整、球形、膜结合结构,直径约180 nm,表面光滑连续,无聚集或破裂,表明分离后结构完整性良好(图1B)。
此外,研究检测到植物EVs的标志性蛋白组分:Exo70、TET8和TET3,从分子层面确认了ADEVs的囊泡身份(图1C)。拉曼光谱分析(Fig. 1D及inset)直接证明,ADEVs内部携带了多种功能性成分:如脂质、糖类、RNA、苹果酸、槲皮素和类胡萝卜素等多种活性分子,是一个功能集成的天然纳米植物复合体,而非空壳载体。
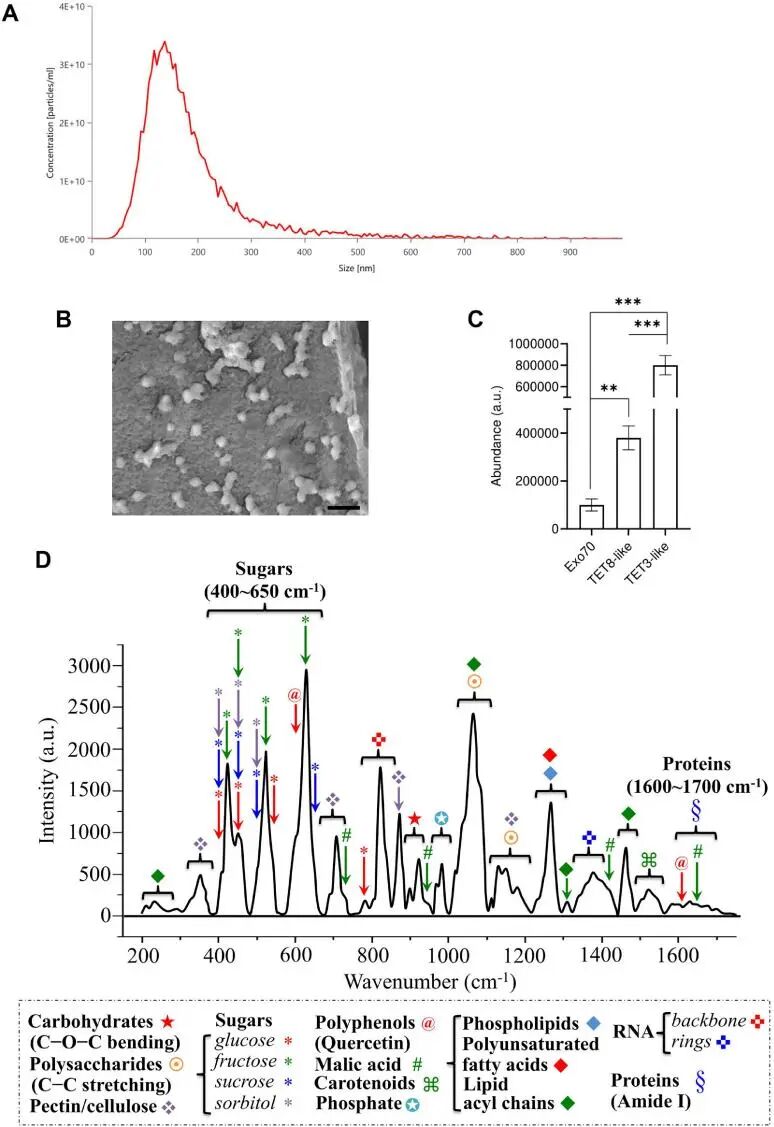
(A) ADEVs的纳米颗粒追踪分析(NTA),显示颗粒浓度(颗粒/毫升)和粒径分布。
(B) ADEVs的代表性扫描电子显微镜(SEM)图像。比例尺:1 µm。
(C) ADEVs的蛋白谱分析显示囊泡相关蛋白Exo70、TET8和TET3富集,证实了所分离结构的囊泡性质。
(D) ADEVs的拉曼光谱。插图中标出了特定分子的指纹信号,包括脂质、碳水化合物、糖分子、RNA、蛋白质和抗氧化代谢物。
2、ADEVs不破坏血脑屏障,反而增强其稳定性
这表明ADEVs不仅没有破坏BBB,反而在48小时后显著增强了屏障的完整性。而且这种增强作用并非通过上调紧密连接的转录水平实现,可能涉及更复杂的翻译后或功能性调节机制。这些发现表明ADEVs与内皮屏障系统的生物相容性,支持其在植物医学导向策略和屏障靶向干预中的潜在应用。
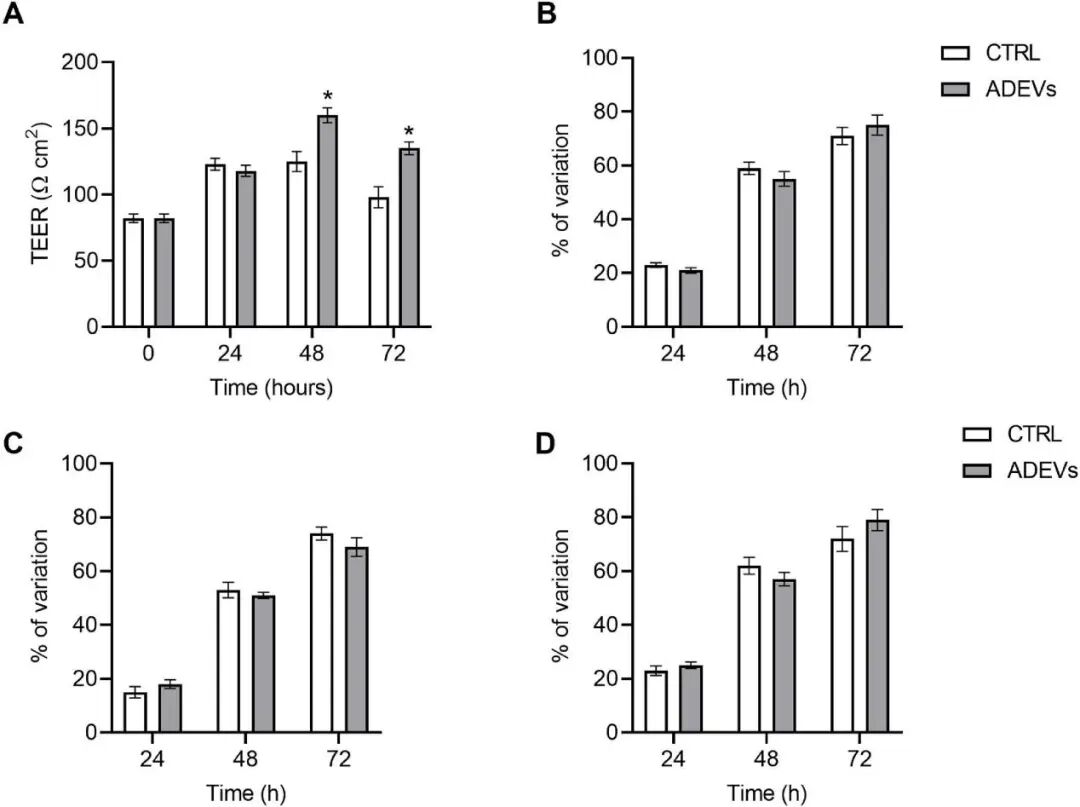
细胞屏障完整性。(A)人脑微血管内皮细胞(hBMECs)单层跨内皮电阻(TEER):未处理组(白色)与ADEV处理组(灰色)在24、48和72小时后的比较。星号表示与对照组相比差异显著(p < 0.05,n = 3个生物学重复)。(B-D)未处理组与ADEV处理组hBMECs中(B)OCLN、(C)CLDN1和(D)ZO-1的mRNA表达水平(以GAPDH为内参,归一化为对照组百分比)。实验组间未观察到显著差异,数据以均值 ± 标准差表示(n = 3)。
3、ADEVs在胶质瘤细胞系中表现出选择性摄取与抗炎效应
这是整篇研究最具区分度的发现。研究团队选用了两种人源神经细胞系:T98G(胶质细胞样,高内吞活性)和SH-SY5Y(神经元样)。
在摄取效率方面(Fig. 3A–B),T98G细胞中出现大量点状、明亮的红色荧光,呈核周聚集分布,符合典型的内吞模式;而SH-SY5Y细胞仅呈现微弱、弥散的荧光信号。定量分析显示,T98G对ADEVs的摄取量显著高于SH-SY5Y(p < 0.05),表明ADEVs与胶质瘤细胞系具有更强的相互作用。
然而,摄取不等于功能激活。在钙信号响应方面(Fig. 3C–J),T98G细胞中ADEVs诱发快速、瞬时的钙信号,峰值高但迅速恢复基线;而SH-SY5Y细胞中,ADEVs处理后钙信号完全没有偏离基线。定量分析进一步证实,T98G中ADEVs诱导的钙信号AUC和峰值均显著高于基线,而SH-SY5Y中两者均无统计学差异。在功能层面,ADEVs在静息状态下不诱导T98G细胞产生炎症因子,但在TNF-α激活的炎症状态下显著抑制IL-6、IL-8和IL-1β的分泌(Fig. 3K)。这种“病理选择性抗炎”效应,提示ADEVs可能作为间接的、肠-胶质轴相关的神经免疫调节候选物。
综合以上体外细胞模型的结果可以看出,ADEVs的作用具有明显的细胞类型选择性:它们更倾向于与T98G胶质瘤细胞系相互作用并调节其炎症反应,而在SH-SY5Y神经元样细胞中几乎不产生功能性响应。 这为理解ADEVs可能通过影响胶质细胞而非直接作用于神经元来间接调节神经功能,提供了重要的体外实验依据。
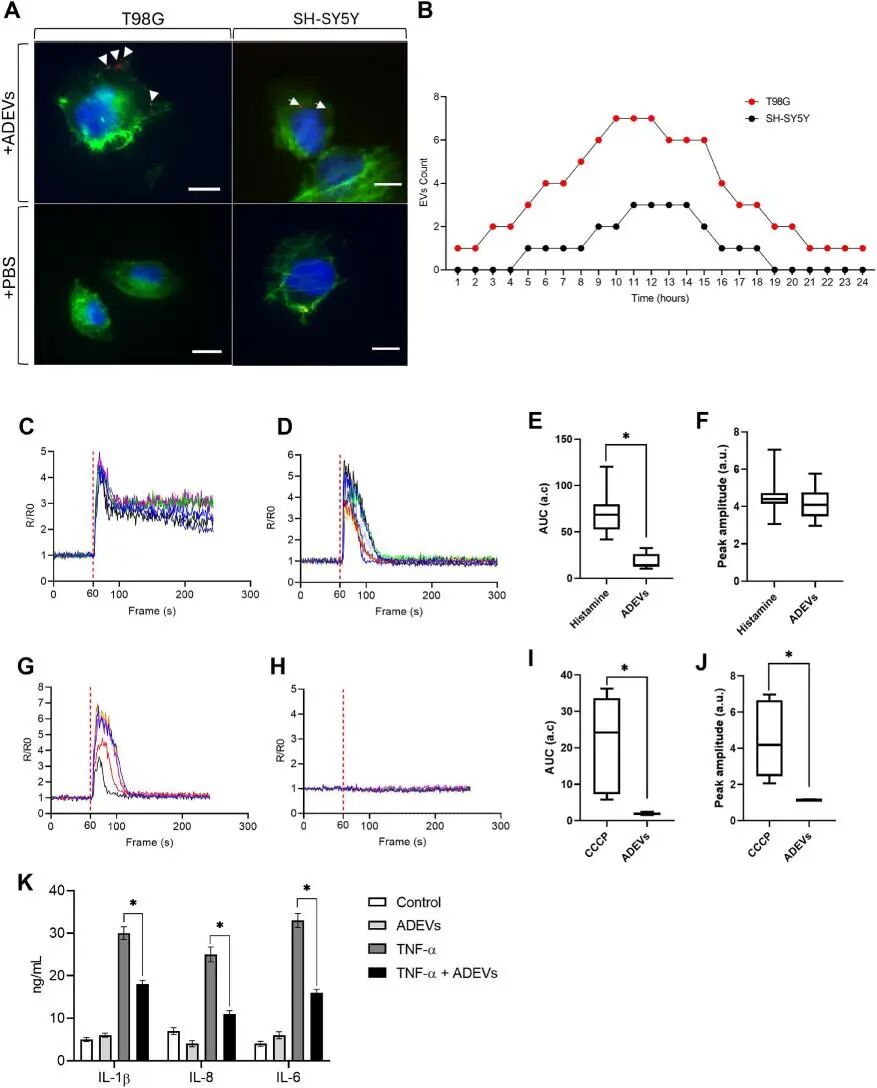
图3. ADEVs在中枢神经系统中的细胞类型特异性
(A) T98G胶质细胞和SH-SY5Y神经元摄取红色荧光标记ADEVs的代表性图像。白色箭头指示ADEVs。比例尺:10 µm。
(B) ADEVs摄取量定量分析显示,T98G细胞的摄取量显著高于SH-SY5Y细胞(p < 0.05)。
(C-D) T98G细胞中,组胺(阳性对照)和ADEVs均诱发钙信号。
(G-H) SH-SY5Y细胞中,CCCP(阳性对照)诱发显著钙信号,但ADEVs无响应。
(E-I) 钙信号总量(AUC)定量分析。
(F-J) 钙信号峰值幅度定量分析。
(K) T98G细胞炎症因子分泌:ADEVs本身不诱导炎症因子;在TNF-α刺激下,ADEVs显著抑制IL-6、IL-8和IL-1β的分泌(p < 0.05)。
4、ADEVs重塑肠道菌群代谢——促糖酵解、抑蛋白发酵
这是整篇研究机制层面最核心的发现。研究团队通过短期(48小时)和长期(3周)结肠模拟系统,评估ADEVs对肠道菌群代谢的影响。
短期结果显示,中等浓度ADEVs使pH维持在生理范围(5.99-6.62),显著升高乙酸、丙酸和丁酸等短链脂肪酸,同时降低支链脂肪酸和氨(蛋白发酵的标志物)。高浓度则导致过度酸化和代谢紊乱。
长期结果显示,ADEVs在远端结肠持续升高乙酸和丙酸,同时降低氨和支链脂肪酸,且不改变菌群总体数量。丁酸盐反而下降,提示ADEVs可能优先驱动丙酸生成通路。
综合来看,ADEVs在适宜剂量下能够将菌群代谢从“蛋白发酵”转向“糖类发酵”,这是一个被普遍认为更有利于肠道和全身健康的代谢转变。
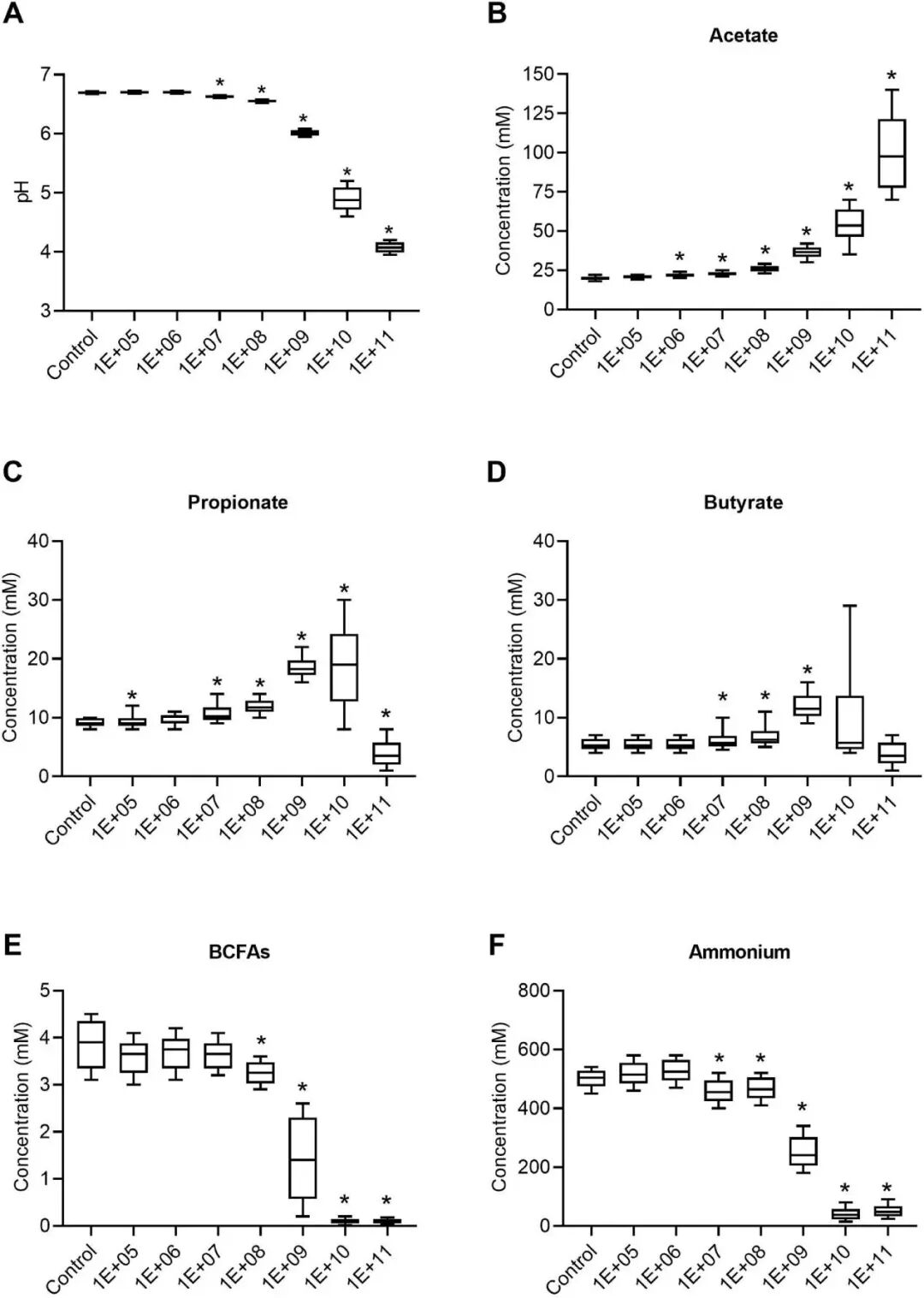
图4. 苹果来源细胞外囊泡(ADEVs)对结肠微生物发酵的剂量依赖性调节作用。
(A)与ADEVs共同孵育48小时后,腔内pH值的变化。
(B-D)微生物碳水化合物分解代谢的主要产物——短链脂肪酸(SCFAs)的生成量:(B)乙酸、(C)丙酸、(D)丁酸。
(E、F)蛋白分解发酵产物:(E)支链脂肪酸(BCFAs)及(F)铵离子的生成量。数据表示为整个处理期间的平均值±标准差(n=8)。星号表示与对照组相比具有统计学显著性差异(p<0.05)。
5、ADEVs在体内与肠-脑信号分子变化相关
研究团队在67只诊断为炎症性肠病(IBD)的犬中进行了一项探索性观察研究。结果显示,约35%的犬在口服ADEVs 8周后,血浆5-羟色胺(5-HT)水平较基线显著升高。5-HT是一种主要由肠道嗜铬细胞产生、参与肠-脑通讯的关键神经递质。需要强调的是,这是一项非随机、无安慰剂对照的观察性研究,5-HT主要来源于肠道而非中枢,因此不能证明因果关系。但这一结果提示,ADEVs可能通过调节肠道环境间接影响肠-脑神经化学信号,为后续研究提供了重要的假设生成依据。
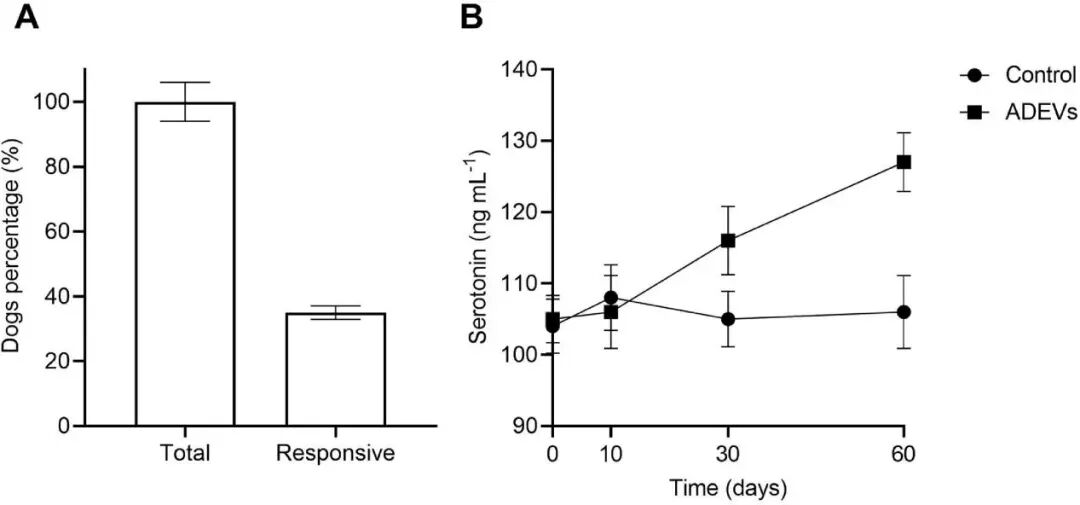
图5. ADEVs介导的脑-肠轴中的血清素转运
(A) 临床诊断为炎症性肠病且对ADEV给药有反应的犬只。
(B) 有反应犬只在ADEV给药后两个月内的血浆血清素水平。n = 3个生物学重复,统计分析采用单因素方差分析 followed by Tukey多重比较检验。技术重复在分析前已取平均值,*p < 0.05。
综合来看,这项研究表明,苹果来源的细胞外囊泡(ADEVs)并非简单的营养载体,而是一个功能集成的天然纳米植物复合体。它能够在人胶质瘤细胞系(如T98G)中表现出优先摄取与功能响应,在炎症状态下发挥抗炎作用,同时保护血脑屏障、重塑肠道菌群代谢,并最终与肠-脑神经化学信号的变化相关联。虽然从实验室发现到真正应用于人类健康还有很长的路要走,但这项研究为我们理解“吃苹果”这件事打开了一扇全新的大门——我们摄入的每一口食物,可能都在以一种我们尚未完全认知的方式,与我们的身体进行着跨物种的生物对话。
文献来源:Maria Pia Cavaleri, Luna Ardondi, Ilaria Vitali, et al. Apple Derived Extracellular Vesicles as Positive Modulators of Glial Inflammation and Gut–Brain Axis Signaling, Phytomedicine, 2026, 158232.
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










