外泌体研究方案中的样本来源与实验模型如何设计?
一、样本与模型在外泌体研究中的核心地位
外泌体是细胞主动分泌的直径30–150 nm的细胞外囊泡,携带蛋白质、miRNA、mRNA、脂质、代谢物等生物活性物质,介导细胞间通讯、组织稳态调控、疾病发生发展等关键生物学过程,已成为生命科学、医学、药学领域的研究热点。
外泌体研究方案的科学性、可靠性与可重复性,高度依赖样本来源的合理性、标准化与质控,以及实验模型的适配性、严谨性与层次化。
样本来源决定外泌体的“来源属性”:不同细胞、组织、体液来源的外泌体,其含量、纯度、cargo组成、生物学功能差异极大;样本采集、处理、储存、预处理不规范,会直接导致外泌体破碎、污染(凋亡小体、微囊泡、脂蛋白、细胞碎片)、蛋白/核酸降解,使实验结果失真。
实验模型是验证外泌体功能与机制的“核心载体”:体外模型快速、可控、高通量,用于初步筛选与表型验证;体内模型更贴近生理/病理微环境,用于功能确证、机制深化与转化价值评估。脱离合理样本与适配模型的外泌体研究,难以获得可信结论,更无法实现临床转化。
因此,外泌体研究方案中样本来源与实验模型设计,必须遵循“标准化采集、分级质控、分层建模、对照完备、伦理合规”原则,兼顾研究目的、技术条件、统计效力与转化导向。本文从样本来源分类、设计原则、采集与预处理规范、质控要点,实验模型分层设计(体外/体内/类器官)、模型选择逻辑、对照设置、统计与伦理要求等方面,系统阐述外泌体研究方案中样本与模型的完整设计方案,为科研人员提供可直接落地的执行框架。
二、外泌体研究方案中样本来源的分类与设计原则
1、样本来源核心分类
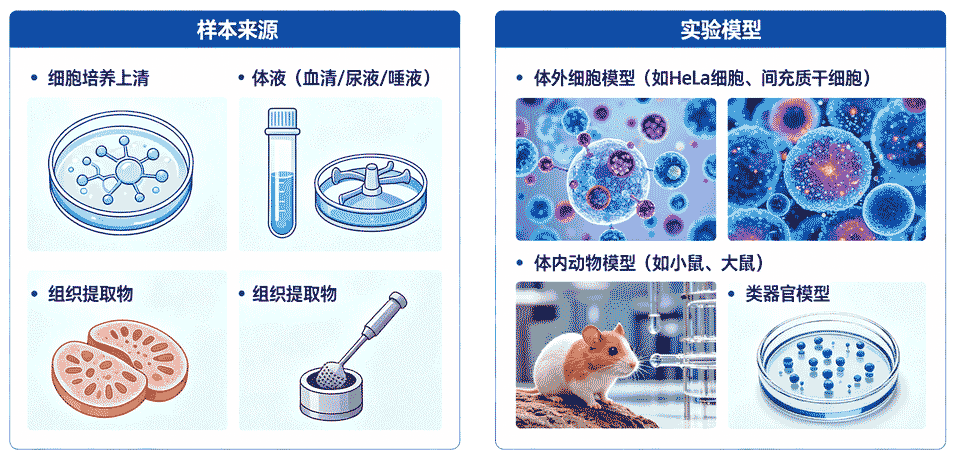
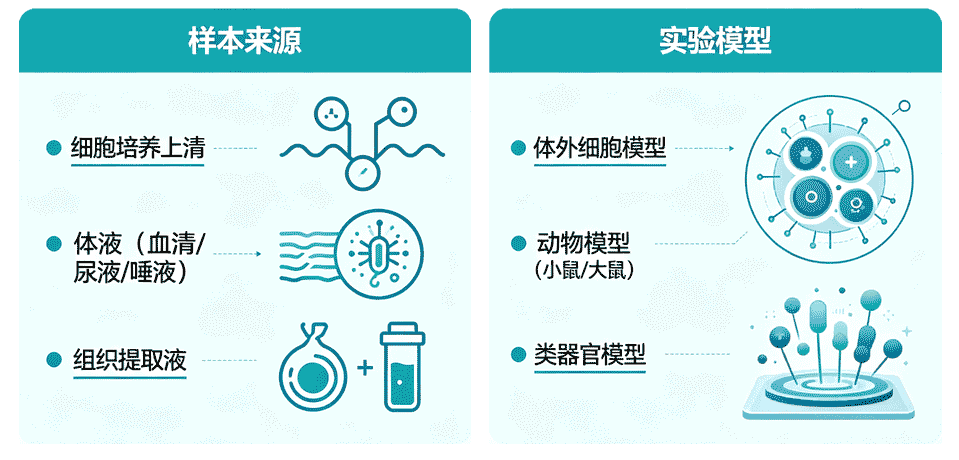
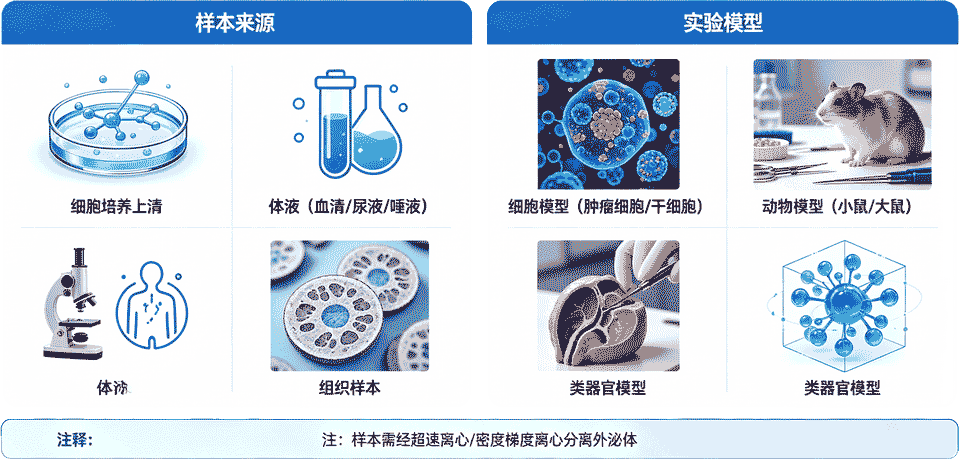
外泌体研究样本主要分为体外细胞培养上清样本、临床体液样本、动物组织/体液样本三大类,每类样本适用于不同研究阶段与科学问题。
体外细胞培养上清样本:最基础、最常用,适用于外泌体分离纯化方法优化、cargo筛选、体外功能验证、机制初探。优势:来源均一、可控性强、无个体差异、易获得大量外泌体、成本较低;局限:无法模拟体内复杂微环境。
临床体液样本:临床转化(液体活检、标志物开发)的核心样本,包括血清、血浆、尿液、脑脊液、胸水、腹水、唾液等。优势:无创/微创、可动态监测、直接关联临床表型;局限:个体差异大、污染严重、标准化难度高。
动物组织/体液样本:连接体外细胞与临床样本的桥梁,适用于体内外泌体功能验证、机制确证、药物递送评价。优势:可人为控制疾病模型、遗传背景;局限:与人类疾病存在差异,成本较高。
2、样本来源设计五大核心原则
适配研究目的原则:基础机制→细胞+动物;标志物→临床体液;治疗研究→干细胞外泌体+动物模型。
标准化与一致性原则:统一采集时间、离心参数、储存温度,避免混合不同条件样本。
质控优先原则:排除溶血、脂血、微生物污染、细胞裂解、过度冻融样本。
样本量充足原则:满足分离、鉴定、多组学、功能实验与重复实验需求。
伦理合规原则:临床样本需知情同意与伦理审批;动物实验遵循3R原则。
 三、外泌体研究方案中各类样本采集、预处理与质控规范
三、外泌体研究方案中各类样本采集、预处理与质控规范
1、细胞培养上清样本:采集与预处理标准化流程
细胞培养:选用低代次、无支原体污染细胞,汇合度70–80%时更换无外泌体胎牛血清培养基。
培养24–48h收集上清,避免细胞凋亡。
预处理:300g×10min → 2000g×10–20min → 10000g×30min → 0.22μm滤膜过滤。
质控:支原体阴性、细胞存活率>90%。
2、临床体液样本:采集、预处理与质控
优先使用血浆,血清因血小板激活会释放大量囊泡干扰实验。EDTA抗凝管采集,2h内完成预处理。
血浆/血清:4℃ 1500g×15min → 3000g×15min → 12000g×30min → 0.22μm过滤。
尿液:清洁中段尿,晨尿更佳,样本量≥50mL。
脑脊液/胸水/腹水:无菌采集,避免血性污染。
质控红线:溶血、脂血样本直接废弃;冻融次数≤3次;-80℃保存,避免-20℃储存。
3、动物样本:采集与预处理规范
动物体液采集同人类血浆流程;组织外泌体需新鲜组织剪碎、匀浆、过滤、梯度离心提取。质控要求:无死亡、感染、溶血,统一周龄、性别、饲养环境。
四、外泌体研究方案中实验模型的分层设计:体外模型
1、体外模型核心作用
快速验证外泌体被受体细胞摄取、明确表型调控、筛选关键cargo与通路、优化给药浓度与时间,具有高通量、低成本、排除体内干扰的优势。
2、常用体外模型类型
受体细胞摄取模型:荧光标记外泌体,共聚焦/流式检测摄取,所有功能研究第一步。
肿瘤相关模型:增殖、迁移、侵袭、凋亡、周期检测。
干细胞/修复模型:氧化应激、缺氧、炎症损伤模型,评价修复与再生能力。
免疫细胞模型:巨噬细胞极化、T细胞活化、细胞因子表达。
通路干预模型:抑制剂、siRNA、过表达载体,验证分子机制。
3、体外模型设计关键要求
细胞选择具有生理相关性。
设置浓度梯度与时间梯度。
必须设置空白对照、PBS对照、热灭活外泌体对照、无关外泌体对照。
五、外泌体研究方案中实验模型的分层设计:体内模型
1、体内模型核心作用
体外结果必须在体内验证,用于观察组织分布、靶向性、治疗效果、生存分析、组织病理改变与机制确证。
2、常用体内模型类型
肿瘤动物模型:皮下移植瘤、转移瘤模型,观察生长与转移。
组织损伤/炎症模型:心、脑、肝、肾、皮肤损伤,评价修复与抗炎效果。
活体示踪模型:荧光标记外泌体,小动物成像观察体内分布。
转基因/基因敲除模型:研究外泌体分泌调控基因。
3、体内模型设计关键要求
动物选择:裸鼠、C57BL/6、SD大鼠等,统一周龄、性别、体重。
分组:正常对照、模型对照、PBS对照、低中高剂量组、阳性药物组。
每组动物数≥6只,保证统计效力。
给药方式:尾静脉、局部、腹腔、瘤内注射,匹配临床场景。
六、外泌体研究方案中实验模型的创新:类器官模型
类器官是三维培养体系,介于体外细胞与体内动物之间,模拟真实组织结构与微环境,保留细胞异质性与极性,结果更贴近人体,适用于肿瘤发生、药物筛选、旁分泌调控、精准医疗研究,是外泌体研究的高级模型。
七、外泌体研究方案中样本与模型的对照体系设计
无对照实验不被学术认可,外泌体研究必须设置多层次对照:
样本对照:正常vs疾病,处理vs未处理。
分离对照:预处理上清vs外泌体组分,去除外泌体上清。
功能实验对照:空白、PBS、热灭活外泌体、无关外泌体、抑制剂、回救实验(rescue)。
八、外泌体研究方案中样本量与统计学设计
体外实验:每组3复孔,独立重复≥3次。
临床样本:标志物研究每组≥30例,验证≥100例。
动物实验:每组≥6只。
统计方法:t检验、方差分析、卡方检验、生存分析、相关性分析,P<0.05为显著差异。
九、伦理规范:外泌体研究方案的必备前提
临床样本:签署知情同意,伦理委员会批准,匿名化处理。
动物实验:遵循3R原则(替代、减少、优化),规范操作,减少痛苦。
十、外泌体研究方案中样本与模型设计的核心逻辑
样本来源决定研究基础,实验模型决定研究高度,质控与对照决定研究可信度。
外泌体研究方案中样本与模型设计必须遵循:
明确科学问题→选择匹配样本(细胞/体液/动物);
严格标准化采集与预处理→排除污染与降解;
构建“体外细胞→类器官→体内动物”三级模型;
设置完整对照体系→保证结果可重复、可验证;
满足伦理与统计要求→符合学术规范与转化需求。
高质量的样本与模型设计,是外泌体研究从“基础探索”走向“临床转化”的关键保障,也是发表高水平论文、获得科研立项的核心支撑。
最新动态
-
05.27
DAP‑Seq实验如何设置对照、保证重复性与数据可靠性?
-
05.27
DAP‑Seq与ChIP‑Seq、CUT&Tag、ATAC‑Seq的关键区别与适用场景?
-
05.26
定制ELISA试剂盒的灵敏度、特异性、重复性等关键性能如何保证?
-
05.11
怎么通过ChIP-seq结果分析转录因子的结合基序与结合位点分布?
-
04.27
双分子荧光互补(BiFC)与FRET的核心区别是什么?
-
04.27
外泌体研究方案中的样本来源与实验模型如何设计?
-
04.24
细胞迁移及侵袭实验攻略
-
04.24
等温量热滴定曲线出现正负峰的原因是什么?
-
04.23
EMSA实验中,细胞核蛋白提取质量对结果影响极大,如何保证蛋白的完整性与结合活性?
-
04.23
免疫荧光检测中常见的非特异性荧光有哪些原因?如何减少或避免?










