噬菌体展示肽库构建与筛选研究
噬菌体展示肽库技术是将随机多肽编码基因与噬菌体外壳蛋白基因融合表达,使多肽展示在噬菌体表面,再通过亲和淘洗富集特异性序列的高通量筛选技术,核心是基因型与表位直接偶联,快速筛选高亲和力配体。
一、技术原理
以丝状噬菌体(M13、fd、f1)为载体,将外源短肽基因插入pⅢ(次要外壳蛋白,N端展示,1-5拷贝,适合高亲和力筛选)或pⅧ(主要外壳蛋白,N端展示,约2700拷贝,适合高丰度展示)基因的合适位点。
每个噬菌体展示一种独特多肽
编码基因在噬菌体DNA内,实现 “表型 - 基因型” 物理偶联
通过亲和筛选富集结合噬菌体,再感染大肠杆菌扩增,多轮后获得高特异性、高亲和力序列
二、噬菌体展示肽库的类型
随机线性肽库:编码连续6–20 aa随机序列,最常用
构象约束肽库(环肽库):肽段两端含Cys,形成二硫键环化,构象更稳定、亲和力更高
靶向定位肽库:针对特定组织/肿瘤/血管的定向库
抗体库(scFv/Fab):展示抗体可变区,用于抗体筛选
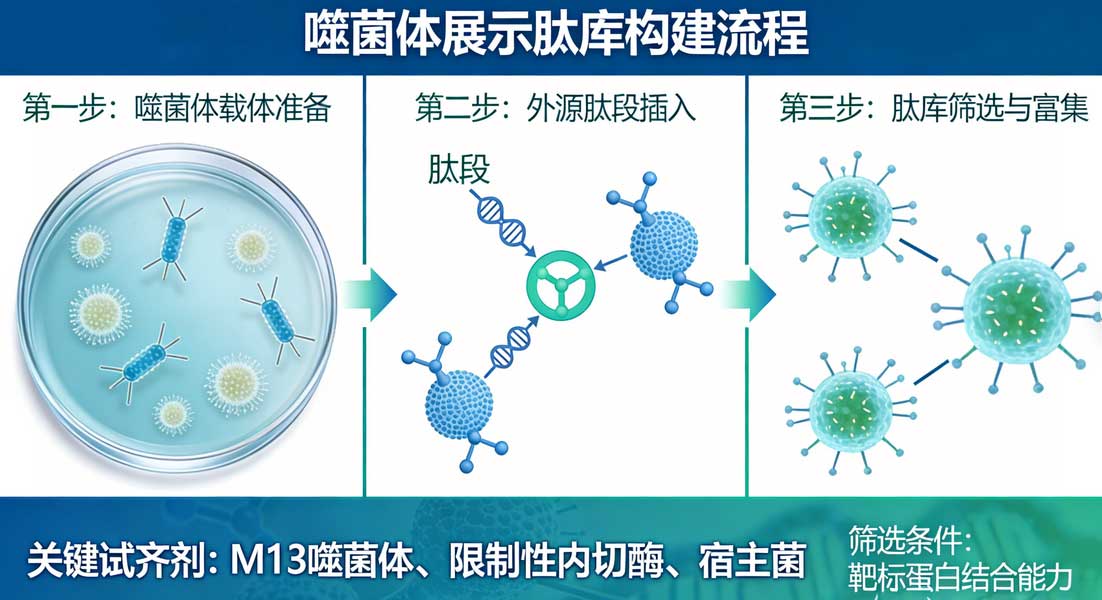
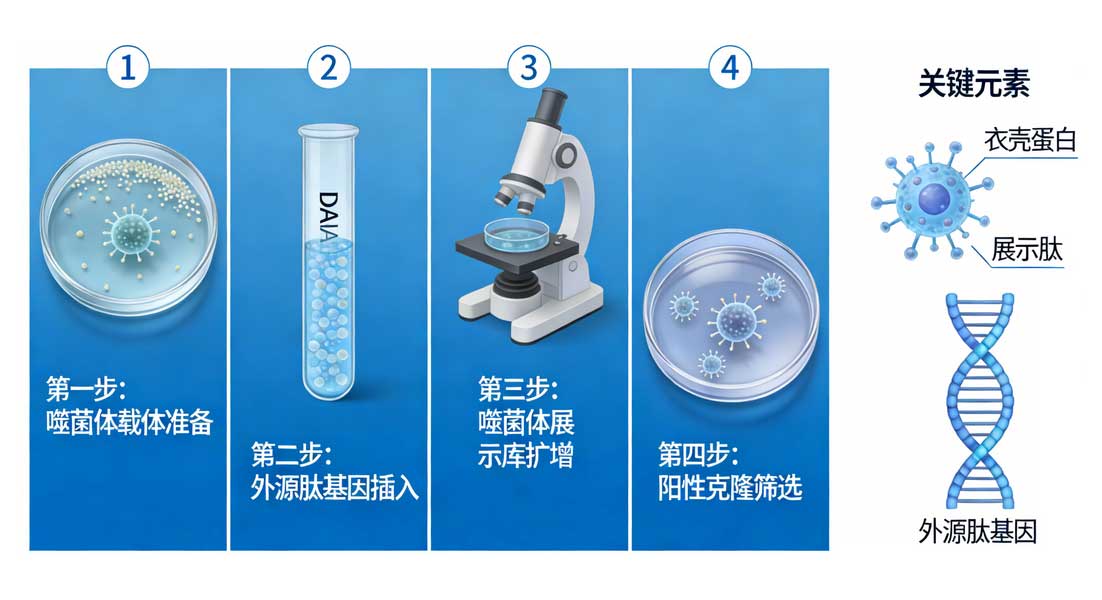
三、肽库构建流程(以M13噬菌体为例)
1. 载体选择
常用噬菌粒载体(phagemid):含pⅢ/pⅧ、复制子、抗性、lac启动子,需辅助噬菌体(M13KO7)提供包装蛋白。
2. 随机肽基因片段制备
全基因合成:合成带酶切位点的随机寡核苷酸片段(NNK密码子,编码20种氨基酸)
PCR扩增:扩增随机序列
3. 载体与外源片段连接
双酶切(如SfiI、NotI、XhoI)
T4 DNA连接酶连接,构建重组噬菌粒
4. 转化(电转化效率最高)
转入大肠杆菌感受态细胞(TG1、XL1-Blue)
涂布抗性平板,37℃培养
库容量:一般≥1×10⁹,覆盖更多多样性
5. 文库拯救与扩增
加入辅助噬菌体超感染
培养液上清含重组噬菌体颗粒
沉淀、纯化、滴定,得到原始肽库
四、生物淘洗(筛选)流程
核心:结合→洗涤→洗脱→扩增→重复
1. 靶标固定
包被抗原、受体、抗体、细胞于酶标板/磁珠/芯片
封闭(BSA/脱脂奶)减少非特异吸附
2. 结合与洗涤
加入噬菌体库,室温/4℃孵育
强洗涤(Tween-PBS):去未结合与弱结合噬菌体
3. 特异性洗脱
酸性洗脱(0.1–0.2 M Gly-HCl, pH 2.2)
碱性洗脱
竞争洗脱(游离靶标)
立即中和至中性
4. 感染扩增
洗脱物感染大肠杆菌
辅助噬菌体拯救,制备下一轮库
5. 多轮淘洗(3–4轮)
每轮提高洗涤强度、降低靶标浓度
富集倍数逐步上升(10²–10⁶倍)
五、阳性克隆鉴定
单克隆噬菌体制备:挑单菌落,培养、拯救
ELISA/结合实验:测与靶标结合活性
DNA测序:确定插入肽序列
亲和常数测定(BIAcore)
特异性/竞争性验证
六、关键技术要点
库容量:≥1×10⁹,覆盖足够多样性
随机化质量:NNK减少终止密码子、均衡氨基酸
洗涤强度:控制非特异结合与阳性丢失
轮次:3–4轮为宜,过多易丢失多样性
阴性选择:用载体/无关蛋白预吸附去除非特异噬菌体
七、主要应用领域
抗原表位作图(B细胞/线性/构象表位)
肿瘤靶向肽(靶向肿瘤血管/标志物)
抗菌/抗病毒肽(受体结合阻断)
诊断/药物载体
酶抑制剂、受体激动剂/拮抗剂
抗体库筛选(全人源抗体)
八、优势与局限
优势
库容量大(10⁹–10¹²),筛选极高效
直接获得基因,便于重组表达
体外筛选,条件可控
可筛选细胞、活体、组织
局限
肽长度有限(一般≤40aa)
大肠杆菌表达限制(无翻译后修饰)
高亲和力克隆有时富集效率低
九、研究趋势
天然肽库/免疫肽库
体内噬菌体展示(活体筛选)
组合化学+噬菌体展示
高通量测序(NGS)替代单克隆测序,深度分析库多样性
多价展示、纳米抗体库、双特异肽
噬菌体展示肽库是体外定向分子进化的核心技术,通过基因融合+亲和淘洗,快速获得靶标特异性多肽/抗体,广泛用于生物医药、诊断、靶向治疗、基础生物学。构建关键是高库容量、高质量随机化;筛选关键是严格洗涤、多轮富集、严谨鉴定。
最新动态
-
05.11
怎么通过ChIP-seq结果分析转录因子的结合基序与结合位点分布?
-
04.27
双分子荧光互补(BiFC)与FRET的核心区别是什么?
-
04.27
外泌体研究方案中的样本来源与实验模型如何设计?
-
04.24
细胞迁移及侵袭实验攻略
-
04.24
等温量热滴定曲线出现正负峰的原因是什么?
-
04.23
EMSA实验中,细胞核蛋白提取质量对结果影响极大,如何保证蛋白的完整性与结合活性?
-
04.23
免疫荧光检测中常见的非特异性荧光有哪些原因?如何减少或避免?
-
04.16
大豆原生质体的亚细胞定位方法
-
04.15
ChIP-seq组蛋白特异性染色质免疫沉淀转录因子结合位点
-
04.10
蛋白质相互作用及亚细胞定位原理与技术










