CUT&TAG基于Tn5转座酶的高效组蛋白修饰分析方法
在表观遗传学研究的宏大版图中,解析组蛋白修饰的分布图谱是理解基因表达调控、细胞命运决定及疾病发生机制的关键。长期以来,染色质免疫共沉淀测序(ChIP-seq)一直是该领域的“金标准”。然而,ChIP-seq固有的局限性——如需要大量起始细胞量、繁琐的交联与超声破碎步骤、高背景噪音以及昂贵的测序成本——极大地限制了其在稀有样本(如早期胚胎、循环肿瘤细胞、特定神经元亚群)及临床微量样本中的应用。
2019年,由美国弗雷德·哈钦森癌症研究中心的Steven Henikoff团队开发的CUT&Tag(Cleavage Under Targets and Tagmentation)技术横空出世,迅速引发了表观遗传学方法学的革命。作为一种基于抗体引导的Tn5转座酶原位切割与标记技术,CUT&Tag以其极高的信噪比、极低的输入量要求(低至单个细胞)以及简便的操作流程,正在逐步取代传统ChIP-seq,成为组蛋白修饰研究的首选工具。本文将深入剖析CUT&Tag的技术原理、相较于ChIP-seq的显著优势、在组蛋白修饰研究中的具体应用及其在2026年的最新进展。
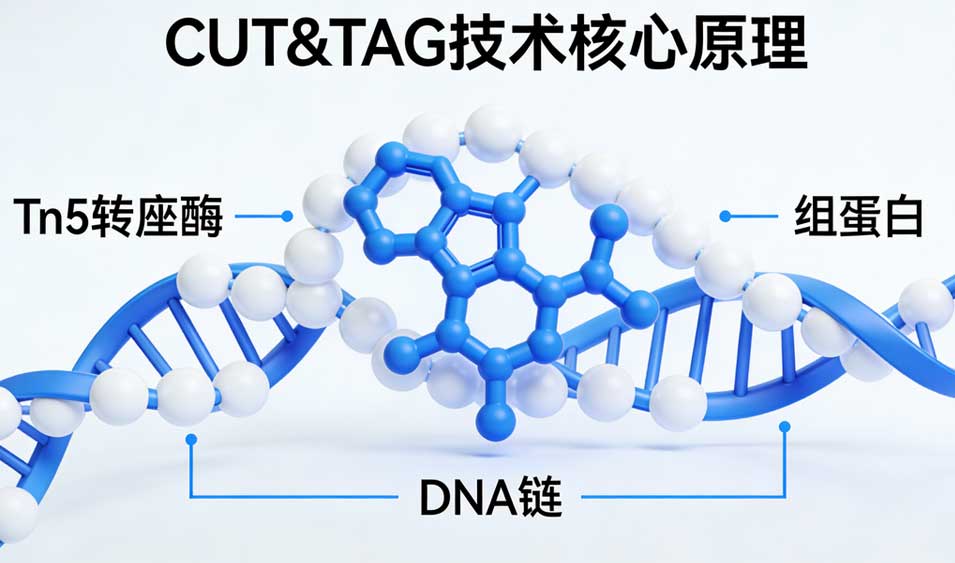
一、技术原理:从“富集”到“原位标记”的范式转变
CUT&Tag的核心设计理念是将抗体的特异性识别与Tn5转座酶的活性巧妙结合,实现了在完整细胞核内对目标蛋白结合位点的原位标记。其工作流程主要包含以下几个关键步骤:
细胞固定与透化:与ChIP-seq不同,CUT&Tag通常不需要甲醛交联(或仅需轻微交联),而是利用洋地黄皂苷(Digitonin)温和地透化细胞膜,保留细胞核结构的完整性,同时允许抗体进入。这一步骤最大限度地减少了非特异性背景。
一抗与二抗孵育:首先加入针对目标组蛋白修饰(如H3K4me3, H3K27ac等)的特异性一抗,随后加入偶联了蛋白A/G的二抗。这一双重抗体系统确保了后续酶复合物的高特异性定位。
Tn5转座酶复合物的组装:这是技术的灵魂所在。预装载了测序接头的超活性Tn5转座酶(Protein A-Tn5 fusion protein)被引入体系。Protein A结构域会特异性地结合到二抗上,从而将携带接头的Tn5转座酶精准地招募到目标组蛋白修饰所在的染色质区域附近。
原位切割与标签化(Tagmentation):加入镁离子激活Tn5转座酶。被招募到目标位点的Tn5会立即在抗体结合位点附近的DNA双链上进行切割,并同时将测序接头插入到切口两端。由于只有结合了抗体的区域才会招募Tn5,因此只有这些区域的DNA片段会被加上测序接头。
文库构建与测序:释放DNA片段,通过简单的PCR扩增即可构建测序文库。由于背景DNA未被加上接头,它们无法被有效扩增,从而实现了极高的信噪比。
这一过程将传统的“交联-破碎-免疫沉淀-纯化-建库”简化为“透化-抗体结合-原位标记-释放”,不仅大幅缩短了实验周期(从数天缩短至一天内),更从根本上降低了背景噪音。
二、核心优势:为何CUT&Tag能颠覆组蛋白修饰研究?
1. 极致的灵敏度与低输入量
传统ChIP-seq通常需要105105至107107个细胞,这对于许多珍贵的生物样本来说是难以逾越的门槛。CUT&Tag凭借其“零背景”特性,仅需100100至10001000个细胞即可获得高质量数据,甚至在优化条件下可实现单细胞分辨率(scCUT&Tag)。这使得研究者能够以前所未有的精度探索干细胞分化轨迹、肿瘤微环境中的稀有细胞亚群以及临床活检样本的表观遗传特征。
2. 卓越的信噪比(Signal-to-Noise Ratio)
ChIP-seq中,超声破碎产生的随机断裂和非特异性抗体结合会产生大量背景噪音,往往需要深度测序(>20M reads)才能覆盖真实的结合峰。相比之下,CUT&Tag的背景极低,通常仅需100万至500万读数(reads)即可达到甚至超越ChIP-seq千万级读数的分辨率。这不仅显著降低了测序成本,还使得弱信号(如低丰度转录因子结合或特定的抑制性修饰)的检测成为可能。
3. 高分辨率与准确性
由于Tn5转座酶在抗体结合位点附近进行切割,CUT&Tag生成的峰(Peaks)极其尖锐,分辨率可达单核小体水平。这对于精确界定组蛋白修饰的边界(如区分启动子区的H3K4me3与邻近的增强子区)至关重要。此外,无需剧烈的超声破碎避免了染色质结构的物理破坏,更好地保留了体内真实的染色质状态。
4. 操作简便与高通量兼容性
CUT&Tag全程可在96孔板中进行,无需昂贵的超声仪器和复杂的磁珠纯化步骤,极易实现自动化和高通量筛选。这为大规模的药物筛选、时间序列分析以及多条件平行实验提供了极大的便利。
三、在组蛋白修饰研究中的深度应用
1、活跃与抑制性修饰的精细图谱
CUT&Tag已成功应用于各类组蛋白修饰的测绘。对于活跃标记(如H3K4me3, H3K27ac, H3K36me3),CUT&Tag能清晰地区分启动子与增强子,甚至能捕捉到瞬时的转录爆发事件。对于抑制性标记(如H3K27me3, H3K9me3),由于其覆盖范围较广且信号相对弥散,传统ChIP-seq往往难以界定边界,而CUT&Tag凭借高信噪比,能够更准确地描绘异染色质的扩散范围和边界元件(Boundary Elements),揭示Polycomb复合物介导的基因沉默机制。
2、发育生物学与细胞命运决定
在胚胎发育早期,细胞数量极少且表观遗传状态动态变化剧烈。CUT&Tag使得在小鼠囊胚、人类原肠胚等微量样本中绘制全基因组组蛋白修饰图谱成为现实。研究者利用该技术追踪了多能性因子与组蛋白修饰的动态互作,揭示了从全能性到多能性转变过程中的表观遗传重编程细节。
3、疾病机制与临床转化
在癌症研究中,CUT&Tag被广泛用于鉴定癌细胞的特异性表观遗传驱动因子。例如,通过分析白血病干细胞中的H3K27ac图谱,研究者发现了超级增强子(Super-enhancers)驱动的致癌基因网络。此外,由于其对福尔马林固定石蜡包埋(FFPE)样本的兼容性日益提高,CUT&Tag正逐渐进入临床病理分析领域,有望成为基于表观遗传标志物的癌症诊断和预后评估的新工具。
四、技术挑战、优化策略与2026年新展望
尽管CUT&Tag优势显著,但在实际应用中仍面临一些挑战。首先是抗体依赖性:与ChIP-seq一样,抗体的质量直接决定实验成败。对于某些缺乏高质量抗体的罕见修饰,技术应用受限。其次是透化效率的控制:不同细胞类型的细胞膜和核膜结构差异巨大,洋地黄皂苷的浓度需要精细优化,过度透化会导致核内蛋白流失,透化不足则阻碍抗体进入。
针对这些问题,近年来涌现了多项改进策略:
CUT&Tag 2.0/3.0:引入了更高效的Tn5变体和优化的缓冲液体系,进一步提升了低丰度靶点的检测能力。
多路复用技术(Multiplexing):利用独特的分子条形码(Barcodes),可以在同一反应体系中同时检测多种组蛋白修饰,或者混合多个样本进行并行测序,大幅降低成本。
空间CUT&Tag:结合空间转录组学技术,最新的空间CUT&Tag协议能够在组织切片上原位保留空间信息的同时,解析特定区域的组蛋白修饰状态,这对于理解肿瘤异质性和组织结构功能至关重要。
截至2026年,随着长读长测序技术(如Nanopore)与CUT&Tag的结合,研究者已经能够在一个实验中同时获取组蛋白修饰信息和长片段染色质结构信息,甚至直接检测DNA甲基化与组蛋白修饰的共定位模式(单分子多组学)。此外,人工智能算法被广泛应用于CUT&Tag数据的降噪和峰检测,使得从超低输入量样本中提取生物学信号的能力达到了新的高度。
CUT&Tag技术的出现,标志着表观遗传学研究从“粗放型”向“精细化”、“微量型”的重大跨越。它不仅在技术层面解决了传统ChIP-seq的诸多痛点,更在科学发现层面打开了通往稀有细胞类型和复杂疾病机制的大门。随着技术的不断迭代和多组学整合的深入,基于Tn5转座酶的CUT&Tag及其衍生技术将继续引领我们深入解码染色质上的“第二遗传密码”,为生命科学和医学研究提供前所未有的洞察力。在未来,我们有理由相信,CUT&Tag将成为每一个分子生物学实验室的常规武器,推动表观遗传学进入一个全新的发展纪元。
最新动态
-
05.11
怎么通过ChIP-seq结果分析转录因子的结合基序与结合位点分布?
-
04.27
双分子荧光互补(BiFC)与FRET的核心区别是什么?
-
04.27
外泌体研究方案中的样本来源与实验模型如何设计?
-
04.24
细胞迁移及侵袭实验攻略
-
04.24
等温量热滴定曲线出现正负峰的原因是什么?
-
04.23
EMSA实验中,细胞核蛋白提取质量对结果影响极大,如何保证蛋白的完整性与结合活性?
-
04.23
免疫荧光检测中常见的非特异性荧光有哪些原因?如何减少或避免?
-
04.16
大豆原生质体的亚细胞定位方法
-
04.15
ChIP-seq组蛋白特异性染色质免疫沉淀转录因子结合位点
-
04.10
蛋白质相互作用及亚细胞定位原理与技术










