蛋白质相互作用及亚细胞定位原理与技术
一、蛋白质相互作用原理
蛋白质相互作用是生命活动的核心分子基础,其本质是通过非共价键维系的分子间识别与结合,主要包括氢键、疏水作用力、离子键、范德华力以及二硫键等。蛋白质依靠自身空间结构形成特定的结合界面,如结构域、结合口袋等,与配体蛋白发生特异性结合,进而参与信号传导、物质转运、细胞周期调控、酶促反应调控等一系列生理过程。根据作用稳定性,可分为稳定型复合物与瞬时型相互作用,前者多构成细胞内固有功能复合体,后者则常见于动态信号传递过程。
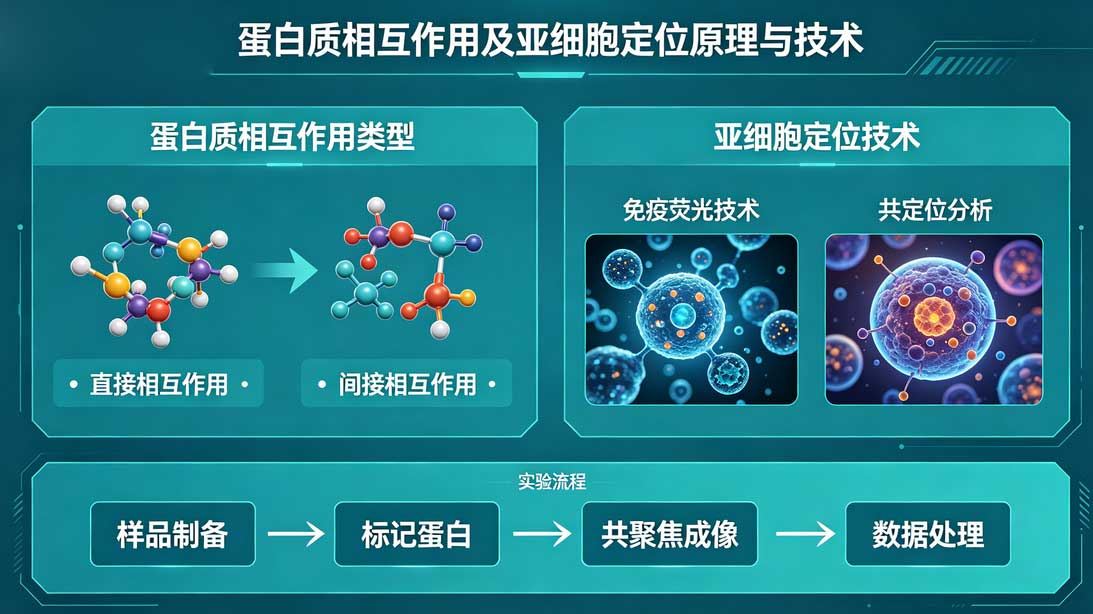
二、蛋白质相互作用研究技术
(1)体内验证技术
酵母双杂交系统以真核转录因子的结构域分离为基础,将待测蛋白分别与DNA结合结构域和转录激活结构域融合,若两种蛋白发生相互作用,可使转录因子功能重建,激活报告基因表达,适用于快速筛选未知相互作用蛋白。荧光共振能量转移技术利用供体荧光蛋白与受体荧光蛋白的能量传递现象,当两种目标蛋白距离足够接近时发生能量转移,通过荧光信号变化判断相互作用,可在活细胞内实时动态观测。双分子荧光互补技术将荧光蛋白拆分为两个无荧光活性的片段,分别与目标蛋白融合,蛋白结合后促使荧光蛋白片段互补恢复荧光,直观反映相互作用的发生与亚细胞位置。
(2)体外验证技术
免疫共沉淀基于抗原与抗体的特异性结合,在非变性条件下裂解细胞,利用抗体捕获目标蛋白,与其相互作用的蛋白会共同沉淀,经检测可验证已知蛋白间相互作用。谷胱甘肽巯基转移酶pull-down实验通过将蛋白与谷胱甘肽巯基转移酶融合表达并固定于亲和介质,孵育待测蛋白后洗脱结合蛋白,用于验证体外直接相互作用,排除细胞内其他分子干扰。表面等离子体共振无需标记蛋白,通过检测芯片表面折射率变化判断蛋白结合情况,可定量分析结合速率、解离速率与亲和力。微量热泳动则利用分子在温度梯度中的运动差异,检测蛋白结合引起的热泳动变化,适用于低亲和力、复杂样品体系的相互作用分析。
(3)组学水平筛选技术
串联亲和纯化联合质谱技术通过两步亲和纯化获得高纯度蛋白复合物,再经质谱鉴定复合物组分,适用于大规模筛选生理状态下的相互作用蛋白网络。蛋白质微阵列将大量蛋白固定于载体表面,孵育荧光标记探针蛋白,通过信号识别高通量筛选相互作用蛋白,可快速构建互作网络。
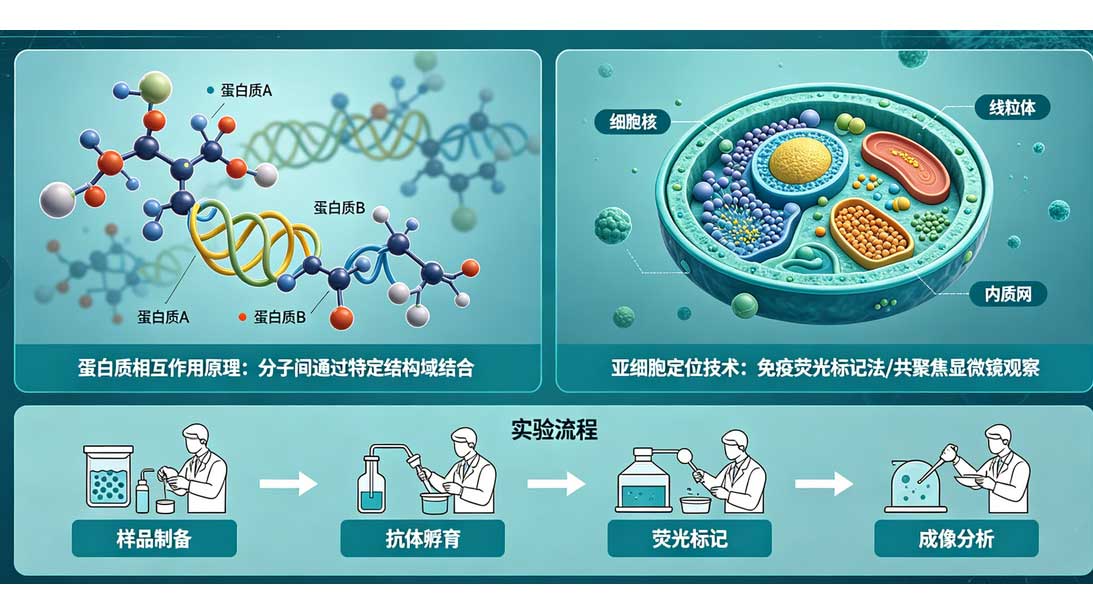
三、亚细胞定位原理
蛋白质亚细胞定位由其自身携带的定位信号序列决定,这类信号序列是一段特定氨基酸序列,引导蛋白质精准转运至对应亚细胞区域并发挥功能。常见定位信号包括核定位信号负责介导蛋白进入细胞核,核输出信号调控蛋白从细胞核输出,线粒体靶向序列引导蛋白转运至线粒体,信号肽则主要介导蛋白进入内质网并进一步定位至细胞膜、溶酶体或分泌到细胞外。蛋白质转运依赖细胞内转运系统与分子伴侣,通过膜上受体识别、通道蛋白介导等方式完成跨膜运输,最终实现特定亚细胞定位。
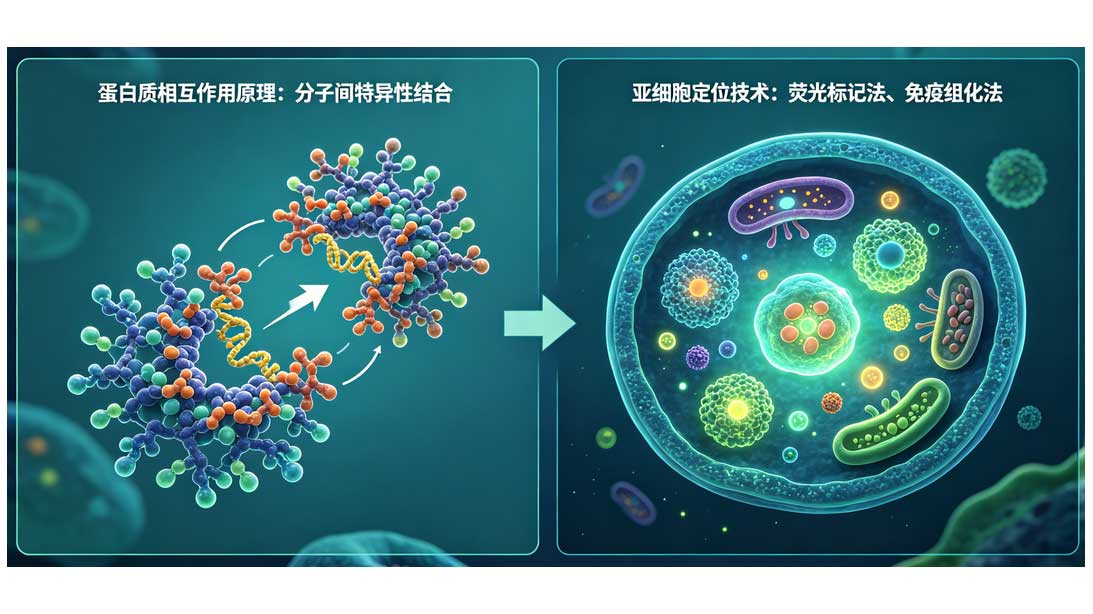
四、亚细胞定位研究技术
(1)荧光标记示踪技术
荧光蛋白标记法是将绿色荧光蛋白及其突变体等荧光蛋白与目标蛋白融合构建表达载体,转染细胞后通过荧光显微镜直接观察融合蛋白的分布,直观反映天然状态下蛋白的亚细胞位置,是目前最常用的活细胞定位技术。免疫荧光技术利用目标蛋白的特异性抗体与细胞内蛋白结合,再用荧光标记二抗进行孵育,通过荧光信号判断蛋白定位,适用于无法构建融合蛋白的内源性蛋白检测。
(2)细胞组分分离技术
差速离心与密度梯度离心通过逐步提高离心速率分离细胞核、线粒体、内质网、细胞质等不同亚细胞组分,提取各组分蛋白后,通过Western blot检测目标蛋白在各组分中的含量,判断其主要定位区域,可实现定量分析。
(3)生物信息学预测技术
在实验验证前,可通过在线工具依据蛋白质氨基酸序列中的定位信号进行预测,分析核定位信号、线粒体靶向序列等特征位点,初步推断蛋白可能的亚细胞分布,为后续实验设计提供参考。
(4)显微成像技术
共聚焦激光扫描显微镜通过逐层扫描获得清晰荧光图像,排除焦平面外信号干扰,精准定位蛋白在细胞内的三维分布。超高分辨率显微镜突破传统光学衍射极限,可观察更精细的亚细胞结构与蛋白定位,适用于微小结构内的蛋白分布分析。
最新动态
-
05.11
怎么通过ChIP-seq结果分析转录因子的结合基序与结合位点分布?
-
04.27
双分子荧光互补(BiFC)与FRET的核心区别是什么?
-
04.27
外泌体研究方案中的样本来源与实验模型如何设计?
-
04.24
细胞迁移及侵袭实验攻略
-
04.24
等温量热滴定曲线出现正负峰的原因是什么?
-
04.23
EMSA实验中,细胞核蛋白提取质量对结果影响极大,如何保证蛋白的完整性与结合活性?
-
04.23
免疫荧光检测中常见的非特异性荧光有哪些原因?如何减少或避免?
-
04.16
大豆原生质体的亚细胞定位方法
-
04.15
ChIP-seq组蛋白特异性染色质免疫沉淀转录因子结合位点
-
04.10
蛋白质相互作用及亚细胞定位原理与技术










