重组抗体片段表达服务 | Fab与scFv单链抗体高效表达
在现代生物医药、诊断试剂开发、基础免疫学研究及靶向药物研发领域,抗体类分子已成为核心功能元件。相较于完整抗体分子,重组抗体片段具有分子量小、组织穿透性强、免疫原性低、易于基因工程改造、可大规模异源表达等显著优势,在靶向治疗、免疫检测、蛋白互作筛选、体内成像等场景中展现出广阔应用前景。Fab片段与scFv单链抗体作为应用最广泛的两类重组抗体片段,其高效、稳定、规模化的表达制备,是推动抗体药物从基础研究走向临床转化的关键环节。重组抗体片段表达服务依托成熟的分子克隆、宿主表达系统优化及蛋白纯化技术,为科研机构与生物医药企业提供从基因设计、载体构建、蛋白表达到功能验证的一站式解决方案,实现Fab与scFv单链抗体的高效表达与高质量制备,为下游研发工作提供可靠原料支撑。
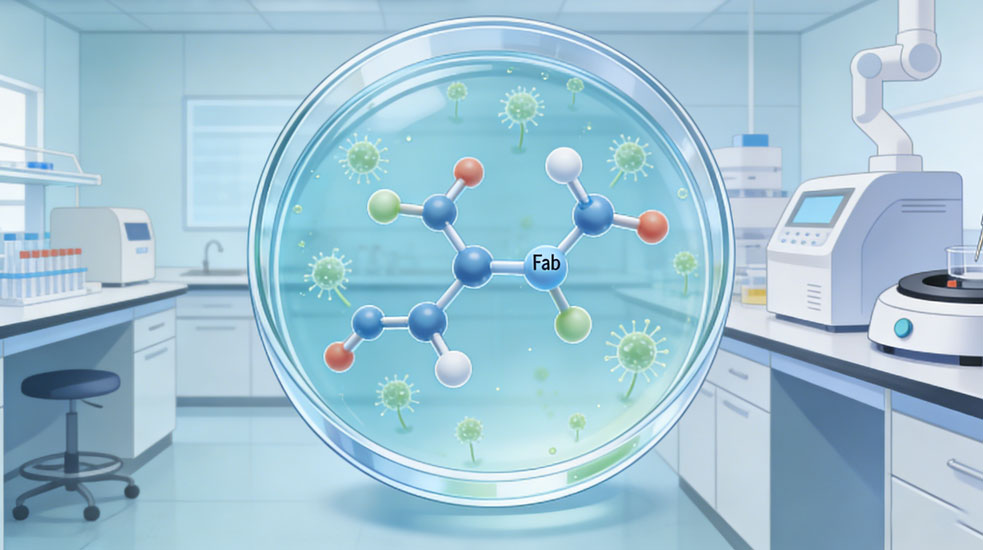
完整免疫球蛋白G(IgG)抗体由两条重链和两条轻链通过二硫键连接形成,结构复杂,糖基化修饰多样,在原核表达系统中难以正确折叠,且生产成本高、体内分布受限。重组抗体片段通过基因工程手段截短抗体结构,保留抗原结合核心区域,去除无关结构域,大幅提升实用性与可操作性。Fab片段由重链N端的VH-CH1结构域与完整轻链VL-CL通过二硫键连接构成,保留天然抗体的抗原结合位点,结构稳定性高,抗原结合亲和力接近完整抗体,同时具备良好的水溶性与组织渗透能力,常用于免疫组化、免疫沉淀、体外诊断试剂开发及靶向药物载体构建。scFv单链抗体则通过柔性连接肽将重链可变区VH与轻链可变区VL直接融合,形成单一多肽链,是最小的具备完整抗原结合活性的抗体单元,分子量仅约27kDa,具有极强的组织穿透性,可快速到达实体瘤深部组织,在肿瘤靶向治疗、体内分子成像、噬菌体展示文库筛选等领域具有不可替代的优势。
重组抗体片段表达服务的核心价值,在于解决科研与工业场景中抗体片段表达量低、折叠错误、可溶性差、纯化困难、功能活性不稳定等共性难题。对于非专业实验室而言,自行开展Fab与scFv表达往往面临基因优化不足、宿主选择不当、表达条件未经验证、纯化工艺粗糙等问题,不仅耗时耗力,还难以获得满足实验需求的蛋白样品。专业化表达服务通过标准化流程与定制化策略,兼顾表达效率与蛋白质量,实现从基因序列到功能活性蛋白的快速交付,大幅缩短研发周期,降低实验成本,保障后续实验数据的可靠性与重复性。
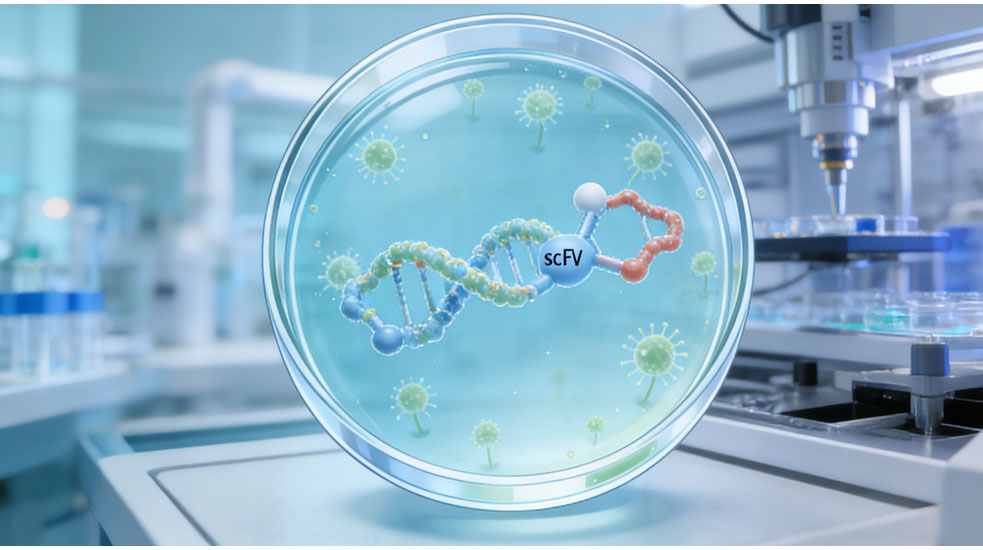
基因设计与序列优化是Fab与scFv高效表达的首要环节。服务平台首先根据客户提供的亲本抗体序列、抗原信息或噬菌体展示文库筛选结果,进行抗体可变区序列分析,去除潜在的疏水性位点、蛋白酶切割位点与稀有密码子,针对目标表达宿主进行密码子偏好性优化,提升转录与翻译效率。对于Fab片段,需分别设计重链Fd段与轻链基因,合理配置信号肽序列,确保两条链在胞内同步表达并正确形成二硫键;对于scFv单链抗体,需选择合适长度与疏水性的连接肽,常用(Gly4Ser)柔性连接肽,保证VH与VL结构域自由折叠,不影响抗原结合空间构象。同时,服务团队可根据应用需求添加His标签、Flag标签、HA标签或SUMO融合标签,既便于后续亲和纯化,又可提升蛋白可溶性,避免表达产物形成包涵体。
载体构建与克隆验证是实现稳定表达的基础。服务平台选用经过工程化改造的高效表达载体,针对原核与真核表达系统分别配置适配元件。原核表达系统以大肠杆菌为主,载体通常包含强启动子、严谨的调控元件、核糖体结合位点及筛选标记,可实现目标蛋白的诱导表达与可控积累。真核表达系统如毕赤酵母、哺乳动物细胞,则针对抗体片段的折叠、二硫键形成及翻译后修饰需求,选用分泌型表达载体,使目标蛋白直接分泌至培养上清,简化纯化流程。在载体构建过程中,采用限制性酶切连接、Gibson同源重组或Gateway克隆技术,将优化后的抗体片段基因精准插入载体多克隆位点,完成重组质粒构建后,通过菌落PCR、酶切鉴定及 Sanger测序,确保基因序列完全正确、阅读框无误,杜绝突变、缺失或移码等问题,为后续高效表达奠定序列基础。

表达宿主系统的选择与优化,直接决定Fab与scFv的表达产量与活性。大肠杆菌表达系统因生长速度快、培养成本低、遗传背景清晰、操作简便,是Fab与scFv片段最常用的表达宿主,尤其适合规模化制备。服务平台根据抗体片段特性选择BL21 (DE3)、Rosetta (DE3)、Shuffle等工程菌株,其中Shuffle菌株可增强胞内二硫键形成能力,显著提升Fab与scFv的可溶性表达水平。针对包涵体表达问题,服务团队通过优化诱导温度、诱导剂浓度、诱导时机及培养转速,采用低温慢速诱导策略,减少蛋白聚集,提升可溶性比例。对于结构复杂、对折叠环境要求较高的 Fab 片段,还可采用周质腔分泌表达策略,利用细菌周质腔的氧化环境助力二硫键正确形成。
毕赤酵母表达系统兼具原核表达的便捷性与真核折叠优势,可实现抗体片段的分泌型表达,蛋白折叠更接近天然构象,适合对活性要求高的scFv与Fab制备。哺乳动物细胞表达系统如HEK293、CHO细胞,虽表达成本较高,但可完成更精准的翻译后修饰,表达产物空间结构最接近天然状态,适用于临床前研究、体内实验等高要求场景。重组抗体片段表达服务可根据客户对产量、纯度、活性及应用场景的需求,灵活选择最优表达系统,并通过培养基优化、补料策略调控、培养条件微调,实现表达量最大化,常规条件下可实现毫克级至克级规模的Fab与scFv制备。
蛋白纯化与复性工艺是保障抗体片段质量的核心步骤。对于可溶性表达产物,服务平台采用亲和层析、离子交换层析、凝胶过滤层析等多级纯化策略,利用融合标签进行一步亲和纯化,再通过脱盐、浓缩去除杂质与添加剂,获得高纯度目标蛋白。对于以包涵体形式存在的表达产物,建立标准化复性工艺,通过温和变性剂溶解包涵体,采用透析复性、稀释复性或柱上复性技术,在可控条件下帮助蛋白重新折叠为天然空间构象,有效恢复抗原结合活性。纯化完成后,通过SDS-PAGE凝胶电泳检测蛋白纯度,通常可达到90%以上,同时利用BCA或Bradford法进行蛋白定量,确保交付样品浓度满足客户需求。
功能活性验证是重组抗体片段表达服务的重要质控环节。服务平台不局限于蛋白制备,更注重抗体片段的实际应用价值,通过多种技术手段验证其抗原结合能力与特异性。采用酶联免疫吸附实验(ELISA)检测抗体片段与目标抗原的结合活性;通过Western Blot验证抗原识别特异性;利用生物膜干涉技术(BLI)或表面等离子体共振技术(SPR)测定平衡解离常数(KD值),定量评估亲和力大小;对于scFv单链抗体,还可进行免疫荧光、流式细胞术等细胞水平功能验证。通过多维度质控,确保交付的Fab与scFv片段不仅纯度达标、浓度稳定,更具备良好的特异性结合能力,可直接用于下游实验。
在实际应用场景中,重组抗体片段表达服务已广泛覆盖基础科研、体外诊断、靶向药物开发等领域。在基础免疫学研究中,高纯度Fab与scFv可用于抗原表位鉴定、蛋白-蛋白相互作用解析、免疫信号通路研究;在诊断试剂开发中,因其分子量小、结合特异性强,可作为核心识别元件构建高灵敏度ELISA、胶体金试纸条、化学发光检测试剂盒;在肿瘤治疗领域,scFv可作为靶向模块与毒素、细胞因子、纳米药物偶联,构建抗体药物偶联物(ADC)或双特异性抗体,提升药物靶向性,降低毒副作用;在体内成像中,小分子抗体片段可快速清除背景信号,实现高分辨率肿瘤组织成像。
随着抗体药物产业快速发展,市场对Fab与scFv单链抗体的需求持续增长,对表达服务的效率、质量与定制化能力提出更高要求。专业化表达服务平台不断升级技术体系,引入高通量克隆、高密度发酵、自动化纯化等先进技术,进一步提升表达效率与批次稳定性;同时针对特殊需求提供定制化改造服务,如抗体亲和力成熟、人源化改造、多价抗体构建、荧光标记与生物素标记等,拓展抗体片段的应用范围。
重组抗体片段表达服务以Fab与scFv单链抗体为核心产品,通过基因优化、载体构建、宿主筛选、表达调控、高效纯化与功能验证的全流程标准化方案,解决了重组抗体片段表达难度大、活性不稳定、制备周期长等技术痛点,为科研工作者与生物医药企业提供高质量、高效率、高可靠性的抗体片段制备解决方案。在精准医疗与靶向治疗快速发展的背景下,高效的重组抗体片段表达服务将持续支撑创新抗体药物的研发进程,推动基础研究成果向临床应用转化,为疾病诊断与治疗提供关键技术支撑。
最新动态
-
05.11
怎么通过ChIP-seq结果分析转录因子的结合基序与结合位点分布?
-
04.27
双分子荧光互补(BiFC)与FRET的核心区别是什么?
-
04.27
外泌体研究方案中的样本来源与实验模型如何设计?
-
04.24
细胞迁移及侵袭实验攻略
-
04.24
等温量热滴定曲线出现正负峰的原因是什么?
-
04.23
EMSA实验中,细胞核蛋白提取质量对结果影响极大,如何保证蛋白的完整性与结合活性?
-
04.23
免疫荧光检测中常见的非特异性荧光有哪些原因?如何减少或避免?
-
04.16
大豆原生质体的亚细胞定位方法
-
04.15
ChIP-seq组蛋白特异性染色质免疫沉淀转录因子结合位点
-
04.10
蛋白质相互作用及亚细胞定位原理与技术










