千年古方,纳米新生:科学家破解半夏如何“指挥”免疫细胞对抗肺癌!
肺癌是全球范围内发病率和死亡率最高的恶性肿瘤之一,现有治疗手段在疗效与毒性方面仍面临显著局限。近年来,免疫调节成为肿瘤治疗的重要策略,其中肿瘤相关巨噬细胞(TAMs)在肿瘤微环境中的极化状态直接影响抗肿瘤免疫应答,其代谢重编程与免疫功能调控受到广泛关注。与此同时,植物来源的纳米囊泡作为天然活性成分的载体,在跨物种信号传递和免疫调节中展现出独特潜力,为中药现代化与纳米医学的融合提供了新思路。
半夏(Pinellia ternata)作为传统中药材,具有化痰、止咳、抗肿瘤等多重药理活性,但其具体作用机制尚未完全阐明。本研究聚焦于从半夏鲜根中提取的纳米级类外泌体囊泡(PEVs),系统探究其在调控巨噬细胞极化及抑制肺癌生长中的作用与机制。
该研究于2026年2月发表在《Phytomedicine》(IF:8.3)期刊上,题为《Pinellia exosomal vesicles remodulate tumor-associated macrophage polarization via the serine synthesis/JAK/STAT signaling pathway to inhibit lung cancer growth》。文章首次揭示PEVs通过抑制丝氨酸合成途径关键基因(PHGDH、PSAT1、PSPH)的表达,进而激活JAK/STAT信号通路,促使巨噬细胞向促炎M1型极化,增强其对肺癌细胞的免疫监视与杀伤功能。同时,PEVs还能直接诱导肺癌细胞S期阻滞,并在体内实验中显著抑制肿瘤生长。该研究不仅阐明了半夏免疫调节作用的代谢与信号机制,也为基于植物囊泡的肺癌免疫治疗提供了新的理论与实验依据。

一、研究创新点
➤发现了传统中药半夏中具有免疫调节功能的纳米载体
➤阐明了PEVs重塑肿瘤免疫微环境(TME)的新机制
➤揭示了PEVs跨细胞协同抗肿瘤的双重作用模式:间接免疫调节和直接细胞作用。
➤提出了PEVs中潜在的关键活性成分及其作用假设
➤验证了口服PEVs的体内抗肿瘤活性及良好安全性
二、主要研究思路
1、PEVs的提取与表征
采用差速超速离心法从鲜半夏根中提取PEVs,并通过TEM、DLS、SDS-PAGE、脂质组学与蛋白质组学进行系统表征。
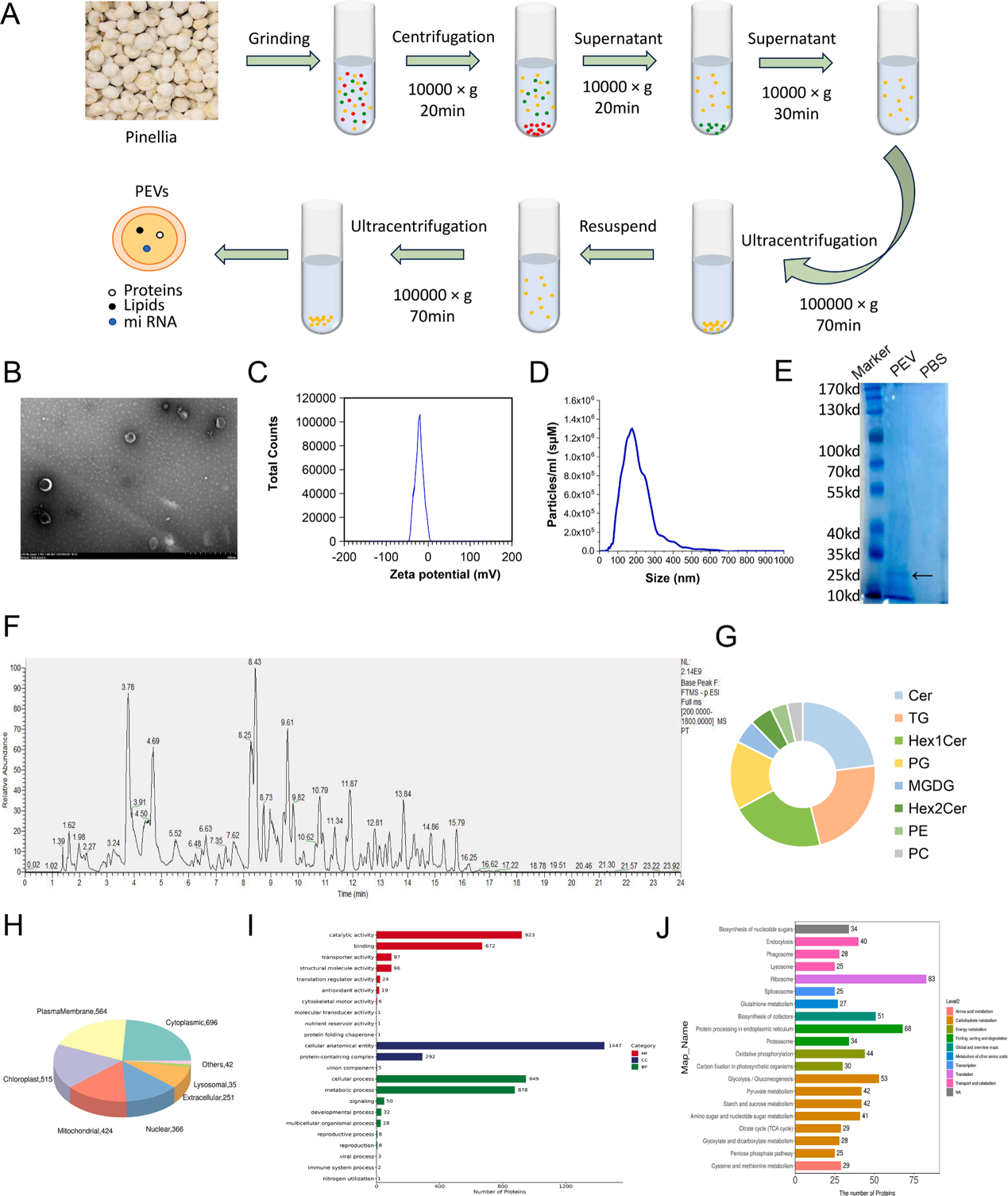
图1. PEVs的提取与表征
2、巨噬细胞极化调控实验
通过使用THP-1来源的巨噬细胞,验证PEVs能促进M0和M2型巨噬细胞向M1型极化,增强其免疫激活功能。
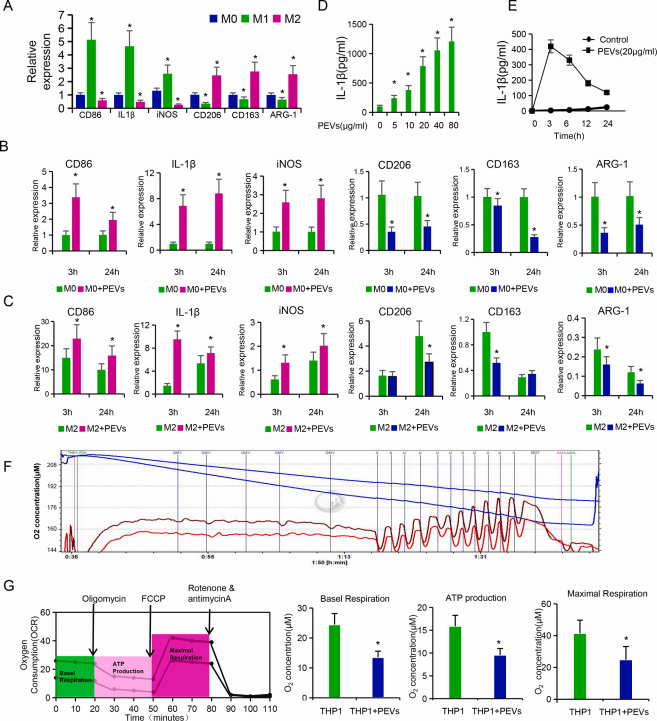
图2. 半夏外泌体(PEVs)促进THP-1来源巨噬细胞向M1样表型的分化与极化
3、PEVs对肺癌细胞的抑制作用
通过共培养体系、条件培养基实验,验证PEVs通过巨噬细胞间接抑制肺癌细胞增殖。
为确定PEVs诱导的巨噬细胞M1极化是否具有肿瘤抑制作用,本研究采用两种实验方法。第一种方法中,将PEVs处理的巨噬细胞条件培养基分别作用于PC9 、HCC827 、A549和H1975肺癌细胞系基于 CCK -8和集落形成实验,用THP1-PEVs条件培养基处理的肿瘤细胞增殖显著减少(图3 A ,3 B-C)。在第二种方法中,将10 μ g/mL的PEVs加入共培养系统的上室。EdU实验显示肿瘤细胞增殖受到抑制,且细胞核被Hoechst染色(图3 D-E)。
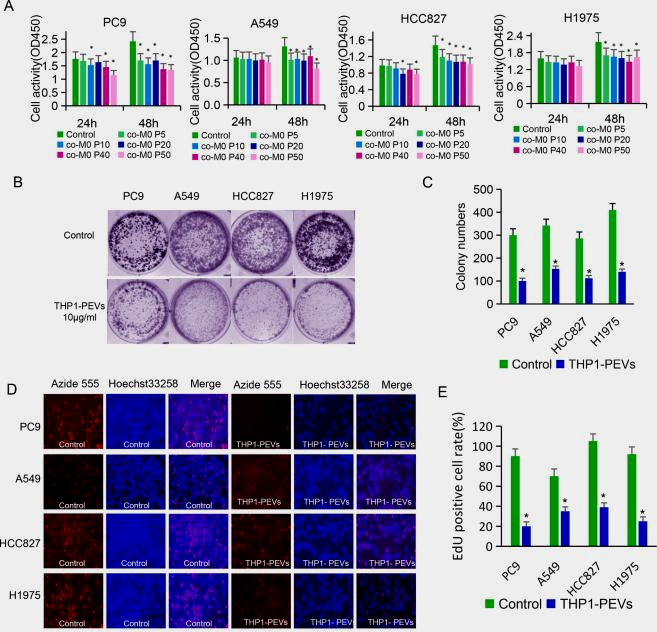
图3. PEVs对肺癌细胞增殖的抑制作用是通过M1样巨噬细胞极化实现的
通过直接处理肺癌细胞,评估PEVs对其增殖、凋亡和细胞周期的影响。
随着 PEVs浓度的增加,细胞存活率逐渐下降在测试浓度范围内,10-20 μ g/mL的 PEVs 在所有细胞系中表现出最强的抑制效果(图4A)。流式细胞术分析显示,所有细胞系在暴露于 PEV 后均出现S期细胞周期阻滞(图4 B-4C),而这些肺癌细胞中仅检测到微小的凋亡变化(图4 D)。而细胞周期相关蛋白CDK2的表达增加,CCND1的表达减少,表明肺癌细胞进入S期阻滞(图4E) 。这些发现表明,PEVs主要通过诱导S期阻滞对肺癌细胞产生直接抗增殖作用,且不依赖于显著的细胞凋亡。
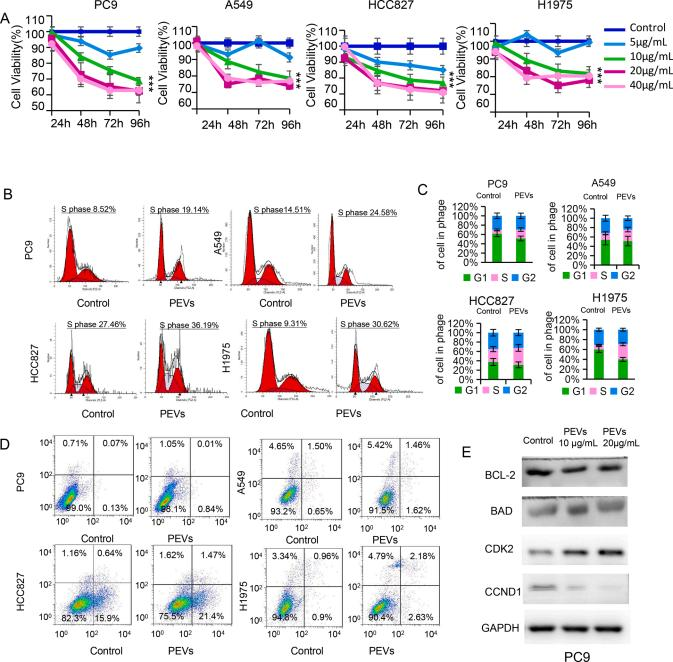
图4. PEVs对肺癌细胞的直接抑制作用
4、通路探究及分子机制研究
转录组测序分析PEVs对巨噬细胞和肺癌细胞基因表达的影响。
转录组测序显示,PEVs处理后的巨噬细胞出现显著的基因表达重编程(图5A-B):促炎相关基因(如CXCL8、IFNB1、IL1β)明显上调,而丝氨酸合成途径关键基因(PHGDH、PSAT1)及氧化磷酸化相关基因(如Ndufs3、Ndufa4)则显著下调(图5D)。 KEGG通路富集分析进一步证实,JAK/STAT、NF-κB等免疫相关信号通路被广泛激活(图5C)。在肺癌细胞中,PEVs亦引起共同差异基因表达(图5F),且与巨噬细胞在JAK/STAT等通路上变化趋势一致(图5G),提示其具有跨细胞的协同调控机制。
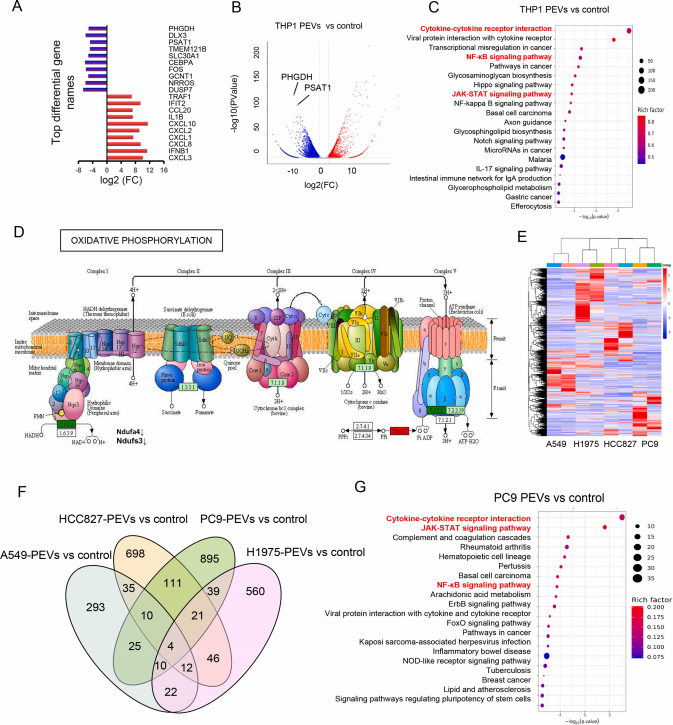
图5. THP-1巨噬细胞与肺癌细胞暴露于PEVs后的 KEGG 通路分析
验证PEVs抑制丝氨酸合成关键基因(PHGDH/PSAT1/PSPH),进而激活JAK/STAT通路。
转录变化通过定量PCR和蛋白质印迹法在mRNA和蛋白水平上得到验证(图6A-B)。这些结果表明PEVs通过同时靶向丝氨酸生物合成途径中的多种酶来抑制丝氨酸合成,该抑制效果在肺癌细胞系及公共临床数据中均得到验证(图6D-E),且这些基因在肺癌组织中普遍高表达。通过分子对接分析,发现SPT对 PHGDH 、PSAT1和 PSPH 具有强结合亲和力(图6 C) 。功能实验显示,敲低上述基因可显著激活JAK/STAT通路中促炎方向的磷酸化信号(如p-STAT1/2/4升高),同时抑制免疫抑制相关信号(如p-STAT3/5/6降低)(图6F-G),说明PEVs通过调控丝氨酸代谢重塑JAK/STAT信号轴,进而推动巨噬细胞向M1型极化。这一调控机制在PC9肺癌细胞中同样得到证实(图6H-J)。
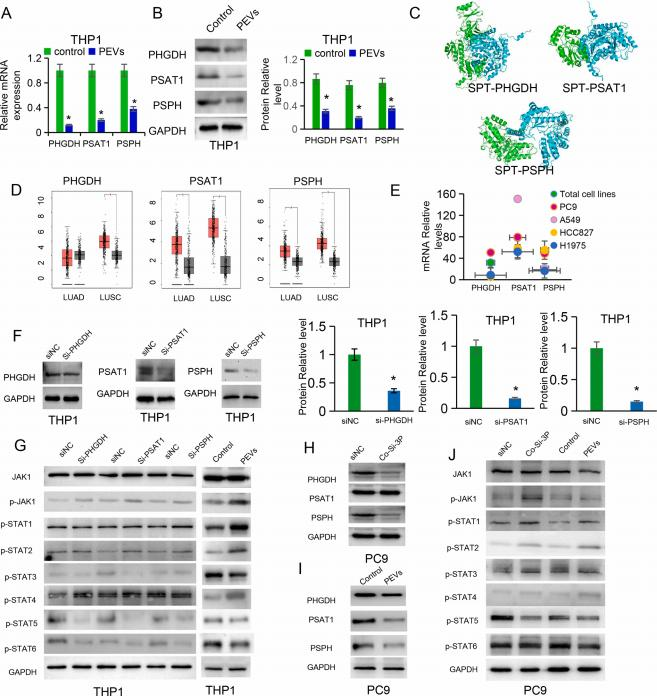
图6. 半夏外泌体(PEVs)通过抑制丝氨酸代谢基因调控JAK-STAT信号通路
05、动物体内实验
建立小鼠LLC肺癌移植瘤模型,口服PEVs后观察肿瘤生长、免疫标志物变化及安全性。
为进一步评估PEVs在体内的抗肿瘤活性,使用LLC肺癌细胞建立了C57BL/6小鼠异种移植模型。将肿瘤细胞皮下注射后,小鼠在7天后开始口服PEVs 。 经过14 天治疗周期后 , 取肿瘤组织进行分析( 图7 A) 。在肺癌移植瘤模型中,口服PEVs能显著抑制肿瘤生长(图7B-C),降低肿瘤细胞增殖标记Ki-67的表达(图7D),并表现出良好的生物安全性,主要脏器未见病理损伤(图7E)。免疫荧光分析进一步显示,PEVs治疗后的肿瘤组织中M1型巨噬细胞标记CD86表达上升,M2型标记CD206表达下降(图7G),表明PEVs在体内能有效逆转肿瘤相关巨噬细胞的极化状态,重塑肿瘤免疫微环境。
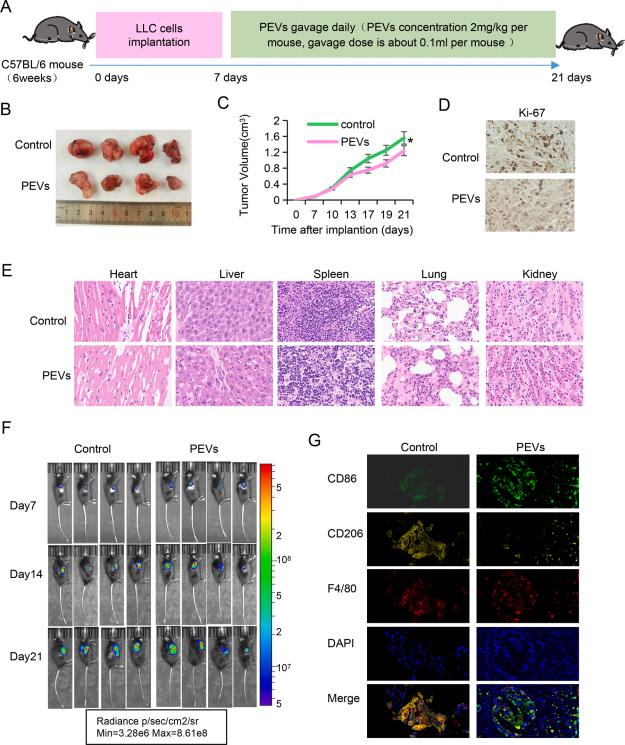
图7. 半夏外泌体(PEVs)在小鼠模型中抑制肺癌进展体内
3、总结
该文章开创性应用植物纳米囊泡治疗癌症:首次从半夏(Pinellia ternata) 中分离出类外泌体纳米囊泡(PEVs),并证实其通过免疫调控机制抑制肺癌,为中医药现代化与纳米技术结合提供了新范式。揭示新颖的免疫代谢调控通路:发现PEVs通过抑制丝氨酸合成途径(PHGDH/PSAT1/PSPH)调控巨噬细胞向M1型极化,并激活JAK/STAT通路,为肿瘤免疫治疗提供了新的代谢干预靶点。提供低毒、天然的肿瘤治疗策略:PEVs来源于传统中药,具有低毒性、高生物相容性的特点,为开发安全有效的天然抗肿瘤药物提供了新思路。
多维度验证机制:研究从细胞、动物模型到转录组、代谢组等多层面系统验证了PEVs的免疫调节与抗肿瘤作用,增强了结论的可信度。
文献来源:Liu M, Wang T, Fu J, Cui T, Li N, Sun T, Liu J, Su C, Song B. Pinellia exosomal vesicles remodulate tumor-associated macrophage polarization via the serine synthesis/JAK/STAT signaling pathway to inhibit lung cancer growth. Phytomedicine. 2026 Feb;151:157759.
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










