“药食同源”顶刊思路(IF=10.5)!来源鉴定+活性追踪+体内验证,全面解析无花果来源外泌体抑制乳腺癌骨转移的双重机制!
乳腺癌是女性最常见恶性肿瘤之一,早期生存率虽显著改善,但远处转移仍为主要死因。骨骼是乳腺癌最常转移部位,约70%晚期患者发生骨转移,表现为溶骨性病变,引发骨痛、病理性骨折、高钙血症等事件,严重影响生活质量及预后。当前治疗包括放化疗及靶向药物(地舒单抗、双膦酸盐),但放化疗毒副作用显著、难以长期应用;靶向治疗仅延缓骨破坏,无法清除骨微环境中残留肿瘤细胞,复发与耐药风险仍存。
因此,开发兼具良好生物安全性、适合长期应用、且能够同时抑制肿瘤生长并重塑骨转移微环境的治疗策略,是当前乳腺癌骨转移研究领域亟待解决的关键问题。
2026年2月,来自陆军军医大学西南医院、西部战区总医院、昆明医科大学等多中心研究团队在《Pharmacological Research》期刊联合发表了题为“Fig-derived exosome-like nanoparticles attenuating bone metastasis of breast cancer through establishing an anti-tumor microenvironment” 的研究论文。该研究首次系统报道了无花果来源外泌体样纳米颗粒(Fig-ELNs) 在乳腺癌骨转移中的治疗作用及分子机制。
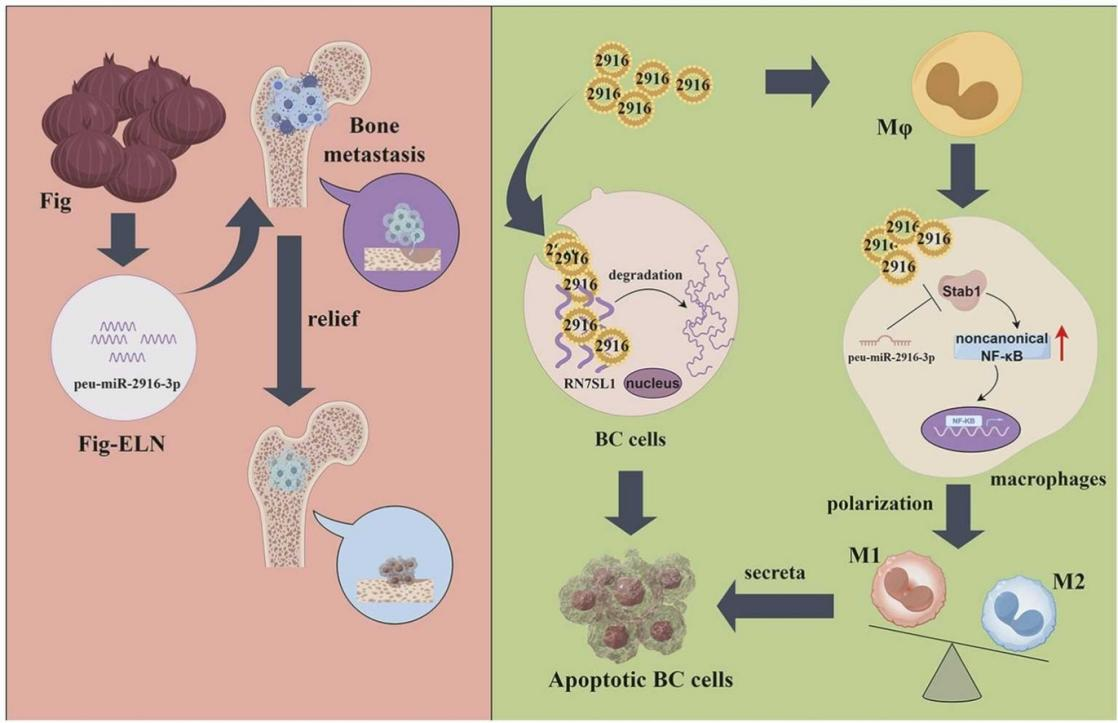
研究证明:Fig-ELNs可通过其携带的微小RNA——peu-miR-2916-p3,直接抑制乳腺癌(BC)细胞增殖(通过靶向RN7SL1促进其降解),并诱导肿瘤相关巨噬细胞向M1型极化(通过靶向Stab1激活非经典NF-κB通路),从而在骨转移局部建立抗肿瘤微环境,显著抑制乳腺癌骨转移进展。Fig-ELNs具备良好的生物安全性,有望成为乳腺癌骨转移的安全、有效的辅助治疗候选策略。

一、研究创新点
❖首次阐明无花果外泌体样纳米颗粒的抗乳腺癌骨转移活性及其物质基础,证实peu-miR-2916-p3为关键效应分子,填补了传统中药无花果抗癌机制研究的空白。
❖揭示植物来源miRNA通过跨物种调控双重靶向肿瘤细胞与免疫细胞:peu-miR-2916-p3一方面靶向RN7SL1直接抑制乳腺癌细胞增殖,另一方面靶向Stab1诱导M1型巨噬细胞极化,实现了“直接杀伤肿瘤”与“重塑抑瘤微环境”的双重协同效应。
❖发现RN7SL1在乳腺癌细胞中的促增殖作用及Fig-ELNs对其稳定性的调控,为乳腺癌治疗提供了潜在新靶点。
❖系统评估Fig-ELNs体内分布及生物安全性,为其向临床转化奠定了重要实验基础。
二、主要研究内容
1、Fig-ELNs的分离与表征
研究者通过差速离心联合超速离心法从无花果匀浆中提取ELNs。纳米颗粒追踪分析显示,Fig-ELNs粒径分布集中于100~200 nm;透射电镜下可见典型的“杯状”囊泡结构;蛋白与核酸定量分析证实Fig-ELNs富含蛋白质及RNA,SDS-PAGE及琼脂糖凝胶电泳进一步提示其主要蛋白分子量约为55 kDa,核酸片段大于500 bp。
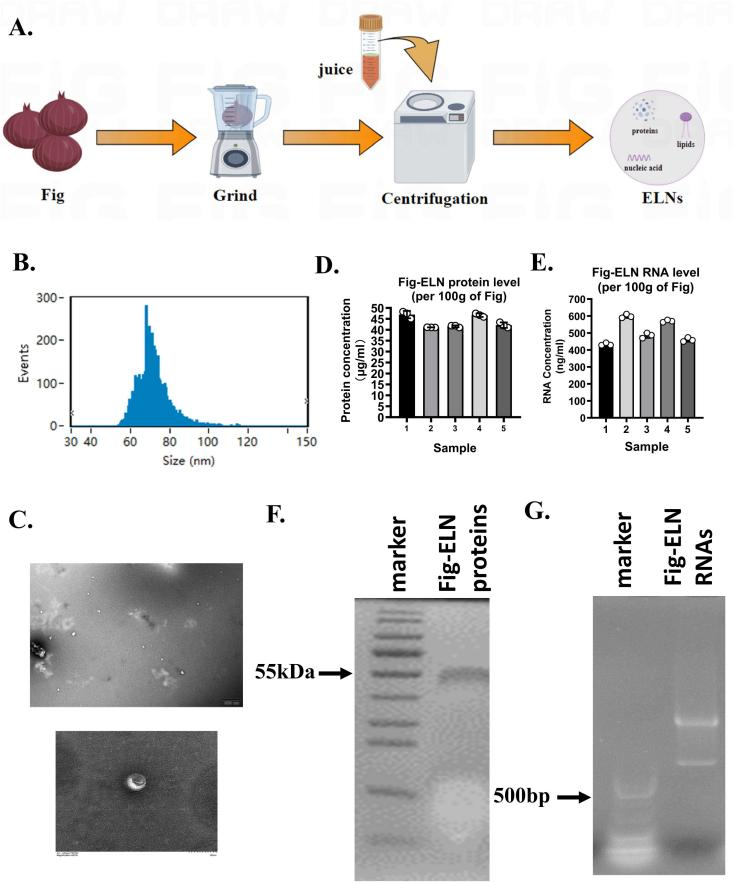
图1. Fig-ELNs的分离及特性
2、Fig-ELNs抑制乳腺癌骨转移
研究者通过PKH-26标记及活体成像技术,考察不同给药途径下Fig-ELNs在小鼠体内的分布特征及组织安全性,证明Fig-ELNs具备良好的生物安全性后,开始进行动物实验。建立人源(MDA-MB-231)及鼠源(4T1)BC细胞胫骨原位骨转移模型,腹腔注射Fig-ELNs,通过活体成像、μCT及组织染色评估疗效。结果发现Fig-ELNs处理后肿瘤体积显著缩小,骨破坏面积减少,破骨细胞活性下降,证实其对乳腺癌骨转移的抑制作用。
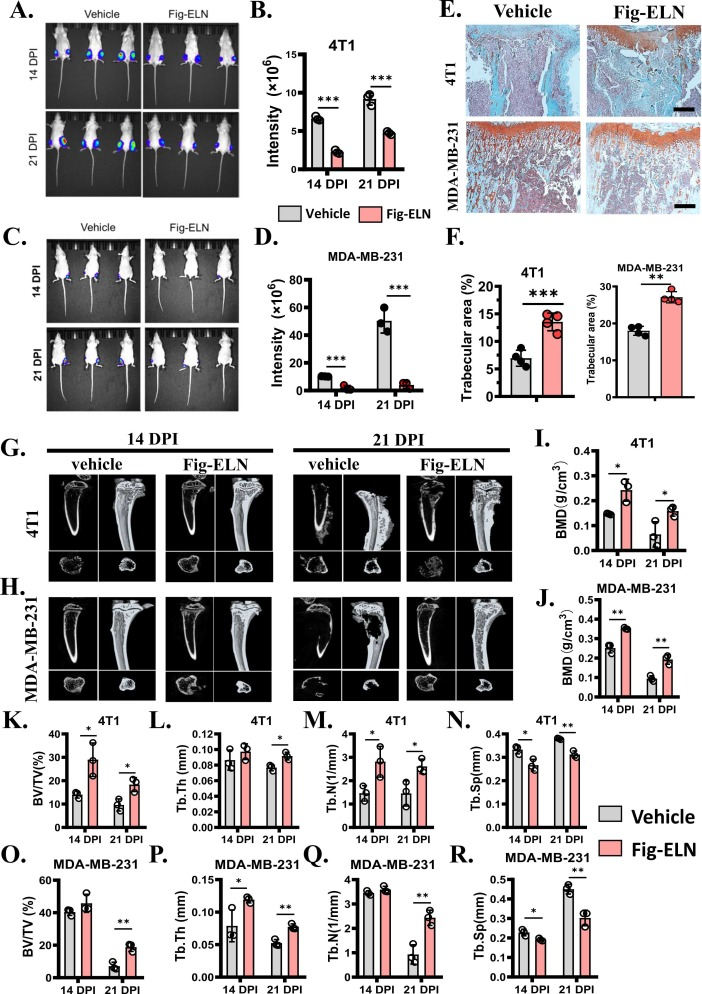
图2. Fig-ELNs的可以减缓BC骨转移进展
3、Fig-ELNs对乳腺癌细胞的直接作用及机制
Fig-ELNs可被MDA-MB-231及MCF-7细胞有效摄取,呈浓度依赖性抑制细胞增殖,并下调细胞周期相关基因(Cenpa、Ccnd1)表达;但对鼠源4T1细胞体外增殖及凋亡无明显影响。转录组测序显示,Fig-ELNs处理后人乳腺癌细胞中RN7SL1表达显著下调;过表达RN7SL1可部分逆转Fig-ELNs的抗增殖效应,提示RN7SL1是Fig-ELNs作用于人乳腺癌细胞的关键下游分子。
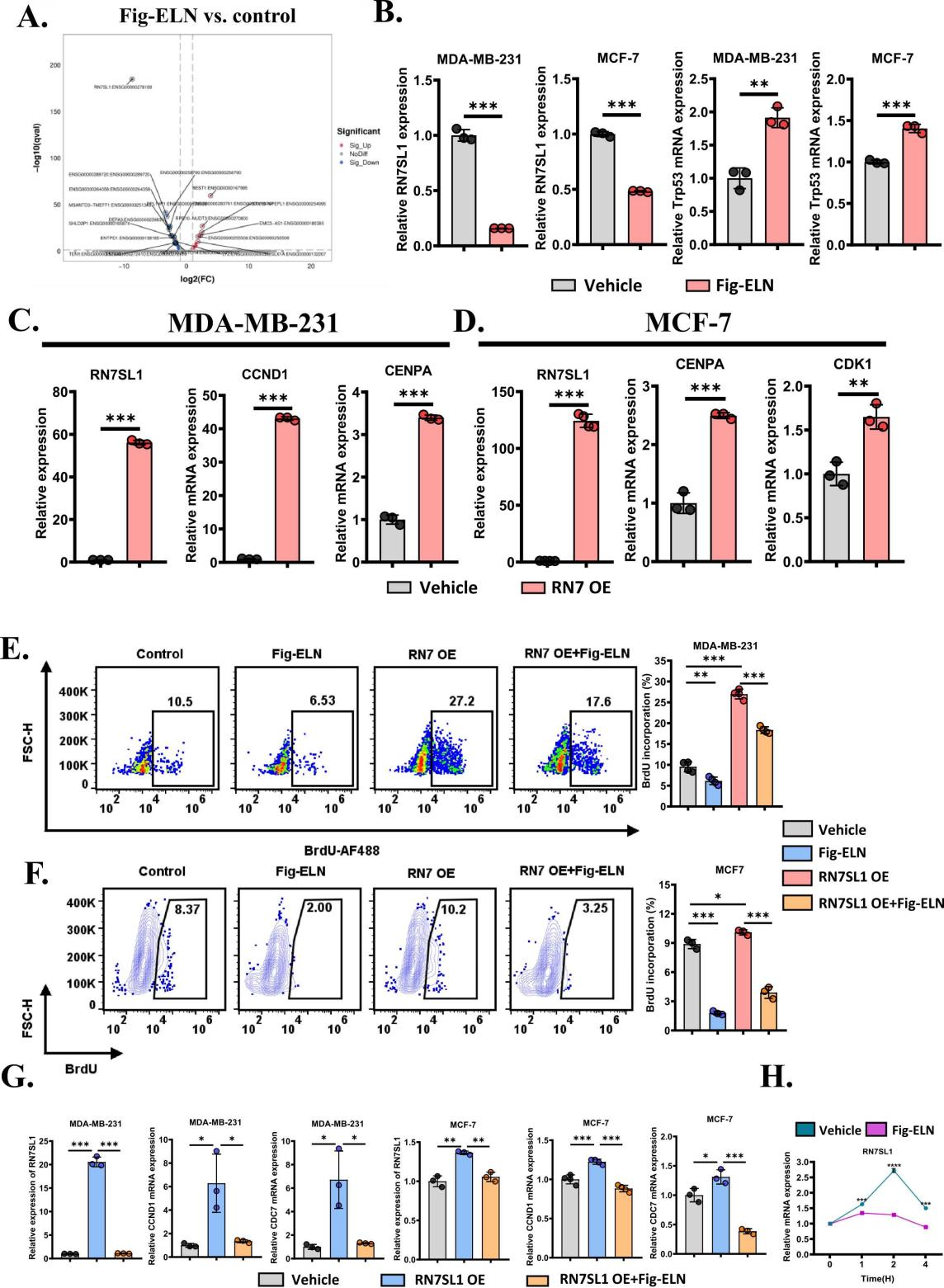
图3. RN7SL1对Fig-ELNs对人类BC细胞增殖的影响至关重要
4、Fig-ELNs诱导M1型巨噬细胞极化及其分子机制
在4T1骨转移模型中,Fig-ELNs处理10天后骨髓M1型巨噬细胞比例显著升高。体外实验证实,Fig-ELNs可协同LPS诱导M1极化标志物(IL-6、TNF-α、IL-1β)表达,抑制IL-4诱导的M2极化标志物(IL-10、Arg1)表达。巨噬细胞条件培养基实验表明,Fig-ELNs刺激的巨噬细胞上清可显著抑制人、鼠乳腺癌细胞增殖,且该效应依赖NF-κB通路——使用NF-κB抑制剂JSH-23可完全消除Fig-ELNs诱导的M1极化及抑瘤效应。
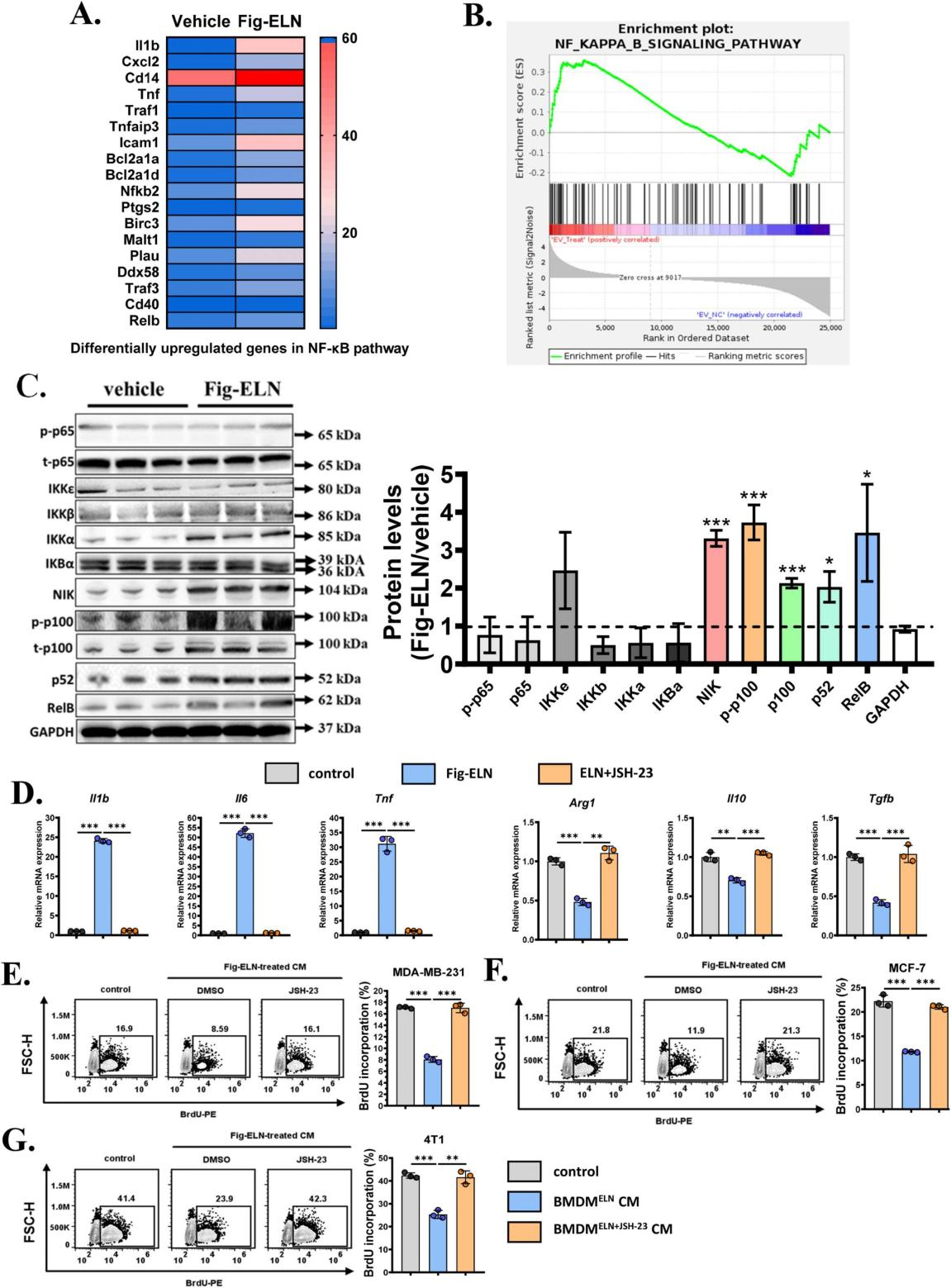
图4. Fig-ELN通过激活非典型的NF-κB通路刺激M1巨噬细胞
5、关键活性成分的筛选与验证
通过核酸/蛋白组分分离实验,研究者发现核酸是Fig-ELNs发挥抗肿瘤及免疫调节作用的主要活性组分。miRNA测序显示,peu-miR-2916-p3及ath-miR-166a-3p是Fig-ELNs中丰度最高的两条miRNA。双荧光素酶报告实验证实,peu-miR-2916-p3可与RN7SL1直接结合并促进其降解;同时,peu-miR-2916-p3也可直接靶向Stab1的3’UTR区。Stab1在巨噬细胞中高表达,且被证实可促进M2极化。Fig-ELNs及peu-miR-2916-p3可显著下调巨噬细胞Stab1表达,激活非经典NF-κB通路;过表达Stab1则可逆转peu-miR-2916-p3诱导的M1极化及NF-κB活化。体内实验进一步证实,peu-miR-2916-p3局部注射可显著抑制乳腺癌骨转移进展。
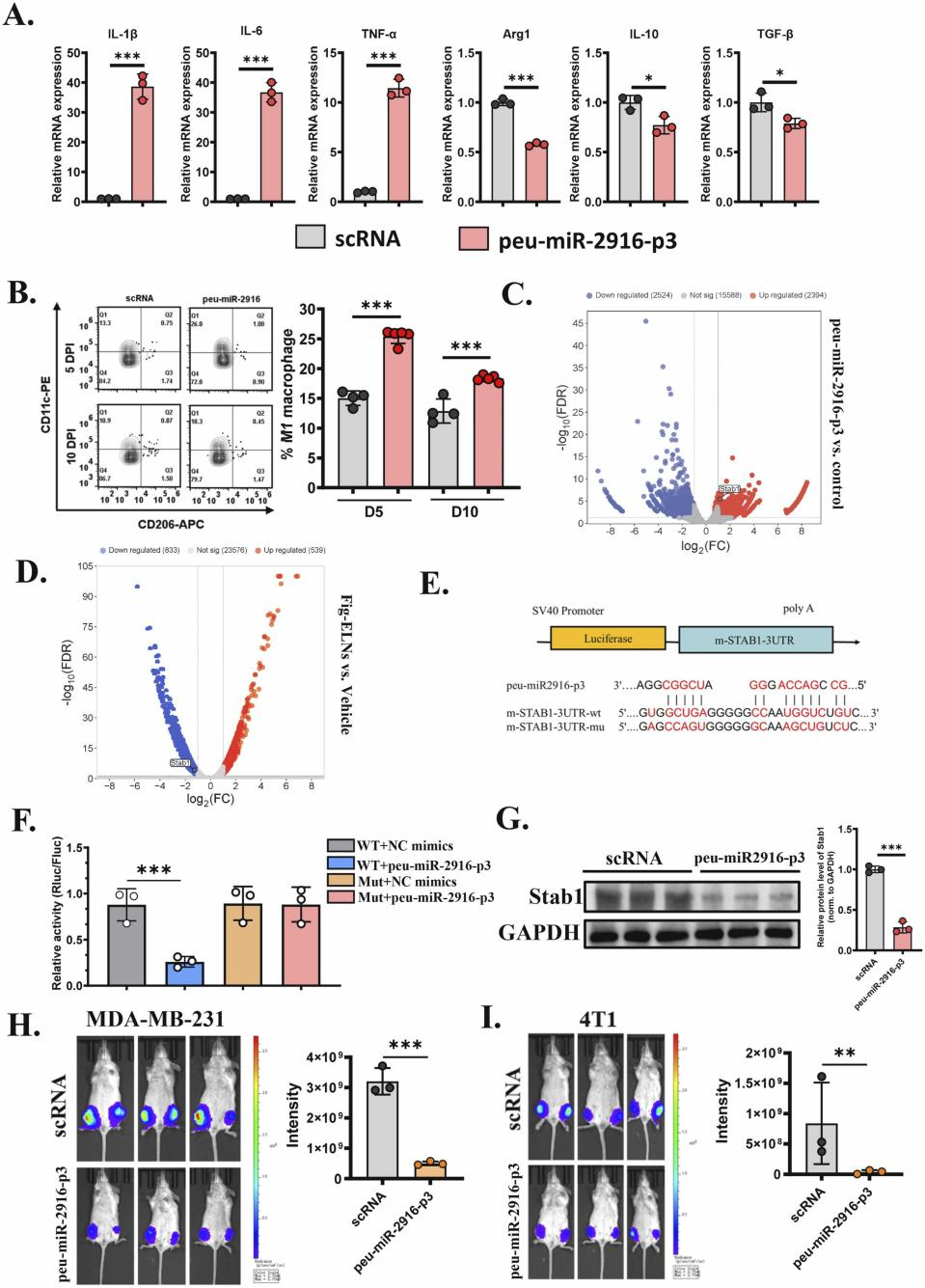
图5. peu-miR-2916-p3通过靶向RN7SL1促进BC细胞的凋亡
三、核心结果总结
|
研究维度 |
核心发现 |
|
Fig-ELNs特征 |
粒径100–200 nm,富含蛋白及RNA,可被乳腺癌细胞及巨噬细胞摄取 |
|
体内分布与安全性 |
腹腔注射后可到达骨组织,主要脏器无明显毒性 |
|
抗骨转移疗效 |
显著降低骨转移荷瘤小鼠肿瘤负荷,减轻溶骨性破坏 |
|
直接抑瘤机制 |
上调RN7SL1降解,抑制人乳腺癌细胞周期进程,诱导凋亡 |
|
免疫调节机制 |
靶向Stab1,激活非经典NF-κB通路,诱导M1型巨噬细胞极化 |
|
关键活性分子 |
peu-miR-2916-p3,丰度最高,同时介导直接抑瘤及M1极化效应 |
四、总结与展望
本研究首次从植物外泌体样纳米颗粒的角度,揭示了传统中药无花果抗肿瘤作用的现代生物学机制。Fig-ELNs及其携带的peu-miR-2916-p3通过双靶点、双途径协同抑制乳腺癌骨转移:既直接作用于肿瘤细胞,又重塑骨转移微环境中的免疫格局。该研究不仅为乳腺癌骨转移提供了兼具生物安全性与治疗潜力的候选策略,也为植物来源外泌体在肿瘤免疫治疗领域的应用开辟了新思路。
未来研究需进一步探索peu-miR-2916-p3的规模化制备工艺、体内递送效率优化及临床转化可行性。同时,RN7SL1及Stab1作为乳腺癌及肿瘤相关巨噬细胞的潜在干预靶点,亦值得深入挖掘。
参考文献:
Wang DD, Qian J, Zou HZ, et al. Fig-derived exosome-like nanoparticles attenuating bone metastasis of breast cancer through establishing an anti-tumor microenvironment. Pharmacol Res. 2026 Feb;224:108088.
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










