一文读懂EMSA技术核心要点,让“emsa” 秒变“easy”
“电泳迁移率变动分析法”或“凝胶迁移实验”(Electrophoretic Mobility Shift Assay, EMSA)是一种用于研究蛋白质-DNA或蛋白质-RNA相互作用的技术。通过EMSA,研究人员可以检测特定蛋白质是否能够特异性地结合到DNA或RNA序列上,从而揭示基因表达调控中的关键机制。EMSA技术广泛应用于生物学和医学研究领域,特别是在基因表达调控、疾病机理研究以及药物靶点发现等方面。
实验原理
EMSA是用核酸探针和样本蛋白混合孵育,样本中的核酸-蛋白质复合物在聚丙烯酰胺凝胶的迁移速度会慢于游离的探针并形成一条滞后带,根据凝胶上滞后带的有无和多少来定量DNA结合蛋白的有无和结合活性。EMSA是一种简单、快速、可定性与定量的体外蛋白质与DNA相互作用检测方法,且适用于未经纯化的蛋白与纯化的重组蛋白。
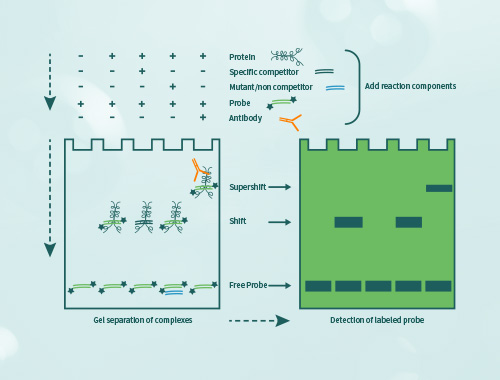
实验步骤
EMSA技术的操作流程主要包括以下几个步骤:
●根据研究目的设计特异性探针实验组以及非特异性对照组;
●将设计好的探针与样本蛋白混合孵育,形成蛋白-探针复合物;
●进行聚丙烯酰胺凝胶电泳,并将蛋白-探针复合物转移到膜上;
●在膜上检测、曝光成像,观察蛋白-探针复合物的位置,从而判断是否有蛋白与目标探针有互作。
案例展示及结果解析
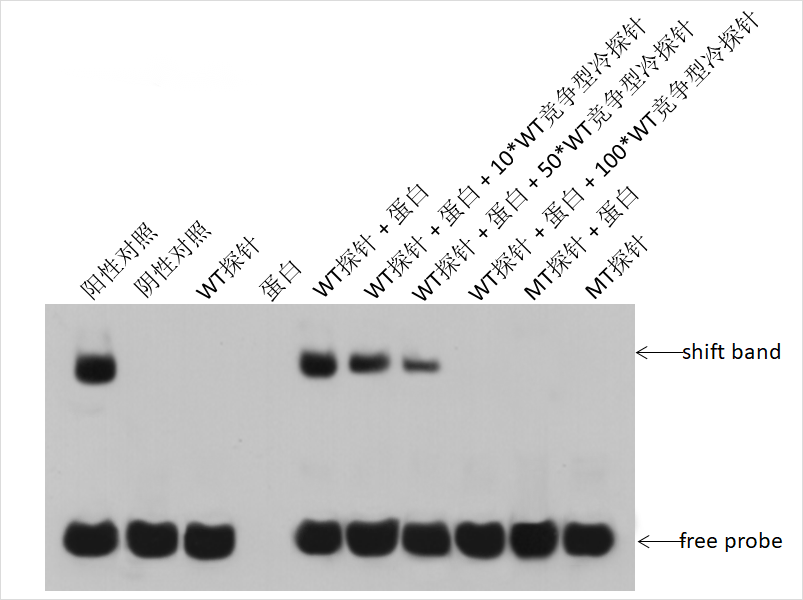
●EMSA实验检测的是生物素信号,即生物素标记的探针,因此通常最下方会出现一列探针条带;
●在同时加入蛋白与WT探针,且两者可以结合的情况下,探针由于结合了蛋白,电泳速率下降,因此会在上方出现迁移条带;
●竞争型冷探针是序列与WT探针一致但没有生物素标记的探针,因此虽然其也能与蛋白结合,但无法被检测到,因此随着竞争型探针上样量增多,迁移条带会变浅或消失;
●MT探针是结合位点序列突变后的WT探针,由于无法再与蛋白结合,所以没有出现迁移条带;有时突变后也会出现迁移条带,说明突变的序列不对,或突变不完全,需要重新设计突变探针;
●有时泳道中不仅会加入蛋白与WT探针,还会额外加入能够结合蛋白的抗体,由于迁移速率进一步被影响,会在常规迁移条带上方再出现另一条迁移条带,称为“超迁移”。
常见问题分析
尽管EMSA是一种强大的实验工具,但在实际操作过程中也存在一些常见问题,如非特异性结合、信号背景过强就让不少科研同胞头疼不已,下面我们一起来看看它们是什么原因造成的,方便大家逐一排查,各个击破。
1.看不到迁移带是什么原因?
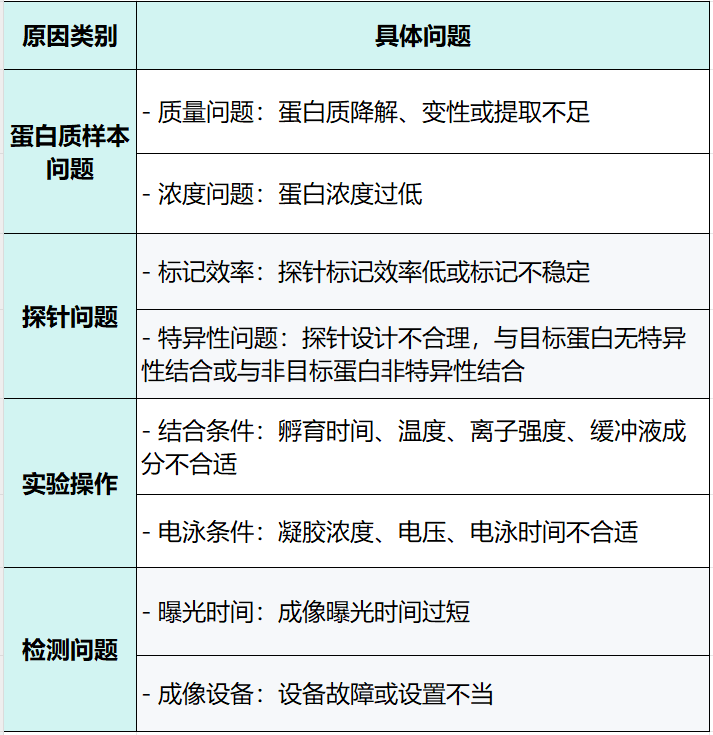
2.实验背景高的原因分析
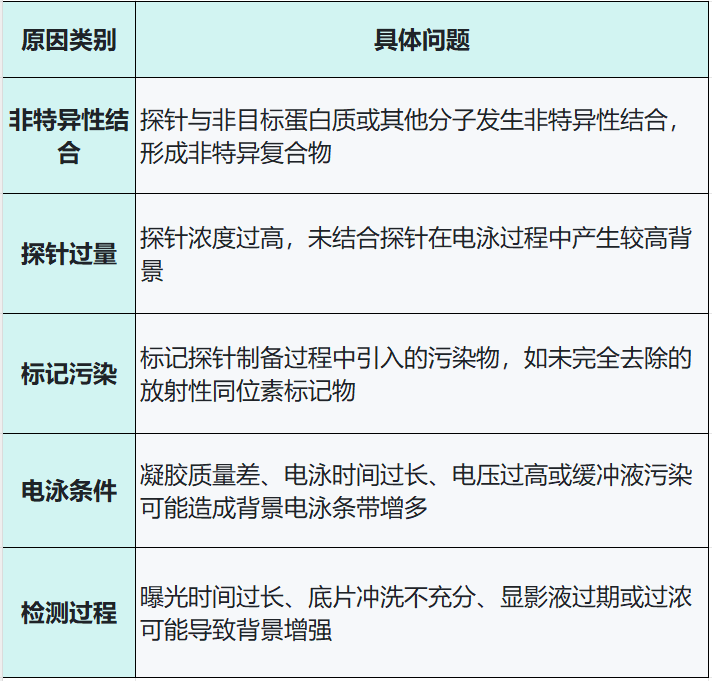
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










