CRISPR触发的内源Oct4或Sox2基因位点染色质重塑激活细胞重编程
信息来源:金开瑞 作者:genecreate 发布时间:2018-03-07 13:58:39
题目:CRISPR-Based Chromatin Remodeling of the Endogenous Oct4 or Sox2 Locus Enables Reprogramming to Pluripotency
期刊:Cell stem cell
影响因子:23.394
主要技术:CRISPR-dCas9-VP64激活系统、诱导性多能干细胞构建、原代细胞制作、iPS鉴定
研究背景
终末分化的成体细胞逆分化,形成多能干细胞状态的过程称为细胞重编程(Cell reprogramming)。在2006年,日本科学家山中伸弥(Shinya Yamanaka)发表诱导性多能干细胞(iPS, induced pluripotent stem cells)构建技术,利用逆转录病毒,把OSKM(OCT4, SOX2,KLF4 and C-myc)四因子在体细胞中进行超表达,成功把小鼠胚胎成纤维细胞诱导形成多能干细胞,开辟了一个全新的干细胞研究领域。随着研究的深入,人皮肤成纤维细胞、T淋巴细胞等也被成功诱导成多能干细胞。而这些多能干细胞与供体DNA是保持一致的,且有分化成多种细胞的潜力,展现出非常广阔的临床应用前景。如把人血液中的T淋巴细胞逆分化形成多能干细胞后,当定向分化技术成熟时, iPS能被有序分化成需要的细胞,比如心肌细胞、神经细胞等。
染色体上重要的基因启动子位点的表观遗传学变化,如DNA甲基化水平变化、组蛋白乙酰化水平变化、染色质重塑等,开启重要基因如OCT4, SOX2等的内源性表达,是iPS诱导过程中至关重要的事件,直接关系到诱导是否成功。
CRISPR-Cas9系统作为一种强大的基因编辑工具,现今已广泛用于常规的细胞或者个体的基因敲除、基因敲入、点突变外。当CAS9蛋白进行失活改造以及结构域添加后,得到CRISPR-dCas9-SunTag-VP64系统,则能实现特异基因转录激活。CRISPR-dCas9内源基因激活技术(SunTag Gene Activation),正好与iPS诱导技术完美契合,解决了激活内源OSKM四基因的问题,从而诞生了新型的iPS构建策略(见图1)。
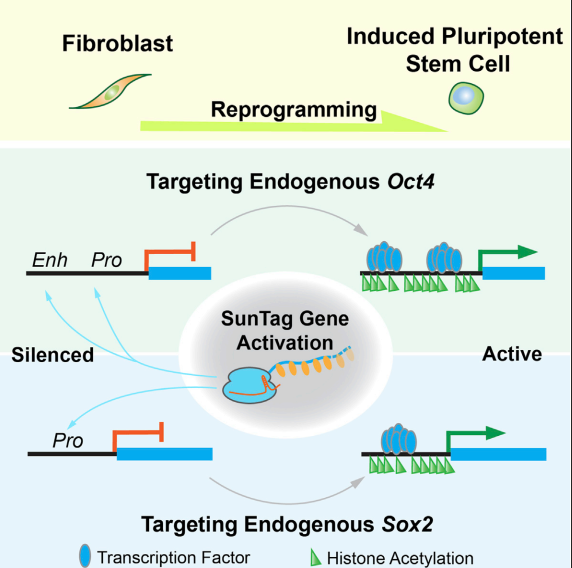
图1. 利用CRIPR-dCas9基因激活系统的iPS诱导策略
研究内容及结果
1. 设计定位于Sox2和Oct4基因启动子区和Oct4增强子区的sgRNA,利用CRISPR-dCas9-SunTag-VP64对Sox2和Oct4进行激活。
本研究首先设计了相应基因靶标的SgRNA,启动子区或者增强子区靶标位置考虑因素包括:sgRNA靶标位置与重要的转录因子(OCT4、SOX2、NANOG)结合位点、组蛋白乙酰转移酶p300结合位点的距离,靶标区附近组蛋白乙酰化分布、DNA甲基化分布等。并以MEF细胞为材料,在RNA水平检测了不同sgRNA对靶标基因sox2和oct4的激活效果(图2)。
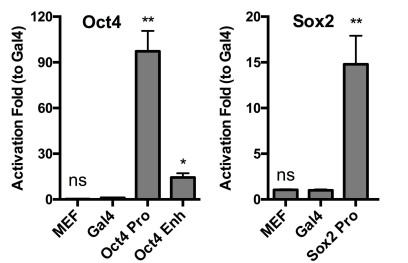
图 2. MEF细胞中,Sox2和Oct4基因启动子区和Oct4增强子区不同sgRNA的转录激活效果验证实验
2. CRISPR-dCas9-SunTag-VP64系统对重要基因进行内源激活,能成功获得iPS.
随后,同样使用此方法,利用筛选出来18个有效sgRNA,分别激活7个重要基因: Oct4, Sox2, Klf4, c-Myc, Nr5a2, Glis 1, Cebpa。将MEF利用病毒感染方法进行18 sgRNA导入后,与dCas9-SunTag-VP64形成复合体,激活了OG2-MEF中相应内源基因的表达,经过17天的诱导后,成功得到了iPS细胞,并稳定传代,且显示出与胚胎干细胞相同的克隆形态。通过免疫荧光和QPCR,显示得到的iPS表达Nanog, Sox2和SSEA-1,相关干细胞基因表达水平与RI胚胎干细胞相比,均相当或者超过。此部分证明CRISPR-dCas9-SunTag-VP64系统进行内源激活时,能成功实现iPS诱导(图3)。
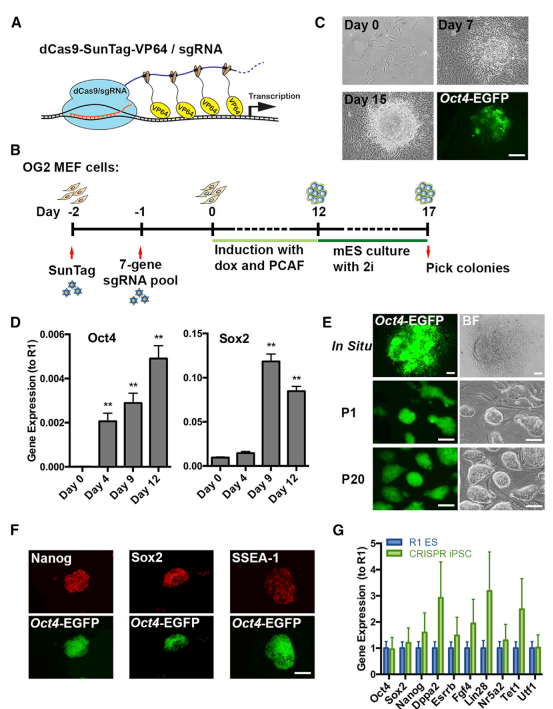
图3. CRISPR-dCas9-SunTag-VP64系统同时激活Oct4, Sox2, Klf4, c-Myc, Nr5a2, Glis 1, Cebpa内源表达时,能成功实现iPS诱导
3. CRISPR-dCas9-SunTag-VP64系统单独对Sox2基因进行内源激活,也能有效获得iPS
研究者单独选取了能对Sox2进行激活的SgRNA进行iPS诱导,发现在有效激活内源Sox2基因表达的情况下,能成功得到诱导性多能干细胞,并能稳定增殖传代。得到iPS通过体内体外实验,如干细胞基因表达情况检测实验(免疫荧光、qPCR等)、囊胚注射实验等,在囊胚注射实验后,还得到了嵌合体小鼠,并能稳定地生殖传递,后代中得到OG2小鼠品系的小鼠。这些实验证明了iPS细胞系的完整干性:稳定自我更新能力和多向分化能力(图4)。
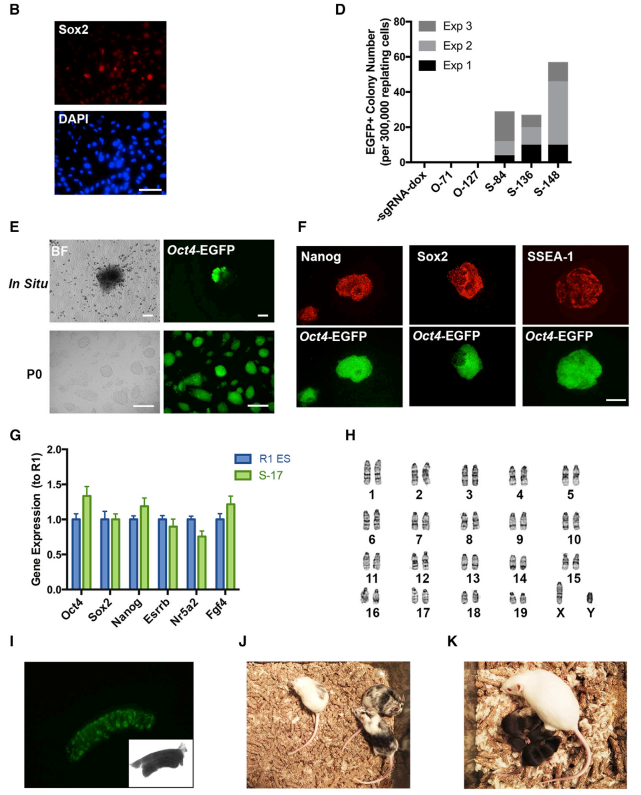
图4. CRISPR-dCas9-SunTag-VP64系统单独激活Sox2内源表达时,能成功实现iPS诱导
4. CRISPR-dCas9-SunTag-VP64系统同时对Oct4基因启动子区和增强子区进行内源激活,能有效获得iPS
接下来,研究者选取靶标位置为Oct4启动子区或者增强子区的sgRNA进行诱导实验,发现单独利用Oct4启动子区的sgRNA或者增强子区sgRNA对Oct4基因进行激活时,虽然表达激活,但内源强度无法得与胚胎干细胞系R1相比。在诱导过程中,单独的sgRNA无法得到iPS。Oct4启动子区的sgRNA或者增强子区sgRNA进行组合时,内源Oct4表达强度得到了很好的提升,最终得到iPS,并能稳定增殖传代。得到iPS通过体内体外实验,如干细胞基因表达情况检测实验(免疫荧光、qPCR等)、囊胚注射实验等,在囊胚注射实验后,还得到了嵌合体小鼠,并能稳定地生殖传递,后代中得到OG2小鼠品系的小鼠。这些实验证明了iPS细胞系的完整干性:稳定自我更新能力和多向分化能力(图5)。
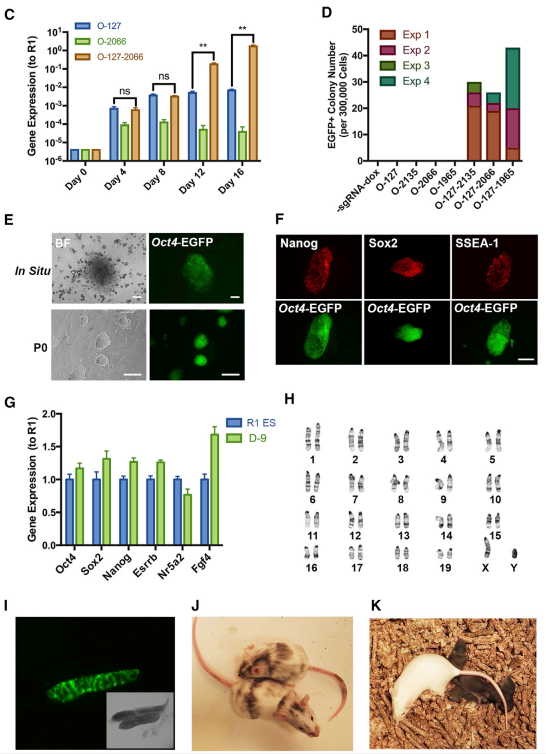
图 5. CRISPR-dCas9-SunTag-VP64系统同时对Oct4基因启动子区和增强子区进行内源激活能有效获得iPS
文章小结
作为利用CRISPR-dCas9激活系统进行iPS构建,作者非常有力地证明了CRISPR-dCas9-SunTag-VP64系统对构建iPS的有效性。可以预见,后续的MEF直接诱导形成心肌细胞、神经细胞的研究中,此系统很可能也有一席之地。此文章既进行了相关技术方法探索,也回答了一个非常好的科学问题:iPS诱导过程中,相关内源基因的表观遗传学变化直观重要。
在表观遗传学研究中,CRIPSR-dCas9激活内源基因表达的应用,会相对广泛一些。CRISPR-dCas9-SunTag-VP64系统稍加改进,很可能是直接改变相关基因表观遗传学特征的利器。
解析文献
P. Liu, M. Chen, Y. Liu, L.S. Qi, S. Ding. CRISPR-Based Chromatin Remodeling of the Endogenous Oct4 or Sox2 Locus Enables Reprogramming to Pluripotency, Cell stem cell, 22 (2018) 252-261.
参考文献
1. Black, J. B., Adler, A. F., et al. (2016) Targeted Epigenetic Remodeling of Endogenous Loci by CRISPR/Cas9-Based Transcriptional Activators Directly Converts Fibroblasts to Neuronal Cells. Cell stem cell 19, 406-414
2Chakraborty, S., Ji, H., Kabadi, A. M., et al. (2014) A CRISPR/Cas9-based system for reprogramming cell lineage specification. Stem cell reports 3, 940-947
3. Chavez, A., Scheiman, J., et al. (2015) Highly efficient Cas9-mediated transcriptional programming. Nature methods 12, 326-328
4. Thakore, P. I., D'Ippolito, A. M., et al. (2015) Highly specific epigenome editing by CRISPR-Cas9 repressors for silencing of distal regulatory elements. Nature methods 12, 1143-1149
5. Buganim, Y., Faddah, D. A., et al. (2012) Single-cell expression analyses during cellular reprogramming reveal an early stochastic and a late hierarchic phase. Cell 150, 1209-1222
6.Takahashi, K., and Yamanaka, S. (2006) Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell 126, 663-676
上一条:噬菌体展示技术解析
下一条:三维基因组(Hi-C)技术解析
最新动态
-
05.12
【高分文献】金开瑞ChIP试剂盒助力解密ETV4—结直肠癌肝转移的核心“枢纽”
-
05.12
分子互作只做Co-IP?试试分子对接+SPR+降解验证
-
05.12
分子动力学模拟(MD)结果怎么读?这份图表解读指南请收好!
-
05.12
最新研究:苹果来源纳米囊泡可重塑肠道菌群代谢、抑制胶质细胞炎症反应,成为肠-脑轴正向调节剂!
-
04.20
分子对接从入门到进阶:“这5张图你必须看懂”!
-
04.20
siRNA实验从入门到精通:合成与转染的那些“坑”你踩过吗?
-
04.20
酵母文库构建技术解析:如何高效筛选功能基因?
-
04.20
【客户文献分享IF:33】重庆医科大学赵金秋团队揭示肝内胆管癌免疫逃逸新机制:YAP通过转录抑制RNF125重塑肿瘤免疫微环境
-
04.20
国自然倒计时:蛋白互作研究还在只做Co-IP?这8种技术让评审专家“无刺可挑”
-
04.20
研究合集:中草药囊泡-生姜/白术/黄芪/半夏/鱼腥草/无花果/铁皮石斛等-36个经典案例!










